PubMed URL:https://pubmed.ncbi.nlm.nih.gov/40965042/
タイトル:Impact of Simultaneous Initiation of Finerenone and Empagliflozin on Urinary Albumin-to-Creatinine Ratio in Asia: Pre-Specified Analysis of CONFIDENCE
<概要(意訳)>
序論
地球上の約80億人のうち、62%がアジアに居住している。アジアにおける2型糖尿病の患者数は増加しており、糖尿病を有する全世界の人々の60%以上がアジアに居住し、そのほぼ半数が中国とインドに集中している。CKDは2型糖尿病の一般的な合併症であり、介入がなければアジアの人々の間でさらに増加すると予測されている。社会人口統計指標が低い地域では、2型糖尿病に関連するCKDの有病率、罹患率、および死亡率が高い。集団間では、食事、活動レベル、環境、遺伝、および人体計測的因子に相当なばらつきが存在しうる。これらの因子は疾患リスクの異質性に寄与しており、さらに、薬物動態および薬力学における民族地理的差異が治療転帰にも影響を及ぼす可能性がある。近年の文献では、臨床試験集団におけるより大きな多様性と、多様な患者群における治療効果をよりよく理解し一般化するための集団特性のより包括的な報告の必要性が強調されているが、ランダム化比較試験におけるアジア人の割合はしばしば少ない。
非ステロイド性ミネラルコルチコイド受容体拮抗薬(MRA)であるフィネレノンとナトリウム・グルコース共輸送体2阻害薬(SGLT2阻害薬)の併用投与により、相加的な治療効果が期待される。CKDおよび2型糖尿病を有する参加者におけるフィネレノンとエンパグリフロジンの併用効果をUACRエンドポイントを用いて評価するCONFIDENCE試験は、SGLT2阻害薬であるエンパグリフロジンとフィネレノンの同時開始が、アンジオテンシン変換酵素阻害薬(ACE阻害薬)またはアンジオテンシン受容体拮抗薬(ARB)を基礎治療とした上で、180日目のアルブミン尿減少においていずれの単剤よりも優れていることを示した。フィネレノンとエンパグリフロジンの同時開始は、フィネレノンまたはエンパグリフロジン単剤療法と比較して、UACRのより大きな減少をもたらした。この試験は、アジア、欧州、北米にまたがる大規模な参加者コホートで実施された。主要解析では、180日目の併用療法によるUACR低下がフィネレノン単独またはエンパグリフロジン単独よりも有意に大きいことが示された(差はそれぞれ29%および32%、いずれもP < 0.001)。主要報告のサブグループ解析では、試験のすべての地域間で主要有効性アウトカムに一貫性があることが報告された。
ここでは、全体試験集団の46%を占めたCONFIDENCEアジア参加者における事前規定された参加者レベルの探索的サブグループ解析を報告する。主解析と同様に、併用療法の安全性と有効性をいずれかの単剤と比較した。
方法
試験デザイン
CONFIDENCE試験(NCT05254002)は、CKDおよび2型糖尿病を有する患者において、フィネレノンとエンパグリフロジンの併用の有効性と安全性を、フィネレノン単独またはエンパグリフロジン単独と比較して評価する第2相二重盲検ランダム化3群間試験であった。試験デザインとベースライン特性は以前に報告されており、ここでは簡潔に記述する。本試験は14ヵ国/地域で実施され、そのうち4ヵ国がアジア(インド、日本、韓国、台湾)であり、残りの10ヵ国は欧州および北米であった。本試験は各施設の治験審査委員会により承認された。本試験はヘルシンキ宣言の原則に従って実施された。すべての参加者が文書によるインフォームドコンセントを提供した。
参加者
本解析はアジアからのサブグループを報告する。18歳以上で2型糖尿病(糖化ヘモグロビン[HbA1c] <11%)、eGFR 30~90 mL/min/1.73 m²、およびアルブミン尿(UACR 100~5000 mg/g)を有する個人が登録された。除外基準には、1型糖尿病および血清カリウム>4.8 mmol/Lが含まれた。すべての参加者は、スクリーニング時点でRAS阻害薬(ACE阻害薬またはARB)の臨床的最大耐用量を1ヵ月以上服用していることが必要であり、スクリーニング前8週間以内にSGLT2阻害薬またはカリウム結合薬を服用していてはならなかった。
手順
参加者は1:1:1の比率で、フィネレノン10または20 mg 1日1回(およびエンパグリフロジン対応プラセボ)、エンパグリフロジン10 mg 1日1回(およびフィネレノン対応プラセボ)、または両薬の併用に無作為に割り付けられた。
試験薬投与期間は180日間であった。安全性および有効性評価は、投与開始後14、30、90、180、および210日目に予定された診察時に実施された。併用可能な治療薬として、インスリン、インスリン分泌促進薬、チアゾリジンジオン、ACE阻害薬、ARB、ループ利尿薬、サイアザイド系利尿薬、およびグルカゴン様ペプチド-1受容体作動薬(GLP-1 RA)が許容された。
尿検体および血液検体は、UACR、血清カリウム、およびeGFRの評価のために試験期間中の診察時に採取された。血圧も各診察時に測定された。有害事象はMedDRAを用いてコード化された。
アウトカム
主要有効性アウトカムは、ベースラインから180日目までの対数変換平均UACRの変化であった。副次有効性アウトカムには、投与終了後30日目(210日目)のベースラインからのUACR変化、および180日目のUACR減少が30%超、40%超、50%超を達成した参加者の割合が含まれた。副次安全性アウトカムには、ベースラインからのeGFR、血清カリウム、および収縮期血圧の変化、ならびに有害事象、臨床検査データ、バイタルサイン、および高カリウム血症イベントが含まれた。
統計解析
有効性解析は最大の解析対象集団(FAS)を用いて実施された。FASは、すべてのランダム化された参加者から、誤ってランダム化され試験薬を服用しなかった参加者、およびGCP(医薬品の臨床試験の実施の基準)が正しく遵守されなかった参加者を除外したものであった。主要有効性アウトカムには反復測定混合モデルが使用され、治療群、受診、治療と受診の交互作用、2つの層別因子(UACRカテゴリーおよびeGFRカテゴリー)、対数変換UACR ベースライン値、および対数変換UACRベースライン値と受診の交互作用が因子として含まれた。併用療法群は、最小二乗(LS)平均の対比比から導出されたパーセント差と両側95%信頼区間(CI)を算出することにより、単剤療法群と比較された。eGFR値の算出にはCKD-EPI式が使用され、日本人参加者には修正版の式が使用された。eGFR、血清カリウム、および収縮期血圧の変化は、主要有効性アウトカムと同様の方法で解析され、反復測定混合モデルを用いたLS平均の算出が行われた。安全性解析は安全性解析対象集団で実施され、試験薬を少なくとも1回服用したすべてのランダム化参加者が含まれた。
結果
参加者
CONFIDENCE試験では、2022年6月23日から2024年8月14日までに合計1,664人の参加者がスクリーニングを受け、800人がランダム化されてFASを構成した。アジアでは、スクリーニングを受けた708人の候補者のうち360人がFASに含まれた(図1):インド132人(37%)、日本76人(21%)、韓国104人(29%)、台湾48人(13%)(表1)。アジア集団は以下のように試験薬に割り付けられた:併用療法群(n=113)、フィネレノン群(n=123)、エンパグリフロジン群(n=124)。表1に示すように、アジア参加者のベースライン特性は3群間で一貫していた。平均(±SD)年齢は64±11歳、平均(±SD)eGFRは53±17 mL/min/1.73 m²、平均(±SD)HbA1cは7.3%±1.2%であった。4人を除くすべての参加者(356/360人、99%)がベースラインでACE阻害薬またはARBを服用していた。
補足表1はアジア参加者と欧州/北米参加者のベースライン特性を示している。アジアの参加者は年齢が若く(平均64歳 vs 69歳)、平均体重が低く(70.4 vs 91.4 kg)、平均BMIが低く(26.2 vs 31.8 kg/m²)、平均収縮期血圧が低く(133 vs 137 mmHg)、UACR中央値が高く(663 vs 504 mg/g)、1000 mg/g以上のアルブミン尿の割合が多かった(32% vs 23%)。アジアの参加者はアテローム性動脈硬化性心血管疾患(ASCVD)が少なく(21% vs 34%)、一方で平均HbA1c値はアジアと欧州/北米で同程度であった。スタチン(63% vs 84%)および抗血小板薬(30% vs 48%)の使用率はアジアの方が低かった。糖尿病治療薬の使用パターンも異なり、アジアの参加者ではインスリンおよびGLP-1 RAの使用が少ないが、ジペプチジルペプチダーゼ-4(DPP-4)阻害薬およびスルホニル尿素薬などのインスリン分泌促進薬の使用が多かった。さらに、降圧薬の使用パターンも異なり、欧州/北米と比較してアジアの参加者では利尿薬およびβ遮断薬の使用が少なく、カルシウム拮抗薬の使用が多かった。
表1:アジア参加者の人口統計学的データおよびベースライン特性
|
ベースライン特性 |
フィネレノン+エンパグリフロジン |
フィネレノン |
エンパグリフロジン |
全体 |
|
N(%) |
113(31) |
123(34) |
124(34) |
360(100.0) |
|
年齢(歳)、平均±SD |
66±11 |
63±10 |
63±10 |
64±11 |
|
男性、n(%) |
91(80.5) |
100(81.3) |
95(76.6) |
286(79.4) |
|
国別、n(%) |
||||
|
インド |
34(30) |
53(43) |
45(36) |
132(37) |
|
日本 |
32(28) |
20(16) |
24(19) |
76(21) |
|
韓国 |
34(30) |
33(27) |
37(30) |
104(29) |
|
台湾 |
13(12) |
17(14) |
18(15) |
48(13) |
|
ベースラインeGFR(mL/min/1.73 m²)、平均±SD |
51±16 |
54±18 |
53±16 |
53±17 |
|
UACR(mg/g)、中央値(IQR) |
645(336-1003) |
738(292-1653) |
654(362-1233) |
663(327-1291) |
|
アルブミン尿の重症度、n(%) |
||||
|
<300 mg/g |
21(19) |
31(25) |
26(21) |
78(22) |
|
300~<1000 mg/g |
63(56) |
41(33) |
60(48) |
164(46) |
|
≧1000 mg/g |
28(25) |
50(41) |
38(31) |
116(32) |
|
ASCVD、n(%) |
23(20) |
24(20) |
30(24) |
77(21) |
|
体重(kg)、平均±SD |
68.8±12.7 |
71.6±14.2 |
70.6±12.7 |
70.4±13.2 |
|
身長(cm)、平均±SD |
163.2±8.3 |
164.4±7.6 |
163.9±8.9 |
163.9±8.3 |
|
BMI(kg/m²)、平均±SD |
25.8±3.8 |
26.4±4.2 |
26.3±4.1 |
26.2±4.0 |
|
収縮期血圧(mmHg)、平均±SD |
132.7±14.0 |
132.4±11.9 |
133.3±12.0 |
132.8±12.6 |
|
血清カリウム(mmol/L)、平均±SD |
4.5±0.4 |
4.5±0.5 |
4.6±0.4 |
4.5±0.4 |
|
HbA1c(%)、平均±SD |
7.2±1.2 |
7.3±1.3 |
7.3±1.2 |
7.3±1.2 |
|
併用薬、n(%) |
||||
|
インスリン |
25(22) |
31(25) |
42(34) |
98(27) |
|
メトホルミン |
70(62) |
78(63) |
78(63) |
226(63) |
|
GLP-1 RA |
15(13) |
11(9) |
14(11) |
40(11) |
|
DPP-4阻害薬 |
64(57) |
70(57) |
70(57) |
204(57) |
|
インスリン分泌促進薬 |
57(50) |
48(39) |
32(26) |
137(38) |
|
ACE阻害薬またはARB |
113(100) |
122(99) |
121(98) |
356(99) |
|
降圧薬 |
113(100) |
122(99) |
122(98) |
357(99) |
|
β遮断薬 |
29(26) |
37(30) |
27(22) |
93(26) |
|
カルシウム拮抗薬 |
81(72) |
82(67) |
80(65) |
243(68) |
|
利尿薬 |
26(23) |
31(25) |
17(14) |
74(21) |
|
抗血小板薬 |
36(32) |
37(30) |
35(28) |
108(30) |
|
スタチン |
75(66) |
81(66) |
72(58) |
228(63) |
eGFRはCKD-EPI式を用いて算出。日本人参加者には修正版の式を使用。ASCVDはMedDRA version 27.0でコード化。
Clin J Am Soc Nephrol. 2026 Jan 1;21(1):72-82.
主要エンドポイント
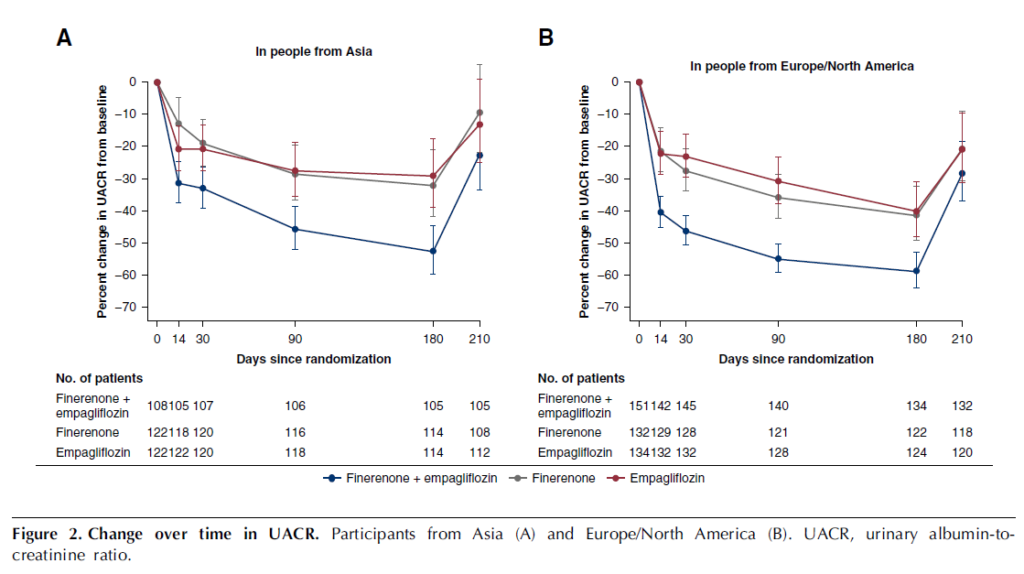
アジア参加者のベースラインのUACR中央値(四分位範囲)は、併用療法群で645(336~1003)mg/g、フィネレノン群で738(292~1653)mg/g、エンパグリフロジン群で654(362~1233)mg/gであった。無作為化後180日目において、333人のアジア参加者のUACRデータが利用可能であった(表2)。180日目において、アジア参加者の併用療法によるベースラインからのUACR低下は53%(95%CI 44%~60%)であった(表2)。この低下はフィネレノン単独よりも30%大きく(95%CI 12%~45%、P = 0.003)、エンパグリフロジン単独よりも34%大きかった(95%CI 16%~47%、P < 0.001)。
180日目において、欧州/北米参加者の併用療法によるベースラインからのUACR低下は56%(95%CI 49%~62%)であった(表2)。この低下はフィネレノン単独よりも29%大きく(95%CI 12%~43%、P = 0.002)、エンパグリフロジン単独よりも31%大きかった(95%CI 15%~44%、P < 0.001)。
表2:180日目および210日目のベースラインからのUACR変化(アジアおよび欧州/北米)
|
時点 |
併用療法(%[95%CI]) |
フィネレノン(%[95%CI]) |
エンパグリフロジン(%[95%CI]) |
併用 vs フィネレノン(%[95%CI]) |
|
アジア |
||||
|
180日目 |
n=105 -53(-60~-44.2) |
n=114 -33(-43~-21) |
n=114 -29(-40~-17) |
-30(-45~-12) P=0.003 |
|
210日目 |
n=105 -22(-34~-9.3) |
n=108 -11(-24~3) |
n=112 -14(-26~-0.1) |
-12(-29~9) |
|
欧州/北米 |
||||
|
180日目 |
n=134 -56(-62~-49) |
n=122 -39(-47~-28) |
n=124 -37(-46~-26) |
-29(-43~-12) P=0.002 |
|
210日目 |
n=132 -24(-33~-13) |
n=118 -16(-27~-4) |
n=120 -16(-27~-3) |
-9(-25~10) |
UACR低下レスポンダー解析
|
閾値 |
地域 |
治療群 |
レスポンダー/総数 |
オッズ比(95%CI) |
|
>30%低下 |
アジア |
併用 |
77/106 |
|
|
アジア |
フィネレノン |
54/114 |
3.02(1.71~5.31) |
|
|
アジア |
エンパグリフロジン |
56/114 |
2.84(1.61~5.00) |
|
|
欧州/北米 |
併用 |
91/134 |
||
|
欧州/北米 |
フィネレノン |
69/122 |
1.63(0.98~2.72) |
|
|
欧州/北米 |
エンパグリフロジン |
67/124 |
1.82(1.09~3.02) |
|
|
>40%低下 |
アジア |
併用 |
67/106 |
|
|
アジア |
フィネレノン |
47/114 |
2.48(1.44~4.27) |
|
|
アジア |
エンパグリフロジン |
43/114 |
2.88(1.66~4.99) |
|
|
欧州/北米 |
併用 |
87/134 |
||
|
欧州/北米 |
フィネレノン |
57/122 |
2.11(1.28~3.49) |
|
|
欧州/北米 |
エンパグリフロジン |
60/124 |
1.97(1.19~3.25) |
|
|
>50%低下 |
アジア |
併用 |
53/106 |
|
|
アジア |
フィネレノン |
37/114 |
2.11(1.22~3.65) |
|
|
アジア |
エンパグリフロジン |
30/114 |
2.85(1.62~5.03) |
|
|
欧州/北米 |
併用 |
78/134 |
||
|
欧州/北米 |
フィネレノン |
47/122 |
2.22(1.35~3.67) |
|
|
欧州/北米 |
エンパグリフロジン |
46/124 |
2.35(1.42~3.89) |
Clin J Am Soc Nephrol. 2026 Jan 1;21(1):72-82.
副次有効性および安全性エンドポイント
図2はUACRの経時的変化を示している。併用療法群の参加者のUACRは、14日後にベースラインから31%低下し、90日後にベースラインから46%低下した。投与終了から30日後のフォローアップ(210日目)では、3群すべてでUACRが上昇した(図2および表2)。さらに、アジアおよび欧州/北米の参加者において、併用療法群では、フィネレノンまたはエンパグリフロジン単独よりも多くの割合の参加者がUACRの30%超、40%超、または50%超の低下を達成した(図2および表2)。
補足図1は、アジアおよび欧州/北米の参加者における血清カリウム値のベースラインからのLS平均変化の経時的推移を示している。フィネレノンとエンパグリフロジン併用中は平均血清カリウム値がベースラインから上昇し、試験薬投与終了30日後(210日目)にベースライン付近に回復した。フィネレノン群でも、投与中に平均血清カリウム値がベースラインから上昇し、210日目にベースライン付近に回復した。エンパグリフロジン群ではベースラインからの血清カリウム値の大きな変化は認められなかった。
補足図2は、アジアおよび欧州/北米の参加者における収縮期血圧のベースラインからのLS平均変化の経時的推移を示している。フィネレノンとエンパグリフロジンの併用は、投与中のベースラインからの収縮期血圧低下と、投与中止後30日間(180日目から210日目)の引き続く上昇と関連していた。収縮期血圧の変化は、フィネレノン群およびエンパグリフロジン群でも同様のパターンを示したが、併用群よりも変化は小さかった。
補足図3は、アジアおよび欧州/北米の参加者におけるeGFRのベースラインからのLS平均変化の経時的推移を示している。エンパグリフロジン群および併用群では早期のeGFR低下が観察され、この低下の大部分は180日目の投与中止後30日間で回復した。14日目において、eGFRの低下はアジアの参加者では欧州/北米の参加者と比較して小さかった。
有害事象
欧州/北米の参加者と比較して、全般的にアジアの参加者では有害事象の発現率が数値的に低かった(41% vs 61%)。また、有害事象による投与中止(1% vs 6%)、重篤な有害事象(3% vs 9%)、および重篤な有害事象による投与中止(0% vs 2%)もアジアでより低かった。有害事象の発現率は3群すべてで同程度であった(表3)。いずれかの有害事象を報告した参加者の割合は3群で38%~44%の範囲であり、重篤な有害事象は参加者の2%~4%で報告された。1件の重篤な有害事象が参加者の死亡に至った(エンパグリフロジン群の心臓死)が、治療関連の重篤な有害事象や試験薬中止に至った重篤な有害事象はなかった。
アジア参加者における治療下で発現した高カリウム血症有害事象の割合は10%であり、アジア以外の7%と比較して高かった。アジアでは、併用療法群で11%、フィネレノン単独で14%、エンパグリフロジン単独で5%に治験責任医師により高カリウム血症が報告された。治療下で発現した高カリウム血症有害事象が入院、試験薬の永久中止、または死亡に至ったものはなかった。検査値による高カリウム血症(血清カリウム>5.5 mmol/L)も、欧州/北米(11%)と比較してアジアの参加者(19%)で高頻度であり、軽度の高カリウム血症(血清カリウム>5.5~≦6.0 mmol/L;16% vs 10%)および中等度の高カリウム血症(血清カリウム>6.0 mmol/L;6.7% vs 2%)が含まれた(表4)。対照的に、30日目のeGFR低下>30%は、欧州/北米の参加者(5%)と比較してアジアの参加者(3%)で数値的に低頻度であった。
表3:アジアおよび欧州/北米の参加者における治療開始後の有害事象
|
治験責任医師報告のAE |
併用療法 (n=112) |
フィネレノン (n=123) |
エンパグリフロジン (n=124) |
合計 (N=359) |
|
いずれかのAE、n(%) |
43(38) |
51(42) |
54(44) |
148(41) |
|
投与中止に至ったAE、n(%) |
2(2) |
2(2) |
0(0) |
4(1) |
|
いずれかの重篤なAE、n(%) |
4(4) |
2(2) |
5(4) |
11(3) |
|
投与中止に至った重篤なAE、n(%) |
0(0) |
0(0) |
0(0) |
0(0) |
|
死亡に至ったAE、n(%) |
0(0) |
0(0) |
1(0.8) |
1(0.3) |
|
高カリウム血症、n(%) |
12(11) |
17(14) |
6(5) |
35(10) |
|
尿路敗血症または腎盂腎炎、n(%) |
0(0.0) |
0(0.0) |
1(0.8) |
1(0.3) |
高カリウム血症は、試験薬を少なくとも1回服用し、初回投与後から永久または一時的中止3日後までに発症または悪化した治験責任医師報告の事象。
表4:アジアおよび欧州/北米の参加者における安全性アウトカム
|
安全性評価項目 |
併用療法 |
フィネレノン |
エンパグリフロジン |
合計 |
|
アジア |
||||
|
血清K>5.5 mmol/L、n/N(%) |
23/111(21) |
32/122(26) |
13/121(11) |
68/354(19) |
|
血清K>5.5~≦6.0 mmol/L、n/N(%) |
18/111(16) |
29/122(24) |
11/121(9) |
58/354(16) |
|
血清K>6.0 mmol/L、n/N(%) |
9/112(8) |
11/123(9) |
4/124(3) |
24/359(7) |
|
30日目のeGFR低下>30%、n/N(%) |
6/112(5) |
2/123(2) |
2/124(2) |
10/359(3) |
|
性器真菌感染症、n/N(%) |
0/112(0.0) |
0/123(0.0) |
0/124(0.0) |
0/359(0.0) |
|
症候性低血圧、n/N(%) |
0/112(0.0) |
0/123(0.0) |
0/124(0.0) |
0/359(0.0) |
|
急性腎障害、n/N(%) |
0/112(0.0) |
0/123(0.0) |
0/124(0.0) |
0/359(0.0) |
eGFRはCKD-EPI式を用いて算出。日本人参加者には修正版の式を使用。
Clin J Am Soc Nephrol. 2026 Jan 1;21(1):72-82.
考察
本CONFIDENCEアジア参加者(n=360)の探索的参加者レベルサブグループ解析において、欧州/北米の参加者と比較して臨床特性に差異が認められた。フィネレノンとエンパグリフロジンの併用療法は、180日目のUACR低下において、フィネレノンまたはエンパグリフロジン単剤療法よりも臨床的にも統計的にも優れていた。地理的分布(アジア vs 欧州/北米)と単剤療法に対する併用療法の利益との間に交互作用は認められなかった。高カリウム血症を除き、有害事象率はアジアの参加者で欧州/北米よりも低かった。実際、検査値による高カリウム血症はアジアでより高頻度であったが、急性eGFR低下はより低頻度であった。アジア参加者の有害事象率は3群間で同程度であり、高カリウム血症有害事象が試験薬中止に至ったものはなかった。
本CONFIDENCEアジアサブグループ解析の知見は、全体試験集団で観察されたものと一致しており、地域間での治療効果の一貫性を示した先行の知見を拡張するものである。アジアサブグループのベースライン特性の多くはCONFIDENCE試験全体集団と同等であったが、いくつかの差異が認められた。これらには、アジアの参加者ではより若い年齢、より多いアルブミン尿、より少ないASCVD、およびスタチン・抗血小板薬の使用頻度の低さが含まれ、降圧薬および糖尿病治療薬の使用パターンにもアジアサブグループとCONFIDENCE全体集団の間で差異が認められた。
アジアサブグループの主要解析では、180日目の併用療法によるUACR低下がフィネレノン単独よりも30%大きく、エンパグリフロジン単独よりも34%大きかった。これらの割合はCONFIDENCE全体集団の対応する値(それぞれ29%および32%)と類似している。この類似度は、上述の参加者のベースライン特性の差異および本試験では測定されていないさらなる差異(例:遺伝、食事、社会経済的因子)にもかかわらず、併用療法の治療効果の一貫性を示している。フィネレノンとエンパグリフロジンのアジアにおける継続的な評価は重要であるが、これらの知見は、主にまたは部分的に他の集団で実施された試験の結果が適用可能であることを示唆している。
CONFIDENCEは、CKDでアルブミン尿を伴う2型糖尿病患者におけるSGLT2阻害薬とフィネレノンの同時開始を評価した。CKDおよび2型糖尿病患者におけるフィネレノン試験であるFIDELIO-DKDおよびFIGARO-DKDの統合解析(FIDELITY)シリーズでは、フィネレノンはベースラインまたは試験薬投与と同時にSGLT2阻害薬を使用しているかどうかにかかわらず心血管および腎有害アウトカムを減少させ、これらの治療薬の併用に関する新たな安全性の懸念は生じなかった。FIDELITYのアジア参加者の知見はFIDELITY全体集団と一致していた。フィネレノンはまた、ベースラインでSGLT2阻害薬を使用している参加者(37%減少)と使用していない参加者(31%減少)で4ヵ月目のUACRをベースラインから減少させた(P交互作用 = 0.17)。本試験は、フィネレノンとSGLT2阻害薬によるUACR低下がアジア人においても独立的かつ相加的であることを確認した。
フィネレノンおよびSGLT2阻害薬の両方で観察されるように、薬剤開始に対するeGFRの短期的変化は、腎機能の長期的な悪化とは一致しない。すなわち、初期数週間の大きなeGFR低下が、その後数年間の大きなeGFR損失を予測するものではない(また、大きな初期低下がなくても長期的な低下が生じうる)。さらに、これらの変化はフィネレノン、エンパグリフロジン、またはその併用の中止後にeGFRがベースラインに向かって回復する傾向があることから、大部分が可逆的であり、eGFRの変化は腎臓の構造的変化ではなく血行動態的なものであることが示唆される。しかし、フィネレノン治療によるUACRの初期低下は、先行のメディエーション解析において、eGFRの悪化を含む臨床的腎アウトカムに対するフィネレノンの治療効果の大部分(84%)を媒介することが報告された。さらに、UACRおよび収縮期血圧の変化は、フィネレノンの心血管効果の50%を共同で媒介すると考えられている。エンパグリフロジンについては、先行のメディエーション解析により、ヘマトクリット、HbA1c、収縮期血圧、および遊離脂肪酸の組み合わせが複合腎アウトカムに対する治療効果の大部分(79%)を媒介することが示された。
2型糖尿病およびCKDを有する人々における心血管および腎罹患率の高さを考慮すると、フィネレノンとエンパグリフロジンの併用は疾患負担の大幅な軽減を可能にしうる。これは、糖尿病患者数が憂慮すべき増加を示しているアジアにとって特に重要である。2型糖尿病およびCKDの世界的な大きな疾患負担は、CONFIDENCEで評価されたような併用療法の同時開始を含む、包括的なガイドラインに基づく薬物療法の日常的な採用を支持している。
糖尿病およびCKDのガイドラインで推奨されているように、2型糖尿病患者のUACRを年1回測定することは、腎疾患の同定に役立ちうる。2型糖尿病の治療開始後のUACRおよび収縮期血圧のより頻回なモニタリングは、治療効果を示し、治療アドヒアランスを促進するのに役立つ。これらの手段は治療アドヒアランスを促進し、eGFRの維持に寄与することで、このハイリスク集団における腎臓および心血管アウトカムの最適化に貢献しうる。
家庭血圧モニタリングによる収縮期血圧低下の早期検出は、利尿薬またはジヒドロピリジン系カルシウム拮抗薬の適時な用量調整を可能にし、低血圧、体液量減少、およびeGFR低下などの関連有害事象の予防に役立ち、併用療法の中止のきっかけとなりうる。このアプローチにより、臨床医は必要に応じて用量を減量または延期でき、特に虚弱な集団において転倒、急性eGFR低下、およびその他の合併症のリスクを最小化できる。
本解析は、CONFIDENCEのアジア参加者における大部分の有害事象の発現率が欧州/北米の参加者よりも数値的に低かったことを示した。治療関連有害事象についてはアジアサブグループ vs 欧州/北米参加者で約50%の減少であり、有害事象による投与中止率や重篤な有害事象率ではさらに大きな減少が見られた。これらの差異の理由は明確ではないが、いくつかの可能性がある。欧州/北米と比較して、アジアの参加者はより若く、ASCVDが少なく、BMIが低く、収縮期血圧が低かった。同様のHbA1cにもかかわらず、インスリン使用が少なく、糖尿病がより軽度であることが示唆された。さらに、有害事象報告に対する参加者の意欲に影響する文化的差異が寄与した可能性もある。全般的な有害事象率のパターンとは対照的に、高カリウム血症はアジアの治験責任医師によりより高頻度に報告され、中央検査室モニタリングでも高頻度の高カリウム血症が確認された。高カリウム血症有害事象の発現率はFIDELITYでもアジアサブグループで非アジア諸国と比較してより高頻度であったが、FIDELITYでは血清カリウム>5.5 mmol/Lまたは>6.0 mmol/Lの頻度にアジアと非アジアサブグループ間で差はなかった。アジアおよび欧州/北米のCONFIDENCE参加者の結果は、高カリウム血症有害事象の発現率がフィネレノンとエンパグリフロジンの併用でフィネレノン単独よりも低かったことを示した。この高カリウム血症の軽減は、ベースラインでMRAを服用している参加者を含め、SGLT2阻害薬による重度高カリウム血症リスクの低下を報告した先行のメタ解析と一致している。
CKD患者では、ジャガイモ、豆類、緑黄色野菜など、アジアの食事に一般的なカリウムを豊富に含む食品が血清カリウムを弱く上昇させる可能性があるが、食事性カリウムと高カリウム血症の全体的な関連は限定的であり、ホールフードからのカリウムの生体利用率は加工食品や塩代替物からのものよりも低いことが多い。アルブミン尿の多さや利尿薬使用の少なさなどの他の因子が高カリウム血症のリスク因子であり、民族性よりも重要である可能性がある。利尿薬の併用はアジアの参加者(21%)で欧州/北米(49%)と比較して低く、これがアジアサブグループにおける高カリウム血症率の上昇および初期eGFR低下の低さに寄与した可能性がある。KDIGO(Kidney Disease: Improving Global Outcomes)は腎疾患患者のカリウム値の評価と管理に関するグローバルガイダンスを公表しているが、このガイダンスにはアジア人集団に対する特別な考慮事項は含まれていない。
本試験の主な強みは、アジアからの参加者数が多いこと、この地域の複数の国が含まれていること、およびランダム化二重盲検デザインであることである。限界としては、参加者の遺伝的または社会経済的プロファイリングの欠如(全体試験集団との比較のため)、およびアジアサブグループにおける治療効果を統計的に測定するための検出力が十分でないサブグループ解析に固有の限界が含まれる。われわれはまた、アジア内の異なる国または地域間での結果の異質性の可能性を認識しており、これにはアジア集団に含まれる4ヵ国間の差異も含まれる。残念ながら、CONFIDENCE試験のサンプルサイズは、このレベルでの差異の意味のある評価には十分ではなかった。
結論として、本試験はフィネレノンとエンパグリフロジンの併用療法が、CKDおよび2型糖尿病を有するアジアの人々において、いずれの単剤療法よりもUACR低下に効果的であることを示した。この治療のリスク・ベネフィットプロファイルは、CONFIDENCE試験の全体国際集団と同様に、アジアの参加者においても良好であると考えられた。アジア参加者の有害事象および重篤な有害事象はより少なく、高カリウム血症のリスクは参加者の地理的起源よりも臨床的因子に関連している可能性がある。
日本の医療への適用(訳者追記)
※以下は原文にない追加情報であり、日本の臨床現場への示唆として付記する。
1. 日本のガイドラインとの整合性
本試験の知見は、日本腎臓学会CKD診療ガイドライン2024および日本糖尿病学会糖尿病診療ガイドライン2024の方向性と一致している。両ガイドラインはCKDを伴う2型糖尿病患者に対してRAS阻害薬を基盤とした治療にSGLT2阻害薬の追加を推奨しており、フィネレノンについても新規エビデンスとして位置づけられている。本試験は日本人76人を含むアジア集団での解析であり、ガイドライン改訂の根拠となりうるエビデンスを提供している。
2. 保険診療での実施可能性
エンパグリフロジン(ジャディアンス)は日本において2型糖尿病、慢性心不全、およびCKDに対する保険適応を有している。フィネレノン(ケレンディア)も2型糖尿病を伴うCKDに対して承認されている。したがって、両薬の併用は日本の保険診療の枠組み内で実施可能である。ただし、本試験で認められた高カリウム血症のリスク上昇(アジアで19% vs 欧州/北米で11%)を考慮すると、血清カリウムの頻回モニタリングが重要であり、特に利尿薬の併用が少ない日本人患者ではその必要性が高い。
3. 日本人での再現性
日本人参加者76人(全アジア参加者の21%)が含まれているが、日本人単独のサブグループ解析は実施されていない。しかし、アジア全体の結果(UACR低下:併用 vs フィネレノン単独 30%差、併用 vs エンパグリフロジン単独 34%差)は全体集団と高い一貫性を示しており、日本人においても同様の効果が期待される。日本人患者の特徴として、欧米と比較して体重が軽く(70.4 vs 91.4 kg)、DPP-4阻害薬の使用頻度が高く(57%)、インスリン使用が少ない(27%)という差異があるが、これらの差異にもかかわらず治療効果の一貫性が示されたことは臨床的に重要である。
🎧 耳で聴きたい方はこちら
長い記事なので、音声でもお楽しみいただけます(2倍速・約25分)