PubMed URL:https://pubmed.ncbi.nlm.nih.gov/41358899/
タイトル:Cardiovascular Disease and Risk Management: Standards of Care in Diabetes-2026
<概要(意訳)>
序論
心血管疾患(CVD)は、動脈硬化性心血管疾患(ASCVD)と心不全という、糖尿病患者に多い2つのCVDを含む広範な用語である。ASCVDは広義には、急性冠症候群、心筋梗塞(MI)、安定または不安定狭心症、冠動脈または他の動脈血行再建術、脳卒中、大動脈瘤を含む末梢動脈疾患(PAD)の既往を指し、糖尿病患者における罹患率と死亡率の主要原因である。糖尿病自体が独立したASCVDリスクを付与し、糖尿病患者では高血圧、脂質異常症、肥満を含むすべての主要な心血管リスク因子が集積し、高頻度に認められる。
多くの研究により、個々の心血管リスク因子の管理が糖尿病患者におけるASCVDの予防または進行抑制に有効であることが示されている。さらに、複数の心血管リスク因子(血糖、血圧、脂質管理)を同時に対処することで大きなベネフィットが得られ、長期的なベネフィットのエビデンスも存在する。特筆すべきは、糖尿病における心血管リスク低減のための介入を支持するエビデンスの大部分が2型糖尿病患者を対象とした試験からのものである点である。1型糖尿病患者における心血管リスク低減戦略の影響を評価するために特別にデザインされた無作為化試験は存在しない。したがって、1型糖尿病患者に対する心血管リスク因子修正の推奨は2型糖尿病患者から得られたデータから外挿され、2型糖尿病患者に対するものと同様である。
現在の包括的リスク因子修正のパラダイムの下、心血管の罹患率と死亡率は1型および2型糖尿病患者の両方で顕著に減少している。実際、すべての主要な心血管リスク因子が目標範囲内に治療されている場合、2型糖尿病患者の死亡、MI、または脳卒中のリスクは一般集団と同等である。これらの罹患率と死亡率を低減する励みとなる機会があるにもかかわらず、推奨されるリスク因子目標を達成し、ガイドラインで推奨される治療を受けている2型糖尿病患者はごく少数に留まっている。したがって、本セクションで概説される治療推奨を実践するためには、質の高い包括的な心血管ケアの提供とリスク因子管理への障壁への対処に継続的に注力する必要がある。
心不全の定義と分類
CVDには心不全も含まれ、糖尿病は心不全発症のリスク因子であり、糖尿病患者における心不全の有病率は糖尿病のない人と比較して少なくとも2倍高く、罹患率と死亡率の主要原因となっている。糖尿病患者は幅広いスペクトラムの心不全を呈する可能性があり、駆出率が保たれた心不全(HFpEF)、駆出率が軽度低下した心不全(HFmrEF)、または駆出率が低下した心不全(HFrEF)が含まれる。過体重・肥満や高血圧を含む併存疾患は、しばしばHFpEFの発症に先行し、HFpEFの病態生理に関与しているとされている。冠動脈疾患は虚血性心疾患における心筋障害の主要なリスク因子かつ原因であり、HFrEFにつながる。さらに、糖尿病患者は閉塞性冠動脈疾患がない状態でも構造的心疾患およびHFrEFを発症するリスクがある。糖尿病患者における心不全の病態生理、ならびに心不全と糖尿病を有する人のスクリーニング、診断、治療の詳細は、米国糖尿病学会(ADA)の以前のコンセンサスステートメントにも記載されている。
心腎代謝疾患の概念
ASCVD、心不全、慢性腎臓病(CKD)を含む、心血管と腎臓の両方における有害アウトカムにつながる心代謝リスク因子の共通の病態生理と相互関係についての認識が高まっている。これら3つの併存疾患は、しばしば肥満とその関連リスク因子によって駆動される代謝リスクによって引き起こされ、3つの疾患すべての発生率はA1C値の上昇とともに増加する。これらの併存疾患の組み合わせは総称して、心腎代謝疾患または心血管-腎臓-代謝の健康と呼ばれている。
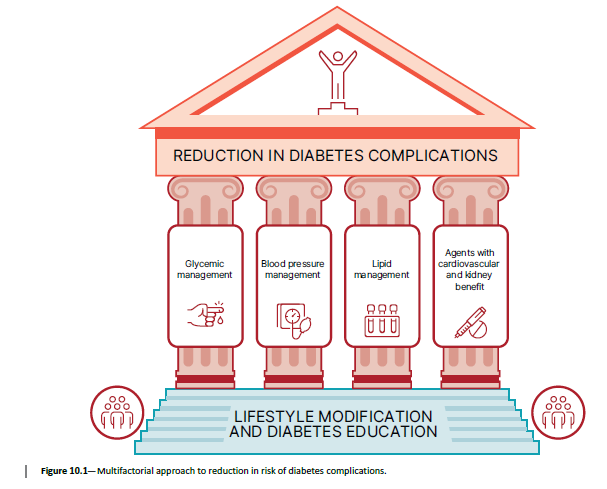
糖尿病患者の管理において心血管と腎臓の併存疾患を同時に考慮する理由には、共通の代謝リスクだけでなく、ナトリウム-グルコース共輸送体(SGLT)阻害薬またはグルカゴン様ペプチド-1受容体作動薬(GLP-1 RA)で治療された2型糖尿病患者において、CVD、心不全、腎臓アウトカムの全スペクトラムにわたって観察される主要なベネフィットも含まれる。したがって、高血糖、高血圧、高脂血症の管理に加えて、心血管および腎臓ベネフィットが実証されたSGLT阻害薬および/またはGLP-1 RAによる治療は、リスク低減の基本要素であり、2型糖尿病患者の心血管および腎臓アウトカムを改善するためのコア薬物療法戦略と考えられている(図10.1)。図10.1:糖尿病合併症リスク低減への多因子的アプローチ
|
【図10.1の構成】 基盤層:生活習慣の改善と糖尿病教育 4本の柱(左から右へ): 1. 血糖管理 2. 血圧管理 3. 脂質管理 4. 心血管・腎保護ベネフィットを持つ薬剤 屋根(アウトカム):糖尿病合併症の減少 |
Diabetes Care. 2026 Jan 1;49(Supplement_1):S216-S245.
高血圧と血圧管理
血圧上昇は、収縮期血圧120〜129 mmHgかつ拡張期血圧<80 mmHgと定義される。高血圧は、収縮期血圧≧130 mmHgまたは拡張期血圧≧80 mmHgと定義される。これは米国心臓病学会および米国心臓協会による高血圧の定義と一致している。高血圧は1型および2型糖尿病患者に多い。高血圧はASCVD、心不全、および細小血管合併症の主要なリスク因子である。さらに、多くの研究により、降圧療法がASCVDイベント、心不全、および細小血管合併症を減少させることが示されている。高血圧の疫学、診断、治療の詳細なレビューについてはADAのポジションステートメント「糖尿病と高血圧」、および高血圧ガイドラインの推奨を参照されたい。妊娠中の糖尿病患者の血圧目標と管理については、詳細は第15章「妊娠中の糖尿病管理」を参照されたい。
スクリーニングと診断
|
推奨事項 10.1 血圧は、すべての定期的な臨床診察時に、または少なくとも6か月ごとに測定すべきである。高血圧の診断がない血圧上昇(収縮期血圧120〜129 mmHgかつ拡張期血圧<80 mmHg)が認められた場合は、高血圧を診断するために別の日の測定を含む複数回の測定で血圧を確認すべきである。 高血圧は、2回以上の機会に得られた2回以上の測定の平均に基づき、収縮期血圧≧130 mmHgまたは拡張期血圧≧80 mmHgと定義される。 A 血圧≧180/110 mmHgかつ心血管疾患を有する患者は、単回診察で高血圧と診断しうる。 E |
|
10.2 高血圧と糖尿病を有するすべての人に、適切な教育後に家庭での血圧モニタリングを勧める。 A |
血圧は、すべての定期的な臨床診察時に、または少なくとも6か月ごとに、一般集団に対して確立されたガイドラインに従うよう訓練を受けた者により測定すべきである:座位で、足は床につけ、腕は心臓の高さで支持し、5分間の安静後に測定する。カフサイズは上腕周囲径に適切なものとする。血圧上昇または高血圧が確認された場合は、高血圧を診断するために別の日の測定を含む複数回の測定で血圧を確認すべきである。ただし、CVDを有し血圧≧180/110 mmHgの患者では、単回診察で高血圧を診断することは合理的である。血圧と脈拍の体位変化は自律神経障害のエビデンスである可能性があり、したがって血圧目標の調整を必要とする。臥位、座位、立位の血圧測定は初回診察時に、また適宜確認すべきである。
家庭血圧自己モニタリングおよび24時間自由行動下血圧モニタリングは、白衣高血圧、仮面高血圧、またはその他の診察室血圧と真の血圧との乖離のエビデンスを提供しうる。高血圧の診断の確認または除外に加えて、家庭血圧評価は降圧治療のモニタリングに有用でありうる。前向き研究の系統的レビューとメタ解析により、24時間自由行動下血圧または家庭血圧測定のいずれからの血圧測定も心血管リスクを予測できると結論づけられた。さらに、家庭血圧モニタリングは服薬行動を改善し、心血管リスクの低減に役立つ可能性がある。
治療目標
|
推奨事項 10.3 糖尿病と高血圧を有する人では、心血管リスク、降圧薬の潜在的な有害作用、および個人の好みに配慮した共同意思決定プロセスを通じて血圧目標を個別化すべきである。 B |
|
10.4 安全に達成可能であれば、治療中の血圧目標は<130/80 mmHgであり、心血管または腎リスクが高い人では収縮期血圧目標<120 mmHgが推奨される。 A |
無作為化臨床試験により、高血圧の治療が心血管イベントおよび細小血管合併症を減少させることが疑いなく実証されている。糖尿病患者における特定の血圧目標の推奨については議論がある。糖尿病患者における血圧目標<130/80 mmHgを支持する推奨は、米国心臓病学会および米国心臓協会、国際高血圧学会、欧州心臓病学会/欧州高血圧学会の血圧/高血圧ガイドラインと一致している。Strategy of Blood Pressure Intervention in the Elderly Hypertensive Patients(STEP)試験の参加者の約20%が糖尿病患者であり、収縮期血圧目標<130 mmHgへの高血圧治療で心血管イベントの減少が認められた。
厳格降圧療法 vs 標準降圧療法の無作為化比較試験
BPROAD試験
BPROADは、収縮期血圧治療目標<120 mmHgを支持する最も強力なエビデンスを提供しており、ベースライン収縮期血圧≧140 mmHg(すでに降圧薬服用中の場合は130〜180 mmHg)の2型糖尿病患者で心血管リスクが上昇している患者を登録した。心血管リスク上昇の定義は、登録の少なくとも3か月前のCVD既往、無症候性CVD、2つ以上の心血管リスク因子、およびCKD(推算糸球体濾過量[eGFR] 30〜<60 mL/min/1.73 m²)であった。
|
登録者数 |
12,821人(2型糖尿病患者) |
|
試験デザイン |
オープンラベル無作為化試験、追跡期間最長5年 |
|
治療群 |
厳格治療群:目標収縮期血圧<120 mmHg vs 標準治療群:目標<140 mmHg |
|
達成血圧 |
厳格群121.6 mmHg vs 標準群133.2 mmHg |
|
一次エンドポイント |
非致死性脳卒中、非致死性MI、心不全の治療または入院、心血管死の複合 |
|
結果 |
厳格治療群で21%のリスク減少(HR 0.79、95%CI 0.69-0.90) |
|
有害事象 |
両群で同等、ただし症候性低血圧と高カリウム血症は厳格治療群でより高頻度 |
ESPRIT試験
ESPRIT試験は、2025年Standards of Care in Diabetesの策定以降に公表された、相当数の糖尿病患者を含む2番目の大規模血圧試験である。心血管リスクが高い(確立したCVDまたは2つのリスク因子を有する)11,255人を、厳格治療(目標収縮期血圧<120 mmHg)vs 標準治療(目標収縮期血圧<140 mmHg)に無作為化した。参加者の39%が2型糖尿病を有していた。
|
登録者数 |
11,255人(39%が2型糖尿病) |
|
一次エンドポイント |
MI、血行再建術、心不全入院、脳卒中、心血管死の複合 |
|
結果 |
厳格治療群で12%のリスク減少(HR 0.88、95%CI 0.78-0.99) |
|
ベースライン糖尿病との関係 |
ベースラインの糖尿病診断の有無にかかわらず効果を認めた |
|
有害事象 |
失神の軽度増加(0.4% vs 0.1%、HR 3.00、95%CI 1.35-6.68) |
SPRINT試験
SPRINTは2型糖尿病患者を除外したが、心血管リスクが上昇した人における血圧目標低下がアウトカムを改善するというBPROADとESPRITの知見を支持するエビデンスを提供している。この試験では、収縮期血圧≧130 mmHgかつ心血管リスクが上昇した9,361人を登録し、収縮期血圧目標<120 mmHg(厳格治療)vs 目標<140 mmHg(標準治療)に治療した。
|
登録者数 |
9,361人(糖尿病患者は除外) |
|
達成収縮期血圧 |
厳格群121 mmHg vs 標準群136 mmHg |
|
一次複合エンドポイント |
MI、急性冠症候群、脳卒中、心不全、心血管死 |
|
結果 |
厳格治療群で25%のリスク減少 |
|
有害事象 |
低血圧、失神、電解質異常、急性腎障害が厳格治療群でより高頻度 |
STEP試験
STEP試験は、60〜80歳の高血圧患者8,511人を収縮期血圧目標110〜<130 mmHg(厳格治療)または130〜<150 mmHg(標準治療)に割り付けた。この試験では約19%の参加者が糖尿病を有していた。一次複合エンドポイント(脳卒中、急性冠症候群、急性代償不全性心不全、冠動脈血行再建術、心房細動、心血管死)は、厳格治療群の3.5%に対し標準治療群では4.6%に発生した(HR 0.74、95%CI 0.60-0.92;P=0.007)。低血圧は厳格治療群(3.4%)で標準治療群(2.6%)より高頻度であったが、めまい、失神、骨折を含む他の有害事象に有意差はなかった。
ACCORD BP試験
ACCORD BPは、2型糖尿病患者4,733人を厳格治療(目標収縮期血圧<120 mmHg)または標準治療(目標収縮期血圧<140 mmHg)に無作為化した。達成された平均収縮期血圧は、厳格群で119 mmHg、標準群で133 mmHgであった。一次複合エンドポイント(非致死性MI、非致死性脳卒中、心血管死)は厳格治療群で有意に減少しなかったが、事前に規定された二次エンドポイントである脳卒中は厳格治療群で41%有意に減少した。血圧治療に起因する有害事象(低血圧、失神、徐脈、高カリウム血症、血清クレアチニン上昇)は、標準治療群より厳格治療群でより高頻度に発生した。ACCORD BPは、複合一次エンドポイントが血圧介入に対する感度が低かったため検出力不足と見なされている。
ADVANCE試験
Action in Diabetes and Vascular Disease: Preterax and Diamicron MR Controlled Evaluation(ADVANCE)試験では、2型糖尿病患者11,140人を、ペリンドプリルとインダパミドの固定配合剤または対応するプラセボの投与群に無作為化した。一次エンドポイント(心血管死、非致死性脳卒中またはMI、または新規もしくは増悪した腎疾患または眼疾患の複合)は、配合剤治療群で9%減少した。達成された収縮期血圧は、治療群で約135 mmHg、プラセボ群で140 mmHgであった。
HOT試験
Hypertension Optimal Treatment(HOT)試験では18,790人を登録し、拡張期血圧<90 mmHg、<85 mmHg、または<80 mmHgを目標とした。心血管イベント率(致死性または非致死性MI、致死性および非致死性脳卒中、およびすべての他の心血管イベントと定義)は、拡張期血圧目標間(≦90 mmHg、≦85 mmHg、および≦80 mmHg)で有意差はなかったが、心血管イベントの最も低い発生率は達成拡張期血圧82 mmHgで生じた。しかし、糖尿病患者では、目標拡張期血圧<80 mmHgの治療群で目標拡張期血圧<90 mmHgの治療群と比較して、MI、脳卒中、心血管死が51%有意に減少した。
治療目標の個別化
糖尿病患者と臨床医は、個々の血圧目標を決定するための共同意思決定プロセスに参加すべきである。厳格な血圧目標のベネフィットとリスクの徹底的なレビューは、個人の優先事項と医療専門家の判断を重視する、患者中心のケアアプローチと一致する。ACCORD BPとSPRINTの二次解析は、臨床因子が厳格な血圧管理からベネフィットを受ける可能性が高い人と、ベネフィットを受ける可能性が低い人を特定するのに役立つことを示唆している。
降圧による絶対ベネフィットは、SPRINTおよびより高いベースライン血圧で実施された以前の臨床試験における絶対的なベースライン心血管リスクと相関した。BPROADとESPRITの結果は、心血管リスクが高い人において治療中の収縮期血圧目標<120 mmHgを達成することが、収縮期血圧<140 mmHgと比較して心血管イベントの減少と関連することを強調している。これらのベネフィットは、低血圧や失神などの治療関連有害事象と比較検討すべきであり、これらは起立性低血圧、重大な併存疾患、機能制限、または多剤併用を有する高齢者や、生活の質を向上させるために高い血圧目標を好む一部の人々に特に関連する可能性がある。
生活習慣介入
生活習慣管理は、血圧を低下させ、一部の降圧薬の有効性を高め、代謝や血管の健康の他の側面を促進し、一般に有害作用が少ないため、高血圧治療の重要な要素である。生活習慣療法は、カロリー制限による余分な体重の減少(第8章「糖尿病の予防と治療のための肥満と体重管理」参照)、週に少なくとも150分の中強度有酸素運動(第3章「糖尿病と関連併存疾患の予防または遅延」参照)、ナトリウム摂取制限(<2,300 mg/日)、果物と野菜の摂取増加(8〜10食分/日)および低脂肪乳製品または非乳製品代替品(2〜3食分/日)、過度のアルコール摂取の回避(男性で1日2杯以下、女性で1日1杯以下)、および活動レベルの増加から構成される(第5章「健康アウトカムを改善するための前向きな健康行動とウェルビーイングの促進」参照)。
10件の無作為化比較試験の系統的レビューでは、対照食と比較して、修正DASHダイエットパターンが平均収縮期血圧(−3.26 mmHg、95%CI −5.58〜−0.94 mmHg;P=0.006)および拡張期血圧(−2.07 mmHg、95%CI −3.68〜−0.46 mmHg;P=0.01)を低下させることができると報告された。これらの生活習慣介入は、糖尿病および軽度の血圧上昇(収縮期>120 mmHgかつ拡張期<80 mmHg)を有する人に対して合理的であり、高血圧が診断された場合には薬物療法と同時に開始すべきである(図10.2)。生活習慣療法計画は糖尿病患者と協力して作成し、糖尿病管理の一環として話し合うべきである。健康的な行動を強化するためのインターネットまたはモバイルベースのデジタルプラットフォームの使用は、高血圧に対する薬物療法の有効性を高めることが認められているため、ケアの一要素として考慮されうる。
|
推奨事項 10.5 血圧>120/80 mmHgの糖尿病患者に対しては、必要に応じた減量、ナトリウム制限を含むDASH型食事パターン、アルコール摂取の制限または回避、身体活動の増加、禁煙を含む生活習慣行動を勧める。 A |
薬物療法
|
推奨事項 10.6 確定した診察室血圧≧130/80 mmHgの人では、個別化された血圧目標を達成するために薬物療法を開始し、漸増すべきである。 A 10.7 確定した診察室血圧≧150/90 mmHgの人では、生活習慣療法に加えて、糖尿病患者において心血管イベント減少が実証された2剤の降圧薬または単一製剤の配合剤を速やかに開始し、適時漸増すべきである。 A 10.8 高血圧治療には、糖尿病患者において心血管イベント減少が実証された薬剤クラスを含めるべきである。 A アルブミン尿または冠動脈疾患を有する糖尿病患者の高血圧には、ACE阻害薬またはアンジオテンシン受容体拮抗薬(ARB)が第一選択として推奨される。 A 10.9 血圧目標達成には一般に多剤併用療法が必要である。ただし、ACE阻害薬、ARB(ARBとネプリライシン阻害薬の配合剤を含む)、および直接レニン阻害薬のいかなる組み合わせも避ける。 A 10.10 非妊娠の糖尿病および高血圧患者において、中等度増加アルブミン尿(UACR 30〜299 mg/g クレアチニン)を有する場合にはACE阻害薬またはARBが推奨され B、高度増加アルブミン尿(UACR≧300 mg/g クレアチニン)および/または推算糸球体濾過量(eGFR)<60 mL/min/1.73 m²を有する場合には、腎疾患の進行予防と心血管イベント減少のために最大耐用量まで強く推奨される。 A 一方のクラスに忍容性がない場合は、他方に切り替えるべきである。 B 10.11 ACE阻害薬、ARB、およびミネラルコルチコイド受容体拮抗薬(MRA)使用時は、開始時および臨床的に適切な間隔でeGFR低下と血清カリウム上昇をモニタリングする。 B 利尿薬使用時は、定期診察時および開始後または用量変更後7〜14日、また臨床的に適切な間隔で低カリウム血症をモニタリングする。 B 10.12 確実な避妊を行っていない妊娠可能な性的活動を行う人では、妊娠中禁忌であるためACE阻害薬、ARB、MRA、直接レニン阻害薬、ネプリライシン阻害薬を避ける。 A |
降圧薬の初期投与数
糖尿病患者に対する初期治療は高血圧の重症度による(図10.2)。血圧が130/80 mmHgから150/90 mmHgの間の患者は単剤で開始してよい。血圧≧150/90 mmHgの患者では、血圧目標をより効果的に達成するために、2剤の降圧薬による初期薬物療法が推奨される。単一製剤の降圧配合剤は一部の人で服薬行動を改善する可能性がある。
降圧薬のクラス
高血圧の初期治療には、糖尿病患者において心血管イベント減少が実証された薬剤クラスのいずれかを含めるべきである:ACE阻害薬、ARB、サイアザイド系類似利尿薬、またはジヒドロピリジン系カルシウム拮抗薬。糖尿病および確立した冠動脈疾患を有する人では、高血圧に対してACE阻害薬またはARBが第一選択として推奨される。アルブミン尿(尿中アルブミン/クレアチニン比[UACR]≧30 mg/g)を有する人では、進行性腎疾患のリスクを低減するために、初期治療にACE阻害薬またはARBを含めるべきである(図10.2)。
ACE阻害薬またはARB療法を受けている人では、腎機能がeGFR<30 mL/min/1.73 m²まで低下した場合でも、腎不全のリスクを有意に増加させることなく心血管ベネフィットを提供しうるため、これらの薬剤の継続が可能である。アルブミン尿がない場合、進行性腎疾患のリスクは低く、ACE阻害薬およびARBはサイアザイド系類似利尿薬またはジヒドロピリジン系カルシウム拮抗薬と比較して優れた心保護効果を示していない。β遮断薬は心筋梗塞既往、活動性狭心症、またはHFrEFの状況では適応となるが、これらの状態がない場合には血圧降下薬として死亡率を減少させることは示されていない。
妊娠と降圧薬
妊娠中の血圧目標と治療に関する追加情報については、第15章「妊娠中の糖尿病管理」を参照されたい。妊娠中は、ACE阻害薬、ARB、直接レニン阻害薬、MRA、ネプリライシン阻害薬による治療は、胎児障害を引き起こす可能性があるため禁忌である。妊娠可能な人には特別な配慮が必要であり、妊娠を希望する人はACE阻害薬、ARB、レニン阻害薬、MRA、またはネプリライシン阻害薬から妊娠中使用が承認された代替降圧薬に切り替えるべきである。妊娠中に有効かつ安全であることが知られている降圧薬には、メチルドパ、ラベタロール、長時間作用型ニフェジピンがあり、ヒドララジンは妊娠中の高血圧または重症子癇前症の急性管理に考慮されうる。利尿薬は妊娠中の血圧管理には推奨されないが、容量管理に必要な場合は妊娠後期に使用されることがある。
多剤併用療法
血圧目標を達成するには多剤併用療法がしばしば必要であり(図10.2)、特に糖尿病患者のCKD存在下で顕著である。しかし、ACE阻害薬とARBの両方を併用すること、またはACE阻害薬もしくはARBと直接レニン阻害薬の併用は、追加のASCVDベネフィットがなく有害事象(高カリウム血症、失神、急性腎障害[AKI]など)の発生率が増加するため禁忌である。血圧目標達成における治療の遅れを克服するため、降圧薬の漸増および/または追加は適時行うべきである。
高カリウム血症と急性腎障害
ACE阻害薬、ARB、またはMRAによる治療はAKIおよび高カリウム血症を引き起こしうる一方、利尿薬は(作用機序により)AKIおよび低カリウム血症または高カリウム血症のいずれも引き起こしうる。ACE阻害薬またはARBによる血清クレアチニン上昇(ベースラインから最大30%まで)をAKIと混同してはならない。AKIは、血清クレアチニンの上昇および/または尿量減少を特徴とする、典型的には短期間(数時間から数日)での急速な腎機能低下と定義される。血清クレアチニンとカリウムは、ACE阻害薬、ARB、MRA、または利尿薬による治療開始後、および治療中とこれらの薬剤の増量後、特に糸球体濾過が低下した人ではモニタリングすべきである。AKIの詳細については、第11章「慢性腎臓病とリスク管理」を参照されたい。
抵抗性高血圧
抵抗性高血圧は、適切な生活習慣管理に加えて利尿薬と相補的作用機序を持つ他の2つの降圧薬を最大耐用量で使用する治療戦略にもかかわらず、血圧≧130/80 mmHgと定義される。抵抗性高血圧を診断する前に、降圧薬の服薬忘れ、白衣高血圧、一次性および二次性高血圧を含む他の多くの状態を除外すべきである。治療計画の遵守困難も抵抗性高血圧の原因となりうる。国際高血圧学会ガイドラインは、高血圧管理における治療計画遵守困難のスクリーニングを強く重視し、日常臨床において治療計画への関与の矛盾を検出するには主観的方法よりも客観的測定(処方記録のレビュー、錠剤カウント、血液または尿の化学分析など)を使用することを推奨している。ただし、すべての診療環境でこれが実行可能ではない場合がある。
糖尿病および確定した抵抗性高血圧を有する人は、原発性アルドステロン症、腎動脈狭窄、CKD、閉塞性睡眠時無呼吸などの二次性高血圧の原因について評価すべきである。一般に、服薬への障壁(費用や副作用など)を特定し対処すべきである(図10.2)。スピロノラクトンやエプレレノンを含むMRAは、2型糖尿病患者において、ACE阻害薬またはARB、サイアザイド系類似利尿薬、またはジヒドロピリジン系カルシウム拮抗薬による既存の治療への追加で、抵抗性高血圧の管理に有効である。さらに、MRAは糖尿病性腎症患者においてアルブミン尿を減少させる。しかし、ACE阻害薬またはARBを含む治療計画にMRAを追加すると高カリウム血症のリスクが増加する可能性があり、これらの人における血清クレアチニンとカリウムの定期的モニタリングの重要性が強調される。血圧管理におけるMRAの役割をより良く評価するには長期アウトカム研究が必要である。
|
推奨事項 10.13 3つのクラスの降圧薬(利尿薬を含む)で血圧目標を達成できない高血圧患者は、MRA療法を考慮すべきである。 A |
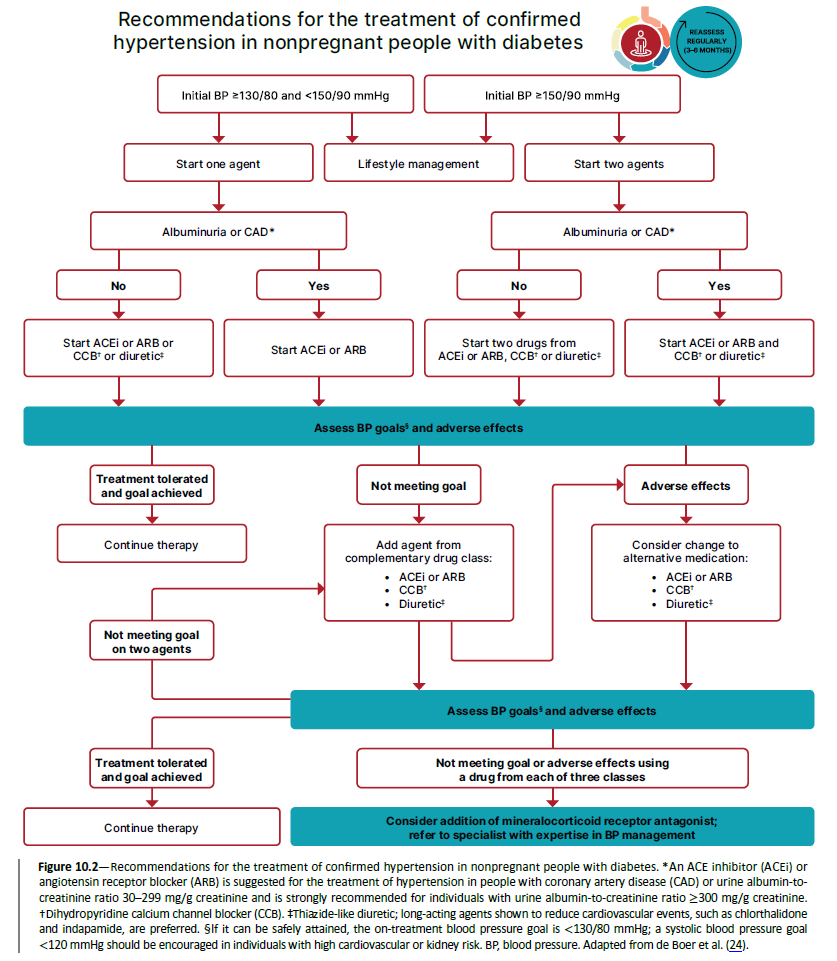
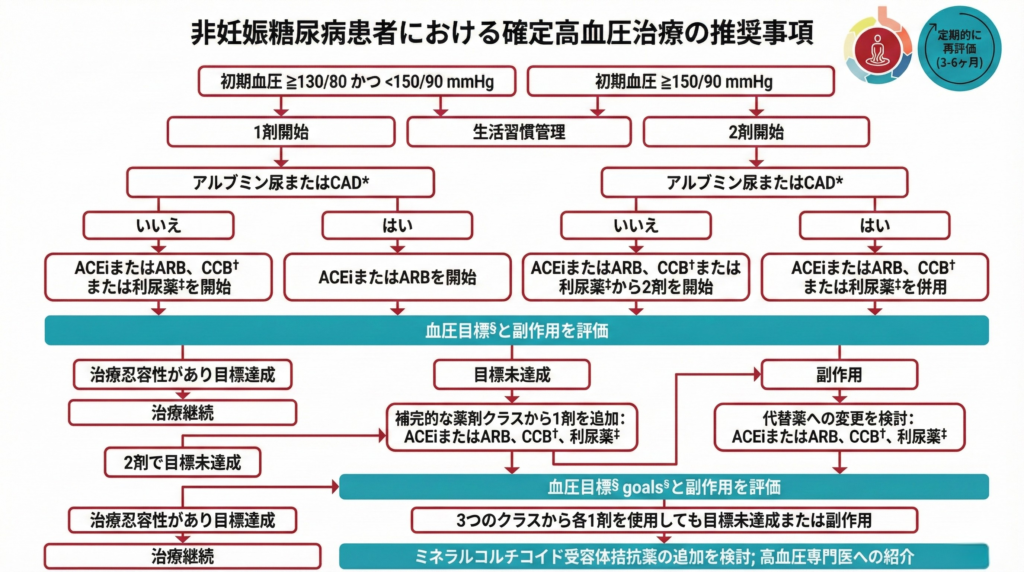
図10.2:非妊娠糖尿病患者における確定した高血圧治療の推奨フローチャート
|
【図10.2の構成と治療アルゴリズム】 ■ 初期血圧による分岐: ・初期血圧≧130/80かつ<150/90 mmHg → 1剤で開始 ・初期血圧≧150/90 mmHg → 2剤で開始 ■ アルブミン尿または冠動脈疾患(CAD)の有無による選択: ・あり → ACE阻害薬またはARBで開始 ・なし → ACE阻害薬またはARB、または CCB†、または利尿薬‡ ■ 評価と調整: ・治療耐容性良好かつ目標達成 → 治療継続 ・目標未達成 → 相補的クラスの薬剤を追加 ・有害事象 → 代替薬への変更を検討 ■ 3クラス(利尿薬を含む)使用後も目標未達成: → MRA追加を検討;血圧管理専門医への紹介を検討 【脚注】 *CADまたはUACR 30-299 mg/g ClにはACE阻害薬またはARBが推奨、UACR≧300 mg/g Clには強く推奨 †ジヒドロピリジン系カルシウム拮抗薬(CCB) ‡サイアザイド系類似利尿薬;心血管イベント減少が示された長時間作用型(クロルタリドン、インダパミドなど)が望ましい §安全に達成可能であれば血圧目標は<130/80 mmHg;心血管または腎リスク高い人では収縮期血圧<120 mmHg推奨 |
Diabetes Care. 2026 Jan 1;49(Supplement_1):S216-S245.
日本の医療への適用
日本のガイドラインとの整合性
ADA 2026の血圧目標<130/80 mmHg(心血管・腎リスク高い人では<120 mmHg)は、日本高血圧学会(JSH)2024ガイドラインと概ね整合している。JSH 2024では、糖尿病合併高血圧患者の降圧目標を130/80 mmHg未満としており、これは2019年版の130/80 mmHg未満を維持している。ただし、より厳格な目標(<120 mmHg)については、BPROAD、ESPRITの結果を踏まえた今後のガイドライン改訂で検討される可能性がある。
保険診療での実施可能性
推奨されている降圧薬クラス(ACE阻害薬、ARB、サイアザイド系類似利尿薬、Ca拮抗薬、MRA)はすべて日本で保険適用があり、汎用されている。家庭血圧測定も広く普及しており、実施に障壁はない。BPROAD、ESPRIT試験は中国で実施されており、東アジア人集団でのエビデンスとして日本人への外挿可能性が高い。
日本人でのエビデンスと注意点
日本人を含む東アジア人では、欧米人と比較して脳卒中の頻度が高く、厳格な血圧管理のベネフィットがより大きい可能性がある。一方、高齢糖尿病患者では、過度の降圧による起立性低血圧、転倒リスクに注意が必要であり、個別化した目標設定が重要である。また、食塩摂取量が多い日本人では、DASH型食事パターン指導において減塩指導を特に強調することが推奨される。
エビデンスレベルの説明
|
A |
十分に実施された無作為化比較試験または一般化可能な結果を持つ試験群を含むメタ解析からの明確なエビデンス |
|
B |
十分に実施されたコホート研究、または症例対照研究からの支持的エビデンス |
|
C |
十分にコントロールされた、または一般化可能な研究からの支持的エビデンスが不十分 |
|
E |
専門家のコンセンサス、または臨床経験 |
🎧 耳で聴きたい方はこちら
音声でもお楽しみいただけます(2倍速・約23分)
