PubMed URL:https://pubmed.ncbi.nlm.nih.gov/34593566/
タイトル:Kidney Outcomes Associated With SGLT2 Inhibitors Versus Other Glucose-Lowering Drugs in Real-world Clinical Practice: The Japan Chronic Kidney Disease Database
<概要(意訳)>
序論:
2型糖尿病(T2DM)は腎不全の主要な原因です。しかし、T2DM患者の腎症進行を遅らせる効果的な長期治療法は限られています。
ACE阻害薬とARBは、慢性腎臓病(CKD)を伴うT2DM患者の腎機能低下を遅らせることが示されています。
しかし、タンパク尿のないT2DMとCKD患者における、ACE阻害薬とARBの腎臓への効果については、これまで十分に特徴付けられていませんでした。
SGLT2阻害薬は、当初T2DMの治療のための血糖降下薬としてのみ承認されていましたが、複数の無作為化比較試験(RCT)において、腎臓および心血管保護作用を持つことが
次第に明らかになってきている。
しかし、これまでのRCTの結果が、臨床現場で遭遇する幅広いT2DMとCKD患者に適用できるかどうか、特に重度のアルブミン尿やタンパク尿のないT2DMとCKD患者におけるSGLT2阻害薬の腎臓への影響については、ほとんど分かっていません。
T2DM患者を対象とした国際的な実臨床研究(CVD-REAL 3)の結果では、SGLT2阻害薬の開始は、他の血糖降下薬と比較して推定糸球体濾過量(eGFR)の低下率が遅いことと関連していることが示されました。
スウェーデン、デンマーク、ノルウェーの日常臨床データを使用した別の大規模レジストリベースのコホート研究では、SGLT2阻害薬がDPP-4阻害薬治療と比較して腎イベントのリスクを低下させることが示されました。
しかし、両研究ともCKD患者は対象集団の10%未満であり、アルブミン尿やタンパク尿の評価は行われていませんでした。
さらに、SGLT2阻害薬開始前の腎機能低下率によって、SGLT2阻害薬の腎機能への効果が異なるかどうかを評価した研究はありません。これは臨床的に重要な問題です。
なぜなら、eGFRが急速に低下する患者は短期間で腎不全になるリスクが高いからです。
J-CKD-DB(CKD対策のためこれまで日本腎臓学会が構築してきた腎臓病総合レジストリ)は、全国規模の多施設CKDレジストリです。
J-CKD-DBのデータを使用して、SGLT2阻害薬を開始したT2DMを伴うCKD患者(DKD患者)と他の血糖降下薬を開始した患者の間でeGFR低下率と腎アウトカムを比較し、その関連がタンパク尿の有無とSGLT2阻害薬開始前のeGFRの急速な低下によって異なるかどうかを検討しました。
また、腎アウトカムとSGLT2阻害薬使用との関連が、eGFR(60 mL/min/1.73 m2未満vs.以上)、年齢(65歳未満vs.以上)、ACE阻害薬またはARBの使用の有無によって定義されたサブグループ間で異なるかどうかも評価しました。
方法:
<データソース、および調査対象者>
J-CKD-DBは、日本の大学病院21施設からCKD患者の実臨床の電子健康記録(EHR)に基づく多施設レジストリです。
2014年12月に開始され、このデータベースには、すべての入院・外来診療、処方、診断コード、臨床検査値に関する情報が含まれています。
J-CKD-DBに参加する施設は、SS-MIX2(厚生労働省電子的診療情報交換推進事業)ストレージを組み込み、SS-MIX2ストレージシステムにデータを転送できる構造化データ入力機能を持つ電子健康記録システムを備えていることが要件とされました。
SS-MIX2の仕様は、臨床検査項目や処方データに関するコード標準化を含む、日本の医療情報標準化における著しい進歩を採用しました。
多目的臨床データ登録システムというデータ抽出・登録システムが開発され、特にSS-MIX2形式を通じて臨床データを効率的に収集することができます。
データは2014年1月1日から12月31日の間に抽出・編集されました。
入力エラーと医師の負担を避けるため、すべてのデータ要素はSS-MIX2ストレージを使用して自動的に抽出され、J-CKD-DBデータセンターに送信されました。
SS-MIX2では、患者プロフィール(HL7 V2.5[ISO 27931]データ形式)、処方(日本の全国医薬品コード、HOTコード)、検査結果(JLAC10コード)、診断(ICD-10)、主要アウトカムの発生率など、基本的な標準規格が採用されました。
入力エラーや医師の負担を避けるため、すべてのデータ要素はSS-MIX2ストレージを使用して自動的に抽出され、J-CKD-DBデータセンターに送信された。
J-CKD-DBの包含基準は以下の通りです:
1)18歳以上、2)タンパク尿≥1(試験紙法)、またはeGFR <60 mL/min/1.73 m2。
したがって、このデータセットにはタンパク尿のない、eGFR <60 mL/min/1.73 m2の患者も含まれています。
本研究は川崎医科大学倫理委員会の監督下で、ヘルシンキ宣言の原則に従って実施されました。
患者記録は匿名化されているため、各参加大学病院のウェブサイト上でオプトアウト方式によるインフォームドコンセントを取得しました。
これは、日本の「人を対象とする医学系研究に関する倫理指針」に準拠したものです。
J-CKD-DBの大学病院21施設のうち5施設が、2014年1月1日から2018年12月31日の間の進行中の前向き縦断研究(J-CKD-DB-Ex)への参加に同意しました。
J-CKD-DB-Ex研究は、実臨床環境におけるCKD患者のeGFR低下の経時的なリスク因子を特定するために設計されました。
今回の分析では、SGLT2阻害薬または他の血糖降下薬を開始する前に1年以上の継続的な登録履歴を持つT2DM患者の記録を選択しました。
治療開始の基準日は、初期治療または追加療法として、SGLT2阻害薬(カナグリフロジン、ダパグリフロジン、エンパグリフロジン、イプラグリフロジン、ルセオグリフロジン、トホグリフロジン)または他の血糖降下薬(配合剤を含む)の処方が作成または調剤された日と定義し、前年にその薬剤クラスの処方がないことを条件としました。
さらに、CVD-REAL 3試験で使用された方法に準拠し、基準日以前に少なくとも2回以上のeGFR測定値があり、そのうち少なくとも1回は基準日から180日以内に行われたT2DM患者の記録を選択しました。
さらに、基準日以前のeGFRの変化を確実に推定するには、最初のeGFR測定と最後のeGFR測定の間に少なくとも180日間の期間が必要であることを指定した。
患者は、基準日から、基準治療の終了時(治療中の分析のみ)、診療所またはデータベースからの転居または離脱、死亡、または最後のデータ収集日まで追跡されました。
<腎機能およびその他の測定>
各参加者から血清クレアチニンとスポット尿の検体を採取しました。
血清クレアチニンは酵素法で測定されました。
eGFRは、日本人係数で修正されたCKD-EPI(慢性腎臓病疫学共同研究)の方程式を用いて算出されました。
腎機能の急速な低下は、年間3.0 mL/min/1.73 m2以上のeGFR低下と定義されました。
スポット尿検体に対して試験紙法による尿検査が実施されました。
尿試験紙の結果は各病院の医療スタッフにより判定され、(−)、(±)、(1+)、(2+)、(3+)として記録されました。
日本臨床検査標準協議会(JCCLS)の方針では、すべての尿試験紙検査は、1+の結果が尿蛋白レベル30 mg/dLに相当するように製造されることになっています。
本研究では、1+以上をタンパク尿と定義しました。
主要アウトカムは、SGLT2阻害薬または他の血糖降下薬治療開始からのeGFR変化率でした。
副次的なアウトカムは、eGFRの持続的な減少(50%以上、その後の測定で確認)または末期腎臓病(ESKD)の複合エンドポイントであった。
末期腎臓病は、eGFRが15mL/min/1.73m2未満(その後の測定で確認)と定義された。
複合エンドポイントの解析では、被験者に複数の事象が発生した場合、最初の事象が結果としてカウントされた。
エンドポイント特異的分析(感度分析)では、被験者に複数の異なるタイプの事象が発生した場合、すべての事象が結果としてカウントされた。
例えば、被験者がeGFRの低下が50%以上を経験し、その1ヵ月後にESKDと診断された場合、複合エンドポイント解析ではeGFRの低下が50%以上のみが転帰としてカウントされるが、エンドポイント特異的分析ではeGFRの低下が50%以上とESKDの両方が別々の転帰としてカウントされる。
結果:
マッチング前に、SGLT2阻害薬の新規導入者1,246例と、他の血糖降下薬の新規導入者2,492例が、本試験の適格基準を満たしました(補足図1)。
SGLT2阻害薬を開始した患者は、より若く、HbA1cとeGFRの値がより高い傾向にありました。
基準日前のeGFR変化の年間平均率、タンパク尿の有病率、降圧薬の使用は、両群で同様でした(補足表2)。
メトホルミン、利尿薬、ACE阻害薬、スタチンはSGLT2阻害薬群でより頻繁に処方される一方、DPP-4阻害薬、インスリン、スルホニル尿素薬の処方は少なかったです。
1対1の傾向スコアマッチング後、コホートはSGLT2阻害薬の新規開始者1,033例と他の血糖降下薬の新規開始者1,033例を含みました。
すべてのベースライン特性は良好にマッチングされ(表1)、すべての変数の標準化差は9.6%以下でした。
SGLT2阻害薬または他の血糖降下薬開始時の平均年齢は64.4歳で、2,066例の開始のうち777例(37.6%)が女性でした。平均HbA1cは61 mmol/mol(7.8%)、平均eGFRは68.1 mL/min/1.73m2で、2,066例の開始のうち549例(26.6%)がeGFR 60 mL/min/1.73m2以下であり、タンパク尿は578例(28.0%)に認められました。
2,066例の治療開始のうち、926例(44.8%)が基準日にACE阻害薬またはARBで治療を受けていました(表1)。
SGLT2阻害薬群における特定のSGLT2阻害薬の分布と、他の血糖降下薬群における基準薬剤クラスの分布は表1に示されています。
DPP-4阻害薬(69.7%)、メトホルミン(54.2%)、スルホニル尿素薬(24.8%)が最も頻繁に開始された他の血糖降下薬でした。
<主要評価項目>
一次解析における平均追跡期間(±標準偏差)は、SGLT2阻害薬群で21.0±9.8ヶ月、その他の血糖降下薬群で19.5±10.4ヶ月でした。
追跡期間中、eGFR測定の回数の中央値は、SGLT2阻害薬群で11回(四分位範囲7-16回)、その他の血糖降下薬群で10回(7-16回)でした。
治療中の解析では、治療開始前のeGFR年間変化率の平均は、SGLT2阻害薬群で-1.3±4.4 mL/min/1.73m²、その他の血糖降下薬群で-1.4±7.2 mL/min/1.73m²でした。
SGLT2阻害薬およびその他の血糖降下薬の投与開始後、eGFRの年間変化率の平均は、それぞれ-0.47 mL/min/1.73m²/年(95%CI:-0.63から-0.31)および-1.22(-1.41から-1.03)でした(図1および2)。
両群間のeGFR低下率の差は0.75 mL/min/1.73m²/年(0.51~1.00)で、SGLT2阻害薬群が優位でした(P<0.001)。
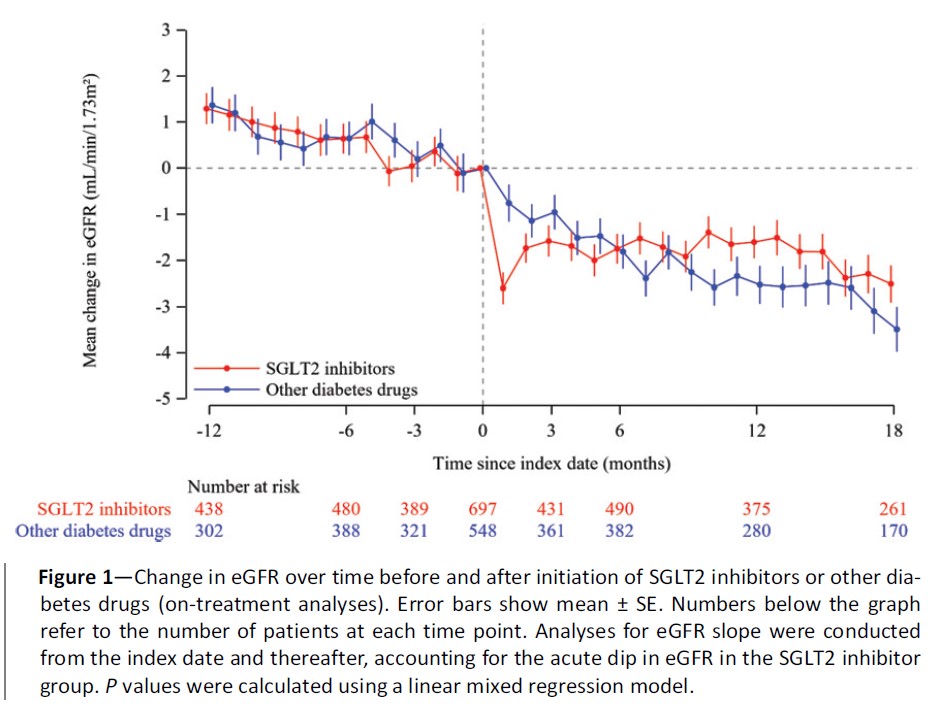
Diabetes Care. 2021 Nov;44(11):2542-2551.
SGLT2阻害薬または他の糖尿病治療薬の投与開始前後のeGFRの経時的変化は、蛋白尿の程度および投与開始前のeGFR低下速度別に、補足図2および3に示されている。
事前に規定されたサブグループごとのeGFRの年間変化率は図2に示されています。
SGLT2阻害薬の使用と、治療開始前の急速なeGFR低下、および開始時点でのACE阻害薬またはARBの使用との間に交互作用が認められました(いずれも交互作用のP値<0.05)。一方、SGLT2阻害薬の使用と、蛋白尿、eGFR(60 mL/min/1.73m²未満vs以上)、年齢(65歳未満vs以上)との間には交互作用は認められませんでした(すべての交互作用のP値>0.34)。
ITT集団でも同様の結果が観察されました(補足図4-7参照)。
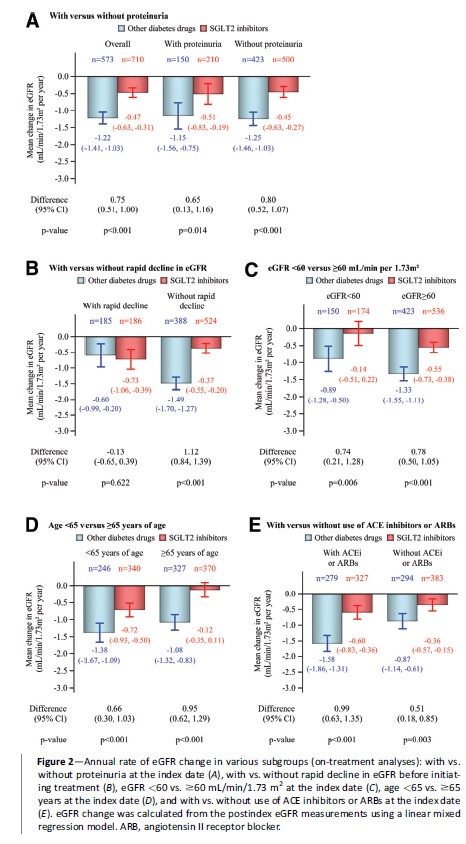
Diabetes Care. 2021 Nov;44(11):2542-2551.
<事後解析>
まず、治療中(on-treatment)解析では、追跡期間が1年未満の参加者を除外しました(補足図8)。
eGFR低下率の群間差は0.73 mL/min/1.73 m2/年(0.48~0.98)で、SGLT2阻害薬群が有利でした(P<0.001)。
次に、SGLT2阻害薬群(n=1,033)では903例でACRが測定され、そのうち15.5%のみがACR>300 mg/gでした。
他の血糖降下薬群(n=1,033)では811例でACRが測定され、16.2%がACR>300 mg/gでした。
そこで、この集団のACRの中央値(76.3 mg/g)を基準とした上下のサブグループ間で、SGLT2阻害薬と他の血糖降下薬の腎機能への効果の違いを評価しました。
結果はサブグループ間で一貫しており(補足図9、10)、SGLT2阻害薬使用とACRの間に交互作用は認められませんでした(ACR <76.3 vs. ≥76.3 mL/min/1.73 m2;交互作用のP = 0.14)。
経時的なACRで調整後のeGFR低下率の群間差は0.75 mL/min/1.73 m2/年(0.51~1.00)で、SGLT2阻害薬群が有利でした(P<0.001)。
第三に、逆確率重み付け解析(治療中解析)では、年間平均eGFR変化率はSGLT2阻害薬群(n=863)で−0.38 mL/min/1.73 m2/年(95% CI −0.51~−0.24)、他の血糖降下薬群(n=1,454)で−1.39(−1.50~−1.27)でした(補足図11)。
eGFR低下率の群間差は1.01 mL/min/1.73 m2/年(0.83~1.19)で、SGLT2阻害薬群が有利でした(P<0.001)。
<副次的アウトカム>
追跡期間中、eGFR50%以上の低下とESKDの複合イベントは、SGLT2阻害薬群で30件、他の血糖降下薬群で73件発生しました。
複合イベントの累積発生率は、他の血糖降下薬群の方がSGLT2阻害薬群より高かったです(図3A)。
イベント発生率は他の血糖降下薬群(36/1,000人年)の方がSGLT2阻害薬群(14/1,000人年)より高かったです。
タンパク尿の有無とeGFRの急速な低下の有無によるグループ間の複合イベントの累積発生率は補足図12と13に示されています。
SGLT2阻害薬の開始は、他の血糖降下薬と比較して複合イベントのリスクが低かったです(HR 0.40、95% CI 0.26-0.61;P<0.001)。
SGLT2阻害薬使用と、タンパク尿、eGFR(60 mL/min/1.73 m2未満vs.以上)、年齢(65歳未満vs.以上)、基準日でのACE阻害薬またはARBの使用、および治療開始前のeGFRの急速な低下との間に、複合イベントとの関連における交互作用は認められませんでした(すべての交互作用のP ≥ 0.35)(図4)。
追跡期間中、eGFR50%以上の低下は、SGLT2阻害薬群で25件、ESKDは7件発生し、一方、他の血糖降下薬群ではそれぞれ69件と26件発生しました。
eGFR50%以上の低下とESKDの累積発生率は、SGLT2阻害薬群と比較して他の血糖降下薬群の方が高かったです(図3BとC)。
SGLT2阻害薬の開始は、他の血糖降下薬と比較して:
– eGFR50%以上の低下のリスクが低く(HR 0.35、95% CI 0.22-0.56;P<0.001)
– ESKDのリスクも低かったです(HR 0.26、95% CI 0.11-0.61;P=0.002)(補足図14、15)
以下の項目間において、eGFR50%以上の低下またはESKDイベントとの関連における交互作用は認められませんでした(すべての交互作用のP ≥ 0.35):
– SGLT2阻害薬使用とタンパク尿
– eGFR(60 mL/min/1.73 m2未満vs.以上)
– 年齢(65歳未満vs.以上)
– 基準日でのACE阻害薬またはARBの使用
– 治療開始前のeGFRの急速な低下
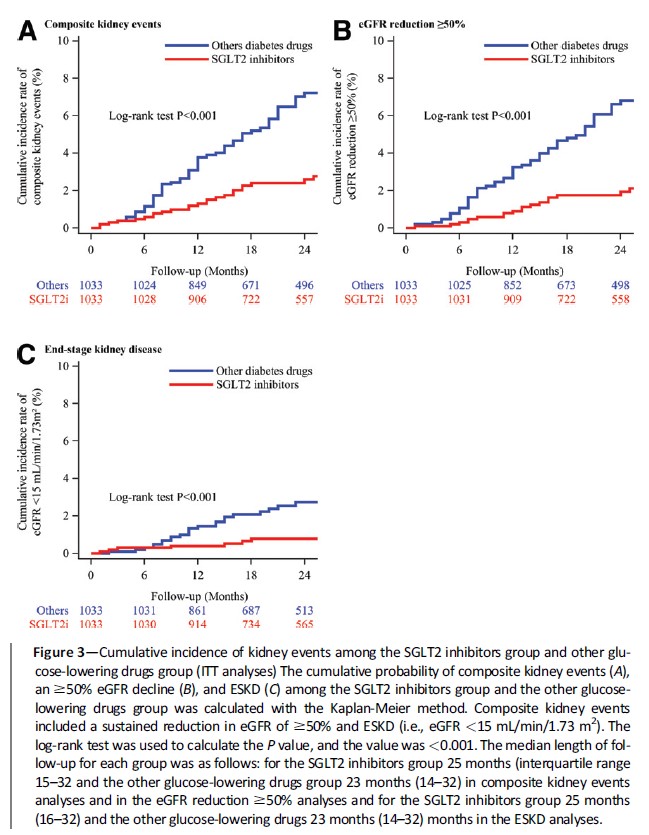
Diabetes Care. 2021 Nov;44(11):2542-2551.
考察:
現在の分析では、CKDを伴う2型糖尿病患者の多施設実臨床電子健康記録ベースのレジストリを用いて、SGLT2阻害薬の開始が他の血糖降下薬と比較してeGFR低下率が有意に低いことを見出しました。
SGLT2阻害薬の他の血糖降下薬に対するeGFR変化への有益な効果は、以下の患者で特に大きかったです:
– 治療開始前にeGFRの急速な低下がなかった患者
– 基準日にACE阻害薬またはARBを使用していた患者
SGLT2阻害薬の開始は、臨床的に重要な複合エンドポイント(eGFR50%低下またはESKD)のリスクも有意に低下させました。
SGLT2阻害薬の複合腎イベント減少における有益性は、以下のサブグループ間で一貫していました:
– タンパク尿(あり vs. なし)
– eGFR(60未満 vs. 60以上 mL/min/1.73 m2)
– 年齢(65歳未満 vs. 65歳以上)
– 基準日でのACE阻害薬またはARBの使用(あり vs. なし)
– 治療開始前の急速な低下(あり vs. なし)
CREDENCE試験では、eGFR 30-90 mL/min/1.73 m2(平均eGFR 56.2)と重度のアルブミン尿(中央値ACR 927)を持つ2型糖尿病患者において、カナグリフロジンの腎臓への効果を評価しました。
ESKD、クレアチニン値の倍化、または腎死を含む複合腎アウトカムは、プラセボと比較してカナグリフロジン群で有意に低かったです(HR 0.66、95% CI 0.53-0.81;P < 0.001)。
DAPA-CKD研究は、2型糖尿病の有無にかかわらず、重度のアルブミン尿(中央値ACR 949)とeGFR 25-75 mL/min/1.73 m2(平均eGFR43.1)の参加者を含みました。
eGFR50%以上の低下、ESKD、または腎死を含む複合腎アウトカムは、プラセボと比較してダパグリフロジン群で有意に低かったです(HR 0.56、95% CI 0.45-0.68)。
両試験は正常アルブミン尿の患者を除外しましたが、2型糖尿病とCKD患者の20-50%は正常アルブミン尿であり、その割合は過去10年間で増加しています。
タンパク尿のない2型糖尿病患者の有害な腎イベントリスクは、アルブミン尿のある患者とCKDのない患者(正常eGFRと正常アルブミン尿)の中間に位置します。
本研究では、ACE阻害薬またはARBを服用している患者の割合は、CREDENCE試験とDAPA-CKD試験で報告された割合の半分(約40% vs. 約99%)でした。
これは蛋白尿を呈する患者が30%のみであったことに起因する可能性があります。
タンパク尿を伴う2型糖尿病患者におけるeGFR低下率は、SGLT2阻害薬を服用していない場合でも、本研究の方がCREDENCE試験とDAPA-CKD研究より低かったようです。
これらの違いは、本研究の対象集団が低リスクであったことを示唆しています。
このような低リスク集団でのRCTの実施は実現可能ではない可能性があるため、本研究は、タンパク尿のない、またはACE阻害薬やARBを服用していない2型糖尿病とCKD患者における、SGLT2阻害薬の他の血糖降下薬に対する腎機能への有益な効果について、唯一利用可能なエビデンスを提供する可能性があります。
腎生検の研究では、2型糖尿病患者の一部のみが純粋な糖尿病性糸球体症(30-50%)を発症しており、その他の患者は糖尿病性糸球体症の有無にかかわらず、尿細管間質または血管疾患を有しています。
異なる構造病変を有する2型糖尿病患者がSGLT2阻害薬に対して異なる反応を示すかどうかは、まだ明らかになっていません。
タンパク尿を伴わない2型糖尿病とCKD患者は、典型的な糖尿病性糸球体症は少ないものの、不相応な間質および血管障害を有しています。
eGFRが急速に低下する2型糖尿病患者では、結節性病変とメサンギウム融解が報告されています。
今回の分析では、治療開始前のeGFR低下率にかかわらず、SGLT2阻害薬の開始は他の血糖降下薬と比較して、複合腎アウトカムのリスクが有意に低いことと関連していました。
逆に、eGFR低下を抑制するSGLT2阻害薬の他の血糖降下薬に対する有益性は、治療開始前にeGFRの急速な低下がなかった患者でより大きかったです。
この違いは平均への回帰効果に関連している可能性があります。
すなわち、治療開始前にeGFRの急速な低下があった患者は、治療群に関係なく、治療後の低下が緩やかになる傾向がありました。
複合腎イベントの累積発生率は、SGLT2阻害薬を服用しているタンパク尿を呈する2型糖尿病患者と、SGLT2阻害薬を服用していないタンパク尿を呈さない患者で同程度でした。
2型糖尿病とCKD患者におけるSGLT2阻害薬の潜在的な疾病修飾効果の背景にあるメカニズムはほとんど 不明であるが、2型糖尿病患者を対象としたEMPA-REG OUTCOME試験の最近の事後解析では、短期的なアルブミン尿の減少が長期的な腎機能低下リスクの減少と統計的に有意な関連があることが示唆されました。
したがって、糸球体過剰濾過の是正とそれに続くタンパク尿の減少によってeGFR低下が軽減される可能性があります。
本研究では、ACR測定値の入手可能性が限られていたため統計的検出力が影響を受け、追跡期間中のACR値による調整は行いませんでした。
そのため、SGLT2阻害薬の腎機能に対する有益性が、治療開始後のタンパク尿の変化の違いとは独立しているかどうかは不確かなままです。
本研究の強みには、複数のサブグループ解析の一貫性と、治療開始前後の複数のeGFR測定値の利用可能性が含まれ、これによりSGLT2阻害薬または他の血糖降下薬開始前の腎機能低下率に基づいて患者をマッチングすることが可能でした。
SGLT2阻害薬は幅広い低リスク集団で使用されており、これは臨床実践におけるSGLT2阻害薬の使用をより正確に反映しています。
日本では国民皆保険が実現しているため、経済的要因がSGLT2阻害薬と他の血糖降下薬の選択に大きな影響を与えた可能性は低いと考えられます。
本研究には以下のような限界があります:
- 観察研究としての性質上、統計的手法を用いても、未測定の交絡因子の可能性を完全には排除できません。
- 以下のような具体的な制限事項がありました:
– 一部患者がSGLT2阻害薬を治療初期に中止した可能性
– 血圧レベルや肥満度(BMIなど)の測定データが不足
– 血清クレアチニン測定法の精度に関する制限
– データの後ろ向き性質による偏り
– 線形モデルによるeGFR推移の評価の限界
– 欠損データの処理に関する課題(57%の患者でデータ欠損あり)
– 併存疾患情報の不足
– 糖尿病の他の細小血管合併症(網膜症、神経障害)に関する情報不足
– eGFR 45 mL/min/1.73 m2未満の患者が少数
- より長期的な観察研究データが必要とされます。
結論:
日常臨床において、SGLT2阻害薬を投与されたT2DMを伴うCKD患者は、他の血糖降下薬を投与された患者よりも、治療開始前のタンパク尿の有無やeGFRの低下速度に関わらず、腎臓の予後が有意に良好であった。
これらのデータは無作為化試験の結果を補完するものであり、臨床試験で観察されたSGLT2阻害薬の腎機能に対する有益性は、日常臨床においてより幅広い患者層に適用できる可能性があることを示唆している。
【参考情報】
我が国における慢性腎臓病患者に関する臨床効果情報の包括的データベースの構築に関する研究(J-CKD-Database)
SS-MIX 普及推進コンソーシアム
