PubMed URL:https://pubmed.ncbi.nlm.nih.gov/32399662/
タイトル:Empagliflozin attenuates neointimal hyperplasia after drug-eluting-stent implantation in patients with type 2 diabetes
<概要(意訳)>
背景:
SGLT2阻害薬がDES(薬剤溶出性ステント)留置後の虚血性心疾患患者の新生内膜性状にどのように影響するかについては、ほとんど知られていない。
本研究では、DES留置後にSGLT2阻害薬(エンパグリフロジン)で治療された2型糖尿病患者を対象にOCT(光干渉断層法)を使用して新生内膜性状に与える影響を調査した。
方法:
2016年3月~2018年1月の間に、DES(Ultimaster®; シロリムス溶出ステントまたはSynergy®; エベロリムス溶出ステント)留置術が予定されている血糖コントロール不十分(HbA1c>7.0%および空腹時血糖値>126mg/dl)な2型糖尿病患者を対象に、SGLT2阻害薬(エンパグリフロジン10㎎/日または25mg/日)群、または他の血糖降下薬(oGLD)群に割り付けた。
ベースラインで、「SGLT2阻害薬とインスリンの使用有、1型糖尿病、eGFR<45 mL/min/1.73m2、慢性完全閉塞病変、左主幹部病変、ステント内再狭窄病変」の患者は除外した。
対象患者は、DES留置術から少なくとも14日以内に、SGLT2阻害薬または他の血糖降下薬の追加治療が開始された。
両群ともに、HbA1cの目標値は7.0%未満とした。
主要評価項目は、「OCTで分析したDES留置12ヶ月後の平均新生内膜厚」とした。
結果:
ベースラインの患者特性は、2群間で有意な差はなかった。
平均HbA1cは、SGLT2阻害薬群で8.3%、oGLD群で8.1%であった。
定量的冠動脈造影法(QCA)によるベースラインの病変特性も、2群間で有意な差はなかった。
研究期間中は、全ての患者はスタチン療法を受けていた。
DES留置12ヶ月後のフォローアップ時に、合計28例が血管造影およびOCTの所見データが利用可能であった。
その内訳は、SGLT2阻害薬群15例(18病変)とoGLD群13例(15病変)であった。
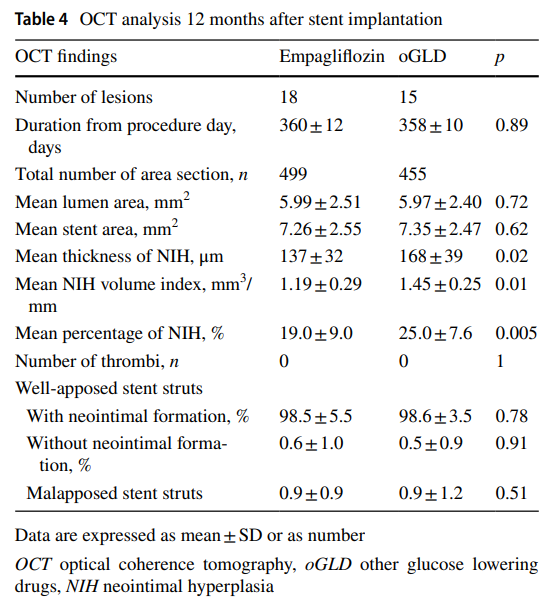
合計954枚のOCT断面画像(SGLT2阻害薬群:499枚、oGLD群:455枚)を分析した。
「OCTで分析したDES留置12ヶ月後の新生内膜性状」では、oGLD群よりもSGLT2阻害薬群の方が
平均の新生内膜厚(137±32 vs 168±39 µm、 p=0.02)は有意に薄く、体積(1.19±0.29 vs 1.45±0.25 mm3/mm、 p=0.01)は有意に小さかった。
全てのOCT断面画像において、血栓は観察されなかった。
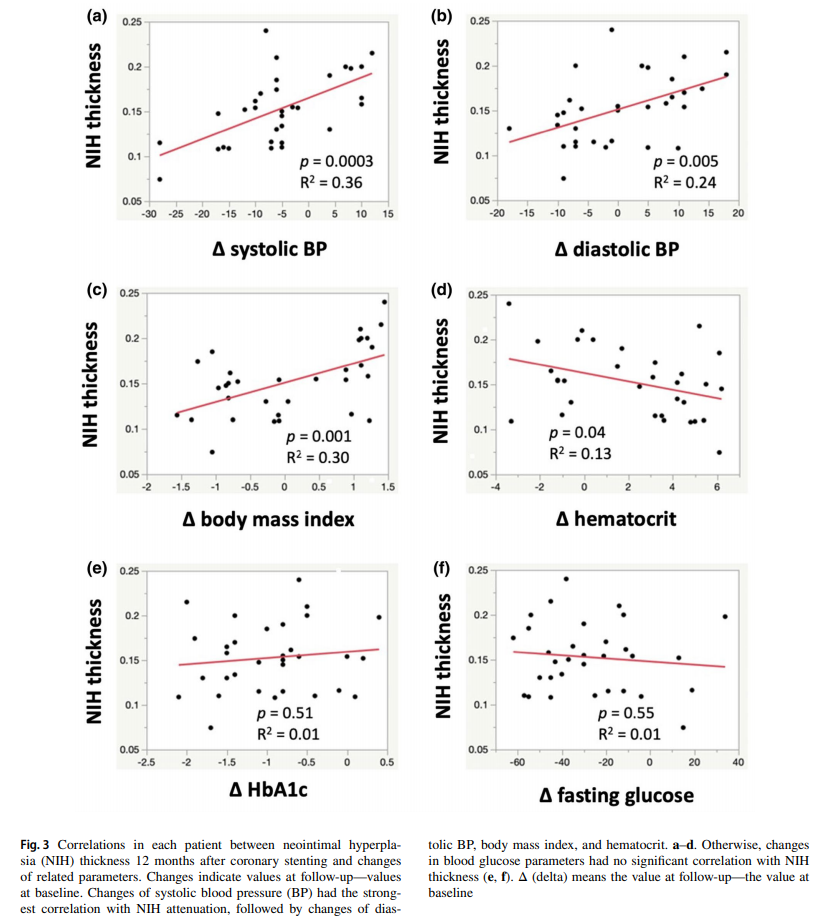
単変量ロジスティック回帰分析により、SGLT2阻害薬の投与による「収縮期および拡張期血圧の変化(低下)、BMIの変化(低下)、ヘマトクリット値の変化(増加)」は、DES留置12ヶ月後の新生内膜厚と有意な相関が示された。
一方で、血糖と脂質パラメータを含む他のパラメータ変化との有意な相関は示されなかった。
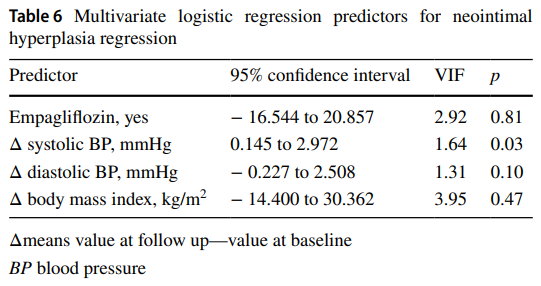
多変量ロジスティック回帰分析により、DES留置後の新生内膜厚の過形成を予防する為の最も強力な予測因子は収縮期血圧の変化(低下)であり、拡張期血圧の変化(低下)がそれに続くことが示された。
Heart Vessels. 2020 Oct; 35(10): 1378-1389.
結論:
生体吸収性ポリマーを使用したDES(薬剤溶出ステント)を留置した血糖コントロール不十分な2型糖尿病患者に対するSGLT2阻害薬(エンパグリフロジン)の追加治療は、他の血糖降下薬の追加治療と比較して、OCTで分析した12ヶ月後の新生内膜過形成を有意に抑制していた。 これは、SGLT2阻害薬の血糖低下効果ではなく、血圧低下効果が一番の要因であった。
