PubMed URL:https://pubmed.ncbi.nlm.nih.gov/32865377/
タイトル:Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure
<概要(意訳)>
背景:
SGLT2阻害薬は、糖尿病の有無に関わらず、心不全患者の入院リスクを軽減する。
左室駆出率が著しく低下したHFrEFを含む、広範囲の心不全患者に対する有用性を検討すする為に、より多くSGLT2阻害薬のエビデンスが必要である。
方法:
本試験(EMPEROR-Reduced試験)の参加施設は、20か国の520施設であった。
対象は、左室駆出率(LVEF)≦40%の慢性心不全[NYHA分類Ⅱ~Ⅳ度]の成人(18歳以上)とした。
全ての被験者は、必要に応じて、利尿薬、レニンアンジオテンシン系阻害薬、アンジオテンシン受容体ネプリライシン阻害薬、β遮断薬、ミネラルコルチコイド受容体拮抗薬、心臓デバイス等の適切な治療を受けていた。
我々は、過去12ヶ月以内に心不全の入院既往のあるLVEF≧30%、またはNT-proBNPがLVEF≦30%で少なくとも600pg/mLのNT-proBNP値を基準とした場合に、非常に高値(LVEF=31~35%で少なくとも1,000pg/mL、36~40%で少なくとも2,500pg/mL)を示す被験者は除外した。 これらのNT-proBNPの閾値は、心房細動を罹患した被験者では2倍であった。
4日~28日間のスクリーニング期間後、本試験の適格基準を満たした被験者を1:1の比率で無作為に、エンパグリフロジン(10 mg/日)、またはプラセボのいずれかを、通常の心不全治療を受けている被験者に追加投与した。
無作為化後の心不全、または他の疾患治療の開始や変更は医師の裁量で可能であった。
試験期間中のフォローアップは、2~3ヶ月毎に実施し、有効性、安全性の評価とバイタルサイン、体重、HbA1c、NT-proBNP、腎機能等を測定した。
さらに、カンザスシティ心筋症アンケート(KCCQ)を使用して患者の生活の質(QOL)を評価した。
SGLT2阻害薬の影響を除いたeGFRに対する効果を評価する為に、エンパグリフロジン、またはプラセボの投与中止から23~45日後にeGFRを再評価した。
全ての被験者は、本試験のレジメンを遵守していたかどうかに関係なく、事前設定した全てのイベントを追跡し分析(ITT解析)した。
統計分析では、階層的データ分析の手順として、主要評価項目と2つの副次評価項目を事前に設定した。
主要評価項目は、初発の「心血管死、または心不全による入院」の複合とした。
1つ目の副次評価項目は、「初発と再発の心不全による入院」とした。
2つ目の副次評価項目は、「二重盲検試験期間におけるeGFRの低下率」とした。
安全性分析には、エンパグリフロジン、またはプラセボを少なくとも1回投与した全ての被験者を含めた。
結果:
2017年4月~2019年11月迄に、合計7,220人の患者が適格性をスクリーニングされ、3,7無作為に3,730人をエンパグリフロジン群(1,863人)とプラセボ群(1,867人)に割り付けた。この2群間におけるベースラインの患者特性は、類似していた。
約50%は糖尿病の既往があり、73%はLVEF(左室駆出率)≦30%、79%はNT-proBNP≧1,000 pg/ml、48%はeGFR<60ml/min/1.73m2、約20%はアンジオテンシン受容体ネプリライシン阻害薬(ARNI)を投与されていた。
二重盲検試験期間の追跡データを収集する最終日は、2020年4月29日であった。
プラセボ群の4人の患者は、プラセボを投与されていなかった。
また、エンパグリフロジン群の303人(16.3%)とプラセボ群の335人(18.0%)は、死亡以外の理由で早期に本試験の参加を早期中止となった。
全体で21人(0.6%)の患者が試験終了時の生命状態が確認できなかったが、新型コロナウイルス感染症 (COVID-19)に関連した影響も少なからず受けていた。
生命状態が不明な患者を含む42人の患者(エンパグリフロジン群22人、プラセボ群20人)は、いくつかのフォローアップ時点でのデータ収集が出来なかった。
フォローアップ期間の中央値は16ヶ月であった。
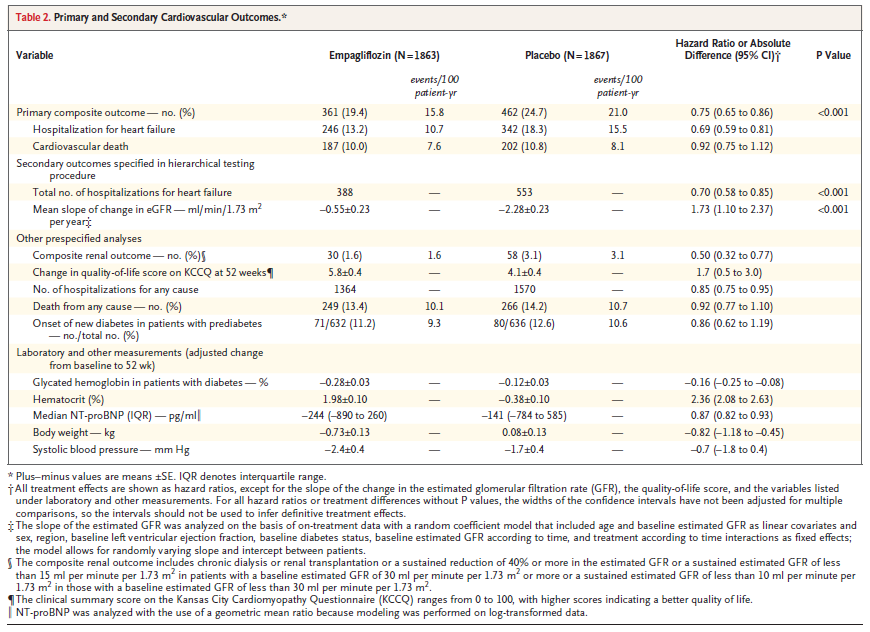
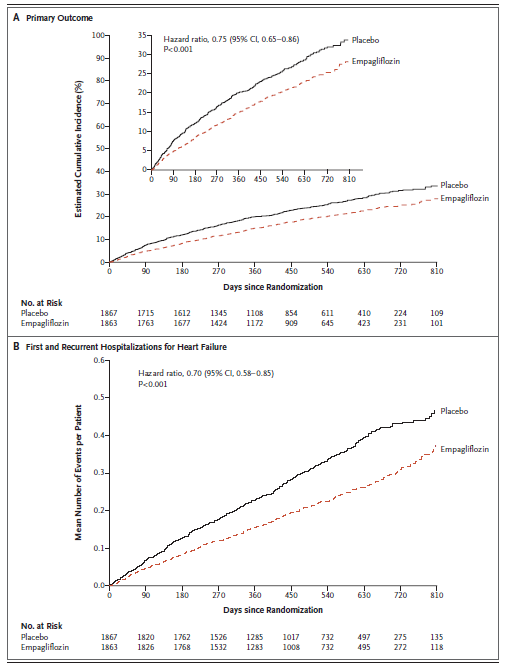
主要評価項目の「心血管死、または心不全による入院の複合」イベントは、エンパグリフロジン群で361人(19.4%)、プラセボ群で462人(24.7%)が発症した。
プラセボ群に対するエンパグリフロジン群のハザード比は、[HR 0.75(95%CI 0.65-0.86)]であり、2群間に有意な差が認められた(p<0.001)。
プラセボ群に対するエンパグリフロジン群の「心血管死」と「心不全による入院」のハザード比は、それぞれ、[HR 0.92(95%CI 0.75-1.12)]と[HR 0.69(95%CI 0.59-0.81)]であった。
エンパグリフロジン群の「心血管死、または心不全による入院の複合」イベントのNNT(治療必要数)は、19(95%CI 13-37)であった。
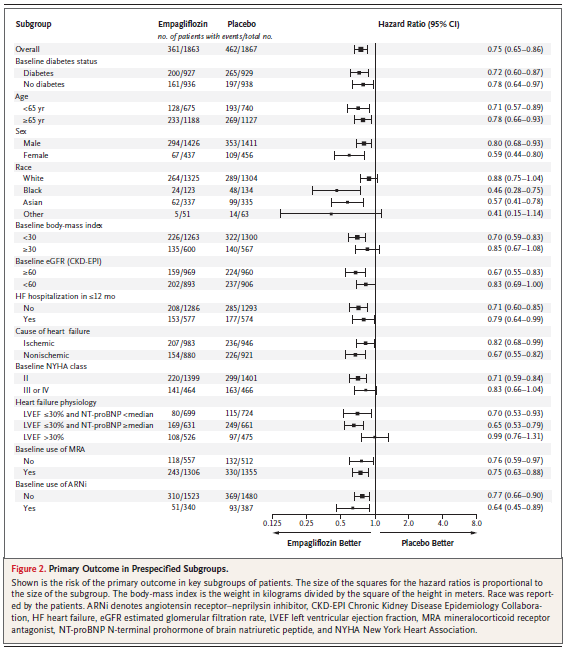
ベースラインでサクビトリルバルサルタンナトリウム水和物(ANRI)の投与と未投与のエンパグリフロジン群のプラセボ群に対する「心血管死、または心不全による入院の複合」のハザード比は、それぞれ、[HR 0.64(95%CI 0.45-0.89)]と[HR 0.77(95%CI 0.66-0.90)]であり、一貫した結果を示した。
また、エンパグリフロジン群は、階層的データ分析に事前設定した2つの副次評価項目(初発と再発の心不全による入院/eGFRの低下率)にも好影響を与えた。
副次評価項目の「初発と再発の心不全による入院」イベントは、エンパグリフロジン群で388件、プラセボ群で553件であった。
プラセボ群に対するエンパグリフロジン群のハザード比は、[HR 0.70(95%CI 0.58-0.85)]であり、2群間に有意な差が認められた(p<0.001)。
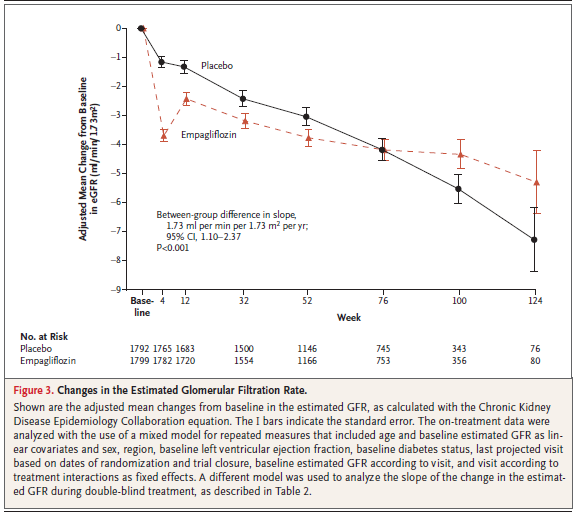
副次評価項目の「二重盲検試験期間におけるeGFRの低下率」は、エンパグリフロジン群で-0.55 ml/min/1.73m2、プラセボ群で-2.28 ml/min/1.73m2であった。
プラセボ群とエンパグリフロジン群の差異は、1.73 ml/min/1.73m2(95%CI 0.58-0.85)であり、2群間に有意な差が認められた(p<0.001)。
階層的データ分析に事前設定していない「複合腎イベント(慢性透析/腎移植/eGFRの大幅な持続的低下)」は、エンパグリフロジン群で30人(1.6%)、プラセボ群で58人(3.1%)が発症した。
プラセボ群に対するエンパグリフロジン群のハザード比は、[HR 0.50(95%CI 0.32-0.77)]であった。
SGLT2阻害薬の影響を除いたeGFRに対する効果を評価する為に、治療前と試験レジメンの中止後23〜45日の間で、966人の患者をペア測定した。
エンパグリフロジン群のeGFR低下は、–0.93(95%CI –1.97-0.11) ml/min/1.73m2 であった。
プラセボ群のeGFR低下は、–4.21(95%CI –5.26-3.17) ml/min/1.73m2 であった。
階層的データ分析に事前設定していない「全ての原因による死亡」は、エンパグリフロジン群で249人(13.4%)、プラセボ群で266人(14.2%)が発症した。
プラセボ群に対するエンパグリフロジン群のハザード比は、[HR 0.92(95%CI 0.77-1.10)]であった。
N Engl J Med. 2020 Oct 8;383(15):1413-1424.
プラセボを投与されなかったプラセボ群の4人の患者は、安全性分析から除外した。
全ての有害事象は、エンパグリフロジン群で1,420人(76.2%)、プラセボ群で1,463人(78.5%)が発症した。
性器感染症の発症は、プラセボ群[12人(0.6%)]よりもエンパグリフロジン群[31人(1.7%)]の方が多かったが、合併症のある性器感染症の発症はプラセボ群[6人(0.3%)]とエンパグリフロジン群[5人(0.3%)]で同等であった。
また、低血糖、下肢切断、骨折等の発症頻度も2群間で同等であった。
結論:
ガイドラインで推奨された治療を受けている心不全患者において、エンパグリフロジン群の「心血管死、または心不全による入院」のリスクは、糖尿病の有無に関わらず、プラセボ群よりも有意に低かった。
N Engl J Med. 2020 Oct 8;383(15):1413-1424.
