PubMed URL:https://pubmed.ncbi.nlm.nih.gov/36325584/
タイトル:Weight change and clinical outcomes in heart failure with reduced ejection fraction: insights from EMPEROR-Reduced
<概要(意訳)>
目的:
SGLT2阻害薬による治療で低下するベースラインからのBMIと体重減少は、駆出率が低下した心不全(HFrEF)患者の転帰に影響を及ぼす可能性がある。
本研究では、HFrEF患者を対象としたEMPEROR-Reduced試験において、ベースラインのBMI、体重減少が主要評価項目(心血管死または心不全による初回入院までの期間)および、副次評価項目に与えるエンパグリフロジンの影響をプラセボと比較した。
方法:
今回の解析では、ベースライン時のBMIによって患者を以下のカテゴリーに分類した。
世界保健機関(WHO)の肥満度分類により、<20、20〜<25、25〜<30、30〜<35、≥35 kg/m2とした。
BMI<20 kg/m2および35>kg/m2のサンプル数が少なかったため、BMI20 kg/m2をカットオフ低値とし、35 kg/m2をカットオフ高値とした。
さらに、体重の変化がうっ血の徴候によって影響を受けるかどうかを評価するために、ベースライン時に末梢浮腫がある患者とない患者の体重の変化を調査した。
結果:
<患者特性>
無作為化された3,730例の内、ベースラインのBMI<20 kg/m2は180例、BMI 20〜<25 kg/m2は1,038例、BMI 25~30 kg/m2は1,345例、BMI 30~<35 kg/m2は774例、BMI>35 kg/m2は393例であった。
BMIが低い患者と比較して、BMIが高い患者は、若く、白人が多く、糖尿病と心房細動を合併していることが多く、血圧とヘモグロビン値が高かった。
左室駆出率(LVEF)は異なるBMIカテゴリーで同程度であった。
BMIが高い患者ほど、心不全重症度が高く(NYHA分類 III〜IV度)、末梢の浮腫やうっ血を伴う容積負荷の徴候がみられた。
KCCQスコアは、BMIが高い患者ほど低かった。
低比重リポタンパク質(LDL)と総コレステロール値については、異なるBMIカテゴリー間に有意な差はなかった。
慢性閉塞性肺疾患(COPD)または悪性腫瘍の既往がある患者の割合は、異なるBMIカテゴリー間でほぼ同様であった。
<ベースラインのBMIカテゴリー別の臨床転帰リスク>
プラセボ群における主要評価項目(心血管死または心不全による初回入院までの期間)の発生率は、BMI< 20 kg/m2で最も高く(24.6件/患者100例/年)、BMI 25~30 kg/m2(19.3件/患者100例/年)で最も低かった。
BMIを連続変数として評価した場合、BMI < 20 kg/m2と「全死亡」との間に関連性が認められたが、潜在的交絡因子で調整した後は、その関連性は認められなかった。
プラセボ群では、各BMIカテゴリー(それぞれ-1.96、-2.31、-1.71、-3.66、-1.83)で、eGFR低下傾向は認められなかった。
<体重変化>
エンパグリフロジン投与群の内、313例(17.4%)が52週目に5%以上の体重減少を示し、79例(4.4%)が10%以上の体重減少を示した。
プラセボ群では、230例(12.8%)が52週目に5%以上の体重減少を示し、69例(3.8%)が10%以上の体重減少を示した。
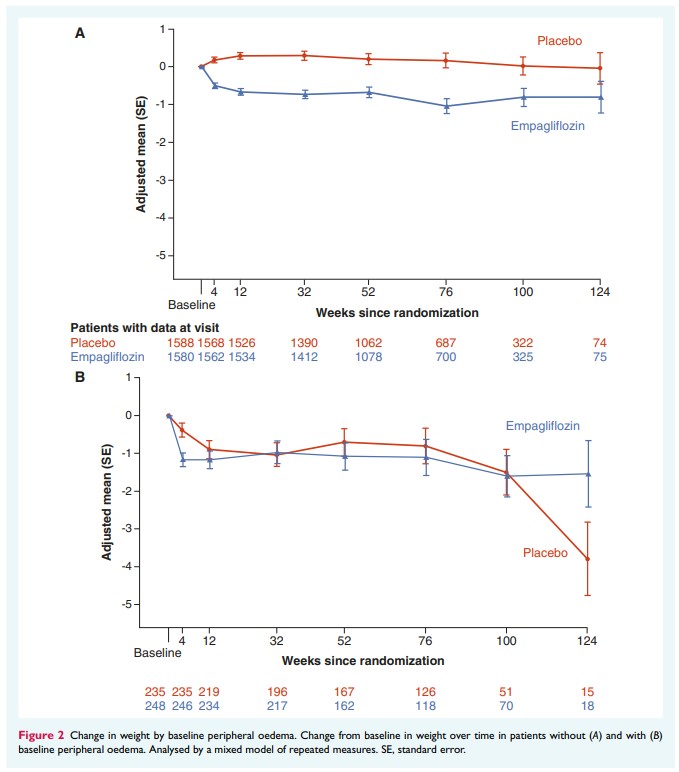
BMI < 20 kg/m2では、ベースラインからの体重増加が両群でわずかに認められたが、体重増加はエンパグリフロジンでわずかに少なかった。
BMI>35 kg/m2では、両群とも平均体重はベースラインから減少したが、初期の変化はエンパグリフロジン群でより顕著であった。
BMI中間の3つのカテゴリー(20〜<25 kg/m2、BMI 25~30 kg/m2、30~<35 kg/m2)では、体重はプラセボ群では比較的安定していたが、エンパグリフロジン群では緩やかな体重減少が認められた(52週目の平均変化量は0.6~1.4kg)。
ベースライン時に末梢性浮腫のある患者(n=504、13.5%)では、末梢性浮腫のない患者(n=3226、86.5%)よりも、体重は若干減少したが、治療群間に差はなかった
エンパグリフロジン投与群の末梢性浮腫を有する患者のベースラインから12週目までの平均体重変化は、-0.90kg(95%CI -1.37~-0.43)であったのに対し、プラセボ投与群では-1.17kg(95%CI-1.63~-0.72)であった。
また、ベースライン時に浮腫のなかった患者の体重変化は、エンパグリフロジン投与群で+0.29kg(95%CI 0.11~0.47)、プラセボ投与群で-0.68kg(95%CI -0.86~-0.50)であった。
Eur J Heart Fail. 2023 Jan;25(1):117-127.
<体重変化と臨床転帰>
体重変化を時間依存性共変量とした解析では、「体重減少」は、エンパグリフロジン群(体重減少1%あたりのハザード比[HR 1.0522(95%CI 1.0300-1.0749)、p<0.01])、およびプラセボ群(体重減少1%あたりのハザード比[HR 1.0599(95%CI 1.0288-1.0919)、p<0.01])で、「全死亡リスクの上昇」と関連していた。
一方で、「体重増加」は、エンパグリフロジン群(体重増加1%あたりのハザード比[HR 0.9871(95%CI 0.9437-1.0325)、p=0.57])、およびプラセボ群(体重増加1%あたりのハザード比[HR 0.9748(95%CI 0.9337-1.0178)、p=0.25])で、「全死亡リスクの上昇」と関連しなかった。
治療群間で、これらの関連に差があるかどうかを検定したところ、全死亡リスクに関する治療と体重変化との有意な交互作用は認められなかった(p=0.94)。
つまり、エンパグリフロジン群とプラセボ群の治療効果は、体重変化の影響を受けなかった。
「体重減少」は、エンパグリフロジン群(体重減少1%あたりのハザード比[HR 1.0115(95%CI 0.9822-1.0417)、p=0.4443])の主要評価項目(心血管死または心不全による初回入院までの期間)のリスク上昇と関連しなかったが、プラセボ群(体重減少1%あたりのハザード比[HR 1.0371(95%CI 1.0067-1.0684)、p=0.0165])では、わずかな主要評価項目のリスク上昇と関連していた。
逆に、「体重増加」は、プラセボ群(体重増加1%あたりのハザード比[HR 1.0160(95%CI 0.9865-1.0464)、p=0.2911])では主要評価項目のリスク上昇と関連しなかったが、エンパグリフロジン群(体重増加1%あたりのハザード比[HR 1.0345(95%CI 1.0051-1.0647)、p=0.0210])では、わずかな主要評価項目のリスク上昇と関連していた。
<ベースラインBMI別におけるエンパグリフロジンの臨床転帰に及ぼす影響>
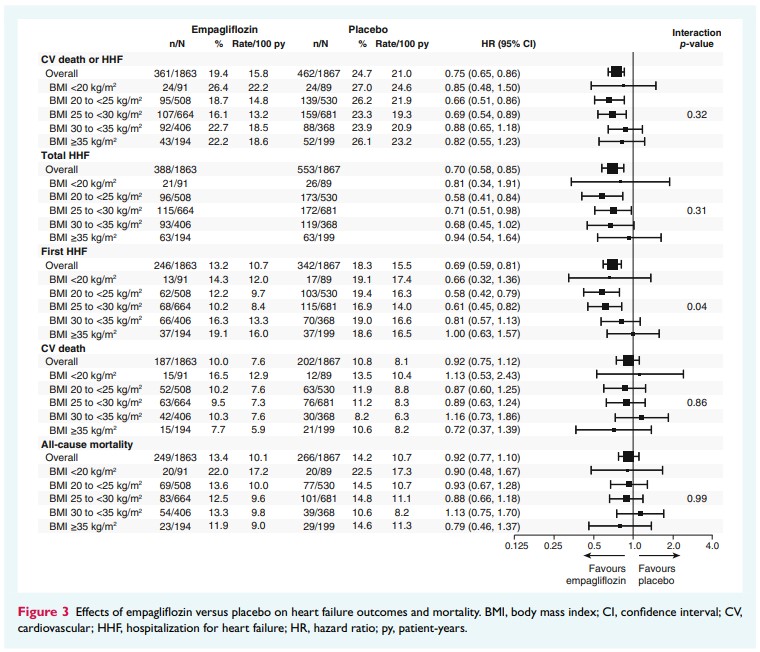
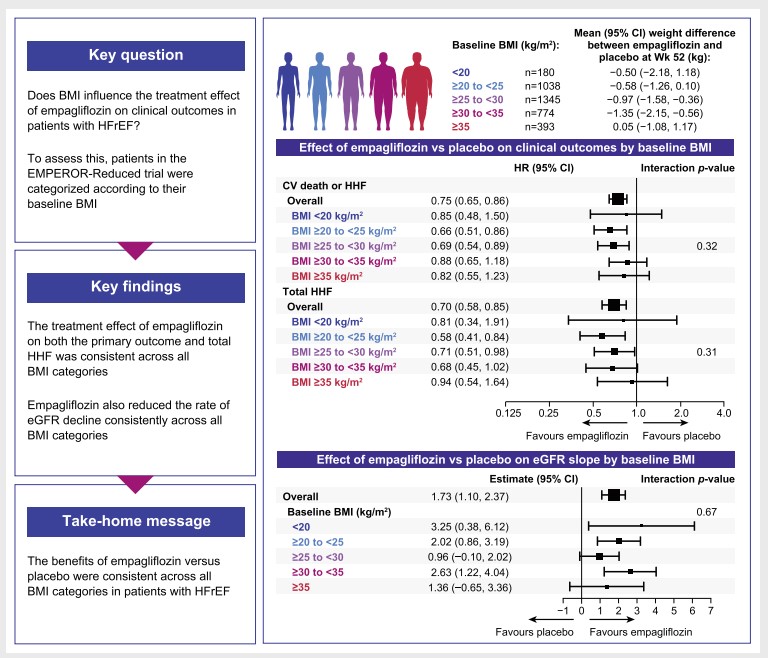
プラセボ群と比較したエンパグリフロジン群の「主要評価項目」に対する治療効果は、すべてのBMIカテゴリーで一貫していた(交互p=0.32)。
同様に、「心不全による入院の総数(交互p=0.31)」、「心血管死(交互p=0.86)」、「全死亡(交互p=0.99)」においても、一貫した治療効果があった。
一方で、「初発の心不全による入院」については、BMIカテゴリーで異なる治療効果があった(交互p=0.04)。
Eur J Heart Fail. 2023 Jan;25(1):117-127.
<ベースラインBMI別におけるエンパグリフロジンの腎機能低下とQOLに及ぼす影響>
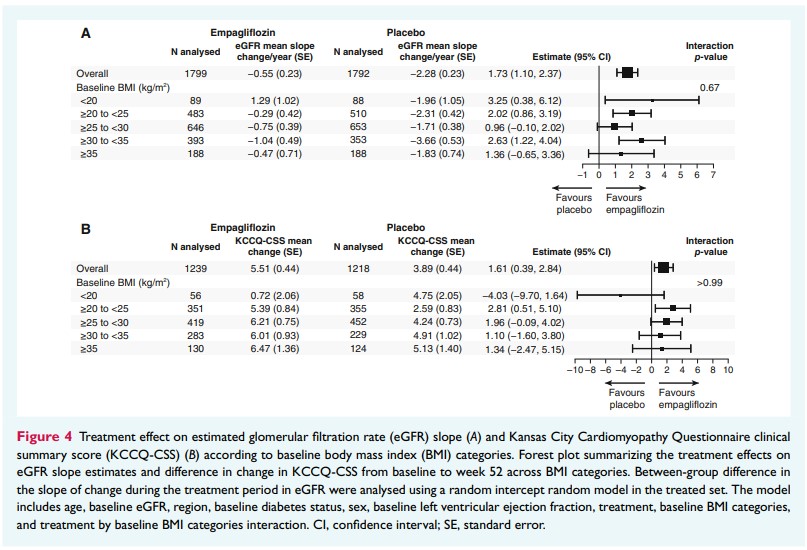
エンパグリフロジン群は、異なるBMIカテゴリーにおいてeGFR低下率に好ましい影響を与えた(交互p=0.67)。
全体として、腎複合アウトカムのリスクは、エンパグリフロジンによりプラセボに対してHR 0.50(95%CI 0.32-0.77)で減少し、異なるBMIカテゴリー間で治療異質性は認められなかった(交互p=0.76)。
ベースラインから52週目までのKCCQ-CSS変化の平均差は、BMIカテゴリー間で一貫していた(52週目の交互p>0.99)。
Eur J Heart Fail. 2023 Jan;25(1):117-127.
<安全性>
全体として、あらゆる有害事象または重篤な有害事象の発生率は、すべてのBMIカテゴリーにおいて治療群間で同程度であった。
症候性低血圧、急性腎不全、および確認された低血糖の発生率は、BMIカテゴリーを問わず両治療群で同程度であった。
治療中止に至った有害事象はBMI<20kg/m2で最も多かった。
性器感染症は少数例であったが、BMIカテゴリーに関わらず、エンパグリフロジンの方がプラセボより発生率が高かった。
考察:
このEMPEROR-Reduced試験の事後解析では、いくつかの重要な所見が報告された。
第1に、主要評価項目(心血管死または心不全による初回入院までの期間)の発生率は、低BMIおよび高BMIカテゴリーで最も高かった。
第2に、エンパグリフロジンの「体重減少」は、プラセボに対して「高BMI群」でわずかに大きい傾向が認められ、「低BMI群」では有意な体重減少は認められなかった。
第3に、「体重減少」はエンパグリフロジン群、プラセボ群ともに「全死亡リスクの上昇」と関連していたが、それにも関わらず、心不全および腎臓の転帰に対するエンパグリフロジンのプラセボに対する効果は、ベースラインのBMIカテゴリー間で一貫していた。
最後に、「QOL」に対するエンパグリフロジンの有益性は、BMIカテゴリー間で一貫していた。
全体として、これらの結果はHFrEF患者の臨床管理の指針として重要な臨床的意味を持つ。
エンパグリフロジンは、ベースラインのBMIや体重減少を理由にHFrEF患者の投与を差し控えるべきでないことが示唆された。
高BMIカテゴリー(BMI 30〜35 kg/m2未満)の「全死亡リスク」は、低BMIカテゴリー(BMI 20 kg/m2未満)の半分以下であった。
BMIを連続変数として評価した場合、「BMIと死亡率」の間には「U字型」の関連があり、NT-proBNPで調整するとBMI 25kg/m2付近で最もリスクが低くなることがわかった。
さらに、エンパグリフロジン群およびプラセボ群では、体重増加はみられなかったが「体重減少」は「全死亡リスクの上昇」と関連していた。
この知見は、心不全患者における体重および体重変化と死亡率との逆相関を示した先行研究と一致している。
このことは、末梢性浮腫のない患者がエンパグリフロジンで体重を減少させたが、プラセボでは体重を減少させなかったという考えからも支持される。
また、HFrEF患者における体重減少は、悪性腫瘍や炎症性疾患の発症など、全死亡リスクを増加させる可能性のある多数の疾患を併発していることが原因である可能性があることも非常に重要である。
今回の解析では、2つの治療群において、「体重減少または増加」と「主要評価項目」との間に一貫した関連は観察されなかった。
さらに、体重減少と死亡率の関連にもかかわらず、エンパグリフロジンの主要評価項目および副次評価項目に対する有益な効果は、BMIカテゴリー間で一貫していたことが示された。
痩せ型の心不全患者にSGLT2阻害薬を投与すべきかどうかを問う医師がいる中で、これらの点は重要である。今回の結果は、この点で安心感を与えるものである。
結論:
HFrEF患者におけるエンパグリフロジンのベネフィットは、プラセボと比較して、全てのBMIカテゴリーで一貫して認められた。
体重減少に関しては、治療群にかかわらず、全死亡リスクの上昇と関連していた。
安全性に関する新たなシグナルは認められなかった。
Eur J Heart Fail. 2023 Jan;25(1):117-127.
【参考情報】
WHO – 世界保健機関の基準によるBMI判定
【みんなの知識 ちょっと便利帳】BMI Calculator, WHOの判定基準によるBMI指数計算, ボディマス指数計算, ダイエット・減量の目安に (benricho.org)
むくみについて
ろうさいニュース -新潟労災病院- (johas.go.jp)
EMPEROR-Reduced試験
EMPEROR-Reduced試験:ジャディアンスの有効性と安全性-日本人集団の解析-|べーリンガープラス (boehringer-ingelheim.com)
