PubMed URL:https://pubmed.ncbi.nlm.nih.gov/38061371/
タイトル:Effects of empagliflozin on progression of chronic kidney disease: a prespecified secondary analysis from the empa-kidney trial
<概要(意訳)>
目的:
慢性腎臓病(CKD)は一般的な疾患であり、生活の質を低下させ、高価な腎代替療法を行わなければ致命的となる腎不全、心血管疾患、死亡のリスクを高める。
CKDを対象とした試験では、従来、腎不全(稀なアウトカム)と、ベースラインからのeGFR年間低下率(通常40~57%)を組み合わせた二項対立型の複合臨床転帰が用いられてきた。
後者は、現在、無作為化試験において、腎不全の有効な代替アウトカムとして規制当局に認められている。
また、このeGFR年間低下率(eGFR勾配)は、CKD進行の有効な代用指標と考えられ、臨床試験の主要評価項目として用いられるかもしれない。
RAS阻害薬、SGLT2阻害薬、ファインレノン(非ステロイド性選択的ミネラルコルチコイド受容体拮抗薬)など、多くの腎保護治療薬は、イニシャルディップ(初期のeGFR低下)を引き起こし、その後、長期的(または慢性的)にeGFR勾配を低下させる。
従って、新しい治療薬がeGFRの総勾配を構成するこれら2つの要素に及ぼす影響を理解することが重要である。
SGLT2阻害薬の無作為化試験では、糖尿病の有無にかかわらず慢性腎臓病患者において、腎臓病の進行リスクを減少させることが一貫して示されている。
CKD患者を対象としたSGLT2阻害薬に関する過去2つの試験の二次解析では、SGLT2阻害薬のeGFR勾配に対する影響は、患者のタイプによって異なることを示すいくつかのエビデンスが得られたが、これらの試験は有意なアルブミン尿を有する患者のみを対象としていた。
この為、この影響は、ベースラインのアルブミン尿やその他の臨床的特徴によって異なるかどうかを検討するには限界があった。
本研究では、進行リスクのあるCKD患者を幅広く対象(低アルブミン尿、低eGFR、糖尿病の有無等)としたEMPA-KIDNEY試験からeGFR勾配や腎アウトカムに対するエンパグリフロジンのプラセボに対する影響を異なるタイプの腎臓病患者において評価した。
方法:
EMPA-KIDNEY試験は、無作為化二重盲検プラセボ対照第3相試験で、8カ国(カナダ、中国、ドイツ、イタリア、日本、マレーシア、英国、米国)の241施設で実施された。
対象患者は、18歳以上で、人種調整後のeGFRが20~45 mL/分/1~73m2未満(アルブミン尿のレベルに関係なし)、またはeGFRが45~90 mL/分/1~73m2未満で、スクリーニング受診時の尿中アルブミン/クレアチニン比(uACR)が200mg/g以上の患者で、適応と忍容性があれば、臨床的に適切な用量のRAS阻害薬単剤を処方することとした。
糖尿病は有無に関わらず対象とし、多発性嚢胞腎は除外された唯一の原発性腎疾患とした。
1日45mg以上のプレドニゾロンまたはそれに相当するもの(副腎皮質ホルモン)を投与されている患者、または過去3ヵ月以内に免疫抑制薬の静脈内投与を受けていた患者は除外した。
適格で同意の得られた全ての患者は、無作為化前の導入(run-in)期間で1日1回投与のプラセボ錠を15週間投与された。
この間、現地の治験責任医師がスクリーニングデータを検討し、現在のRAS阻害薬の使用を評価し、後の無作為化に参加可能な患者を選定した。
対象となる患者が報告した原発性腎疾患は、現地の主任研究者によって確認された。
試験期間中における患者の臨床責任は、地元の医師にあった。
導入期間の終了後、適格患者は、中央分析と長期保存に必要な血液と尿のサンプルを採取され、エンパグリフロジン(10mg1日1回)、またはプラセボを経口投与する群に無作為に1:1に割り付けられた。
追跡調査の際、患者は腎臓の状態(透析治療または腎臓移植の有無)、試験薬のアドヒアランス(中止理由も含む)、併用薬の詳細に関する情報を提供した。
また、重篤な有害事象(およびプロトコールで指定された非重篤な有害事象)については、構造化面接を行い、血圧と体重の臨床測定を行い、クレアチニン、肝機能、カリウムの局所安全性評価のために採血を実施した。
血液検体および来院時の尿検体は、中央検査機関に送られ、有効性の解析および保存された。
英国で本研究に参加している患者は、エンパグリフロジンの中止によるeGFRの影響を評価する為、最終追跡調査の約4週間後におけるクレアチニンの分析用に血液サンプルの提供を求められた。
本研究のアウトカムは、「ベースラインから最終追跡調査までの期間(総勾配と定義)」と「2ヵ月後から最終追跡調査までの期間(慢性勾配と定義)」に分けて算出されたeGFRの年間変化率とした。
これは、当初のプロトコールにおける3次アウトカムに該当し、この探索的解析は事前に指定されていた。
イニシャルディップ(初期のeGFR低下)は、ベースライン時と2ヵ月後の追跡調査時のeGFRの差として算出された。
結果:
2019年5月15日~2021年4月16日の間に、6,609例の患者が無作為に割り付けられ、その後、中央値で2.0年(IQR 1.5~2.4)追跡された。
事前に規定された「eGFRのサブグループ」には、eGFR 30mL/分/1.73m2未満が2,282例(34.5%)、eGFR 30~45mL/分/1.73m2未満が2,928例(44.3%)、eGFR 45mL/分/1.73m2以上が1,399例(21.2%)含まれた。
事前に規定した「uACRのサブグループ」には、uACR 30mg/g未満が1,328例(20.1%)、uACR 30~300mg/gが1,864例(28.2%)、uACR 300mg/g以上が3,417例(51.7%)含まれた。
低eGFRの患者は、高齢で、糖尿病を罹患する割合が高かった。
eGFR 45mL/min/1.73m2以上の患者は、uACR値が最も高かったが、これはスクリーニング時にuACR 200mg/g以上でなければ適格とされなかった為である。
uACR値が高い患者は、若く、糖尿病を罹患する割合が低く、平均eGFRが高かった。
無作為化から2ヵ月後の追跡調査までの間、エンパグリフロジン治療の影響で低下した「eGFRの初期低下(イニシャルディップ)」は、プラセボと比較して、2.12mL/分/1.73m2(95%CI 1.83-2.41)、相対的低下は6%であった。
この相対的低下は、主要なサブグループ(糖尿病の有無、eGFR、uACR)間で有意に異なったが、年齢、BMI、HbA1c、および脂質低下薬の使用による影響を受けており、他の事前に規定されたサブグループでも概ね同様であった。
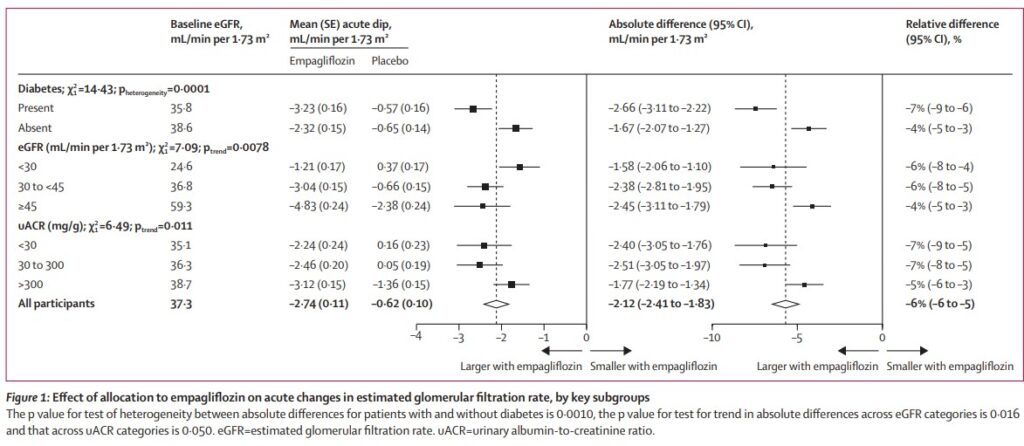
Lancet Diabetes Endocrinol. 2024 Jan;12(1):39-50.
全体として、「2ヵ月後から最終追跡調査までの期間(慢性勾配と定義)」で算出(イニシャルディップの影響を除外)したeGFRの年間低下率は、プラセボと比較して、エンパグリフロジンは1.37mL/min/1.73m2(95%CI 1.16-1.59)の遅延を示した。
これは、平均50%(95%CI 42-58)の相対的減少に相当する。
糖尿病の有無におけるeGFRの年間低下率では、糖尿病の無い患者と比較して、糖尿病の有る患者でより大きな遅延効果を示し、より大きな相対的減少効果が観察された(62%[50-73]対40%[29-51];異質性p=0.0074)
eGFRカテゴリー(<20、20 to <30、30 to <45、≥45)におけるeGFRの年間低下率では、
相対的減少効果が異なる(傾向p=0.012)が示され、eGFRカテゴリーが高くなるにつれて、その効果は大きくなることが示された。
uACRカテゴリー(<30、30 to 300、>300 to <1000、1000 to <2000、≥2000)におけるeGFRの年間低下率では、
相対的減少効果が異なる(傾向p<0.0001)が示され、uACRカテゴリーが高くなるにつれて、その効果は小さくなることが示された。
「ベースラインから最終追跡調査までの期間(総勾配と定義)」で算出されたeGFRの年間変化率は、
プラセボと比較して、エンパグリフロジンは0.75mL/min/1.73m2(95%CI 0.54-0.96)遅らせた。
これは、平均26%(95%CI 19-33)の相対的減少に相当する。
これらの差は、eGFRの初期低下(2か月間のイニシャルディップの影響)と慢性勾配と定義したeGFRの年間変化率に対する影響を組み合わせた結果を反映している。
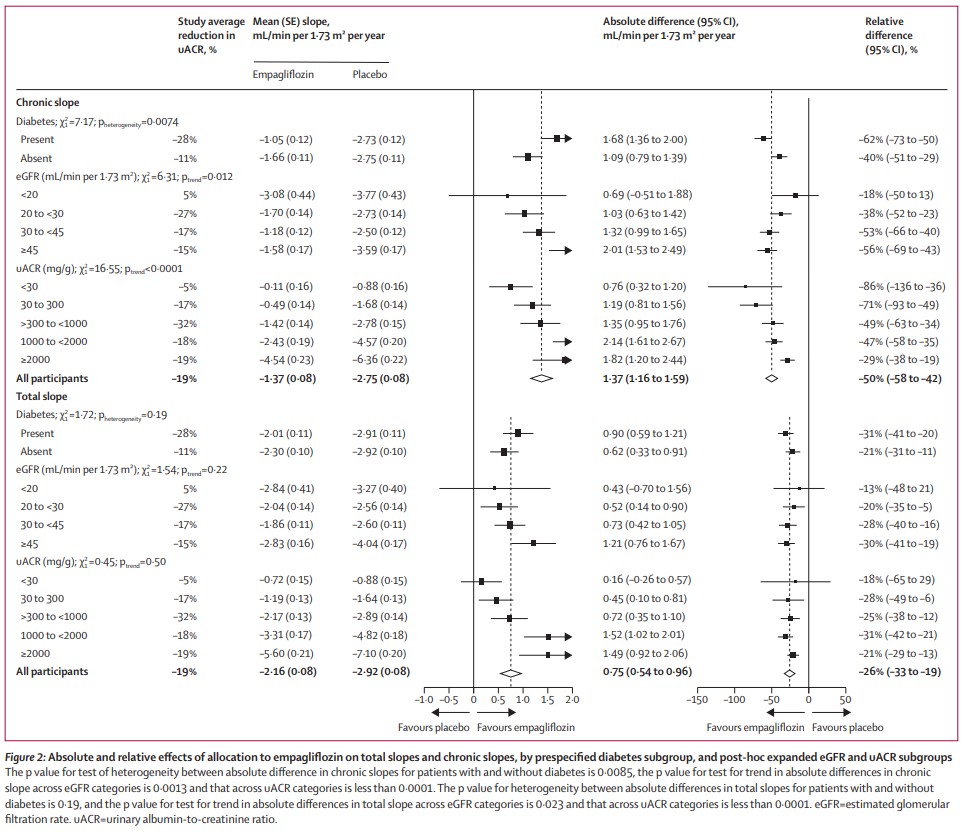
Lancet Diabetes Endocrinol. 2024 Jan;12(1):39-50.
考察:
我々の解析では、進行リスクのあるCKD患者コホートにおいて、エンパグリフロジンは、イニシャルディップ(投与2ヶ月におけるeGFRの初期低下)により、約2mL/分/1.73m2(6%の相対的低下)の僅かな腎機能低下を引き起こし、その後、長期的な腎機能低下を半減させた。
この全体的な結果は、末期腎不全、ベースラインから40%以上の持続的なeGFR低下、eGFR 10mL/min/1.73m2未満の低下、または腎不全による死亡というカテゴリー別複合アウトカムで評価した場合の腎臓病進行リスクの29%(95%CI 19-38)の減少を補足するものである。
CKDの進行に対するエンパグリフロジンの有益な効果は、糖尿病の状態やeGFRによって異なるが、アルブミン尿によって最も顕著であり、アルブミン尿の低い患者では、相対的な有益性が実際に大きくなる可能性がある。
これらの所見は、CKD患者を対象とした他のSGLT2阻害薬の臨床試験における結果と一致しているが、これらの臨床試験は糖尿病、有意なアルブミン尿、またはその両方を有する患者に焦点を当てたものである。
EMPA-KIDNEYの大規模試験に組み入れられた患者の範囲は広いため、CKD患者を対象とした他のSGLT2阻害薬の大規模試験に組み入れられた患者よりも、より多様な集団を対象とした検討が可能となった・
特に、EMPA-KIDNEY試験には、他の試験では除外されていた、eGFR 25mL/min/1.73m2未満で、uACR 200mg/g未満の患者が含まれている。
糖尿病がなく、有意なアルブミン尿(uACR<200mg/g)がない患者にSGLT2阻害薬を使用することを(推奨するのではなく)提案しているいくつかの国際的なガイドラインに反して、これらの解析では、アルブミン尿が少ない患者(糖尿病の有無にかかわらず)は、急性腎障害や心血管疾患のリスク低下という他の利点に加えて、SGLT2阻害による腎機能の維持という点でかなりのベネフィットを享受できる可能性が高いことが示唆された。
EMPA-KIDNEY試験には、1型糖尿病の患者は殆ど含まれておらず、常染色体優性多発性嚢胞腎患者や腎移植を受けた患者は試験の対象ではなかった。
また、CKDの進行リスクが低い患者(eGFR 45mL/min/1.73m2以上でuACR 200mg/g未満の患者)は意図的に除外された。
本試験は、明確な有益性のエビデンスが得られたため、予定よりも早く試験が中止となり、患者は平均2年間しか治療を受けなかったが、この治療による長期的な影響を評価するため、治療終了後にさらに2年間の追跡調査が行われている。
結論:
EMPA-KIDNEY試験において、エンパグリフロジンは、プラセボと比較して、イニシャルディップ(eGFRの初期低下)を引き起こし、その後、CKDの長期的な進行を実質的に遅延させた。
この長期的なベネフィットは、ベースラインにおける糖尿病の有無、eGFR値、uACR値によって異なった。
この試験は、最もリスクの高い患者のアウトカムに明らかなベネフィットが得られた為、早期に中止されたが、これらの解析は、アルブミン尿のレベルが低い患者など、よりリスクの低い患者には、他の証明された心血管系および死亡率のベネフィットに加えて、腎機能の維持という点でもベネフィットが享受されることを示唆している。
これらの結果は、エンパグリフロジンが広範囲の患者において慢性腎臓病の進行速度を遅らせることを示唆している。
この知見は、アルブミン尿を用いてSGLT2阻害薬による治療を推奨する患者を層別化してきたガイドラインを覆すものである。
アルブミン尿が低い患者(その結果、慢性腎臓病の進行リスクが低い患者)は、急性腎障害や心血管疾患のリスクの減少に加えて、腎機能の維持という点でもSGLT2阻害薬による治療が有益である。
SGLT2阻害薬が広く使用されるようになれば、CKDが公衆衛生に及ぼす影響に大きなインパクトを与えることが示唆される。