PubMed URL:https://pubmed.ncbi.nlm.nih.gov/36331190/
タイトル:Empagliflozin in Patients with Chronic Kidney Disease
<概要(意訳)>
背景:
慢性腎臓病(CKD)は、しばしば進行性で、糸球体濾過量(GFR)の低下とアルブミン尿の存在が、その後の腎不全発症の重要な危険因子となる。
CKDの進行を遅らせ、透析や腎移植を回避することは、透析や腎移植がQOLや心血管系の罹患率や死亡率に及ぼす影響や、腎代替療法に伴う多額の費用を考えると、非常に望ましいことである。
アルブミン尿が増加している糖尿病性腎臓病(DKD)患者を対象とした大規模なプラセボ対照試験では、RAS阻害薬、SGLT2阻害薬、非ステロイド型選択的ミネラルコルチコイド受容体拮抗薬(MRA)のフィネレノンは、いずれも腎不全への進行リスクを低下させることを示した。
地域差はあるが、世界的には、CKD患者の大半はuACR(尿中アルブミン/クレアチニン比)のレベルが低く(300 mg/gCr未満)、糖尿病を罹患していない。
したがって、幅広い層のCKD患者を研究することは、公衆衛生的に非常に重要である。
uACR 200mg/gCr以上のCKD患者を対象としたSGLT2阻害薬(ダパグリフロジン10mg/日)のDAPA-CKD試験で事前に指定したサブ解析では、糖尿病の有無に関わらず、腎不全に対するベネフィットがあることが示された。
しかしながら、eGFR 30 mL/min/1.73m2未満の患者に対するデータは限られており、これらのベネフィットはCKD患者のより幅広い層では異なる可能性がある。
EMPA-KIDNEY試験は、腎疾患および心血管疾患の進行に対するエンパグリフロジン10mg/日(SGLT2阻害薬)の効果と安全性を評価するために実施された国際共同無作為化並行群間二重盲検プラセボ対照臨床試験である。
本試験は、糖尿病の罹患がない患者、eGFR 30 mL/min/1.73m2未満の患者、uACRレベルの低い患者を含め、より幅広いCKD患者層を対象とすることを目的とした。
方法:
EMPA-KIDNEY試験は、8ヶ国の241施設で実施された。
スクリーニング受診時におけるアルブミン尿のレベルに関係なく、人種調整した20≦eGFR<45 mL/min/1.73m2、またはuACR(尿中アルブミン/クレアチニン比)≧200 mg/gCrかつ45≦eGFR<90 mL/min/1.73m2の成人(18歳以上)を適格患者とした。
患者は臨床的に適切な用量の単剤RAS阻害薬を服用していることが必要であったが、治験責任医師がRAS阻害薬の適応がない、あるいは忍容性がないと判断した場合には、プロトコールに明記されているように、患者を組み入れることが可能であった。
一方で、多発性嚢胞腎患者および腎移植を受けた患者は除外された。
すべての適格患者は無作為化前のRun-in(導入)期間に入り、1日1回投与のプラセボ錠が15週間投与された。
この間、現地の治験責任医師はスクリーニングデータを検討し、現在のRAS阻害薬の使用状況を評価し、後の無作為化の対象となる可能性のある患者を承認した。
試験期間中、患者の臨床的責任は地元の医師にあった。
少なくとも6週間のRun-in期間を完了した後、参加に同意した患者から中央分析および保存のための血液および尿検体を採取した。
患者はエンパグリフロジン(10mg、1日1回)またはプラセボ群に無作為に割り付けられた。
各経過観察時に、患者は腎臓の状態(透析治療または腎移植の有無)、指定された試験レジメンの遵守状況(中止の理由を含む)、併用薬の詳細に関する情報を提供した。
また、重篤な有害事象(およびプロトコールで規定された非重篤な有害事象)について構造化面接で質問され、血圧と体重の臨床評価を受け、クレアチニン、肝機能、カリウムの局所安全性評価のために血液検体を採取された。
尿検体(選択された来院時に入手)および血液検体は、有効性解析および保存のために中央検査室に送られた。
事前に規定された主要アウトカムは、「腎臓病の進行または心血管死の複合アウトカムにおける初発までの期間」であった。
腎臓病の進行には、「末期腎不全(維持透析の開始または腎移植)、eGFR 10mL/分/1.73m2未満の低下、ベースラインから40%以上のeGFR持続的低下、または腎死(腎臓が原因による死亡)」が含まれた。
持続的eGFRの低下の評価には、少なくとも30日間隔で2回連続して予定されたフォローアップ(追跡調査)受診時に測定された値のいずれか、または、最終フォローアップ受診時または死亡(または同意の撤回、追跡調査不能)前の最後の予定された受診時に測定された値のいずれかが用いられた。
血清クレアチニンの中央検査室での測定値がGFRの推定に使用され、中央での測定結果が欠落している場合は、地域の検査室での測定値が使用された。
事前に指定された主要な副次的アウトカムは、「心不全による入院または心血管死、全ての原因による入院(初発と再発を含む)、全死亡」であった。
その他の副次的アウトカムは、「腎疾患の進行、心血管死、ESKDまたは心血管死の複合」であった。
三次評価、安全性評価、検査評価および計画された探索的評価に関する詳細は統計解析計画に記載されている。
主要アウトカムの事前に規定した主要サブグループ解析は、「ベースライン時における糖尿病の状態、eGFR、uACR(尿中アルブミン/クレアチニン比)」によって層別化した。
死亡、心不全、心筋梗塞、脳卒中、肝障害、ケトアシドーシス、下肢切断、急性腎障害、重篤な生殖器感染症による入院の可能性のあるすべてのイベントは,事前に規定された定義と試験施設から収集された情報源を用いて,試験群の割り付けを知らない臨床医により判定された。
結果:
2019年2月から2021年4月までに、合計8,544例の患者がスクリーニング訪問に参加した。
8,184例(95.8%)が無作為化前のランイン(導入)期間に入り、6,609例が無作為化された。
無作為化時における患者の平均年齢は63.8歳、女性は33.2%、非糖尿病は54.0%であった。
平均(±SD)eGFRは37.3±14.5 mL/min/1.73m2であり、患者の34.5%はeGFR 30 mL/min/1.73m2未満であった。
uACR(尿中アルブミン/クレアチニン比)の中央値は329 mg/gCrであり、患者の48.3%はuACR 300 mg/gCr以下であった。
このようにCKD進行リスクのある幅広い患者が本試験の対象となった。
2022年3月7日、独立データ・安全性モニタリング委員会は、624件の初回一次アウトカムイベントに基づき、正式な中間解析の時点で、有効性を理由に試験を早期に中止する条件はいずれも満たされていると報告した。
追跡調査(フォローアップ)は2022年7月5日に終了し、その時点での追跡調査期間の中央値は2.0年(IQR 1.5~2.4)であった。
合計6,552例(99.1%)が生存しており、最終追跡を完了したか、追跡中に死亡した。
18例(0.3%)で生存状態が不明であり、39例(0.6%)で同意が撤回された。
すべての適格イベントは判定された。
12ヶ月の追跡調査(試験のおおよそ中間点)で、エンパグリフロジン群の3,245例の内、2,909例(89.6%)、プラセボ群の3,239例の内、2,924例(90.3%)は、服薬コンプライアンスが良好(>80%)であったと報告された。
エンパグリフロジン群18例(0.5%)、プラセボ群31例(0.9%)が試験中にSGLT2阻害薬による治療を非盲検で開始したものを含み、最終追跡調査の時点で、エンパグリフロジン群557例(16.9%)、プラセボ群640例(19.4%)が割り付けられた試験レジメンを中止した 。
<一次および二次アウトカム>
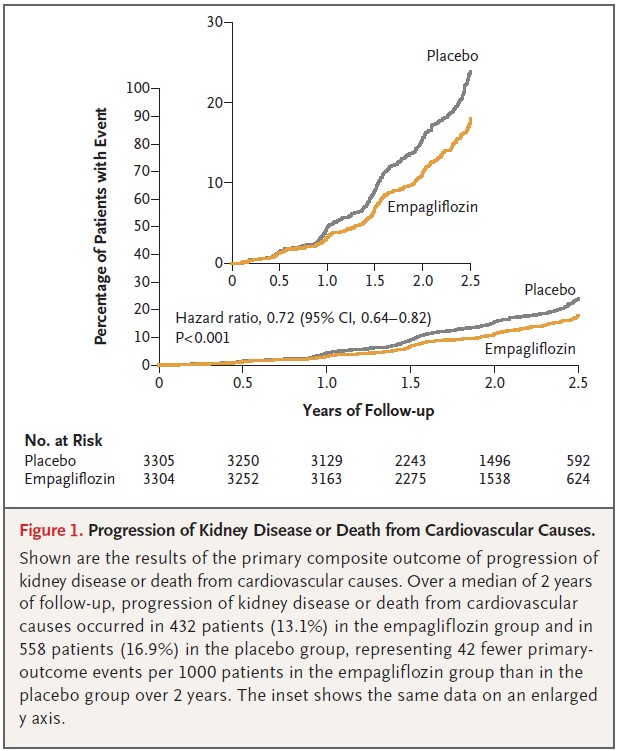
主要アウトカムの「腎疾患の進行または心血管死」は、エンパグリフロジン群で3,304例の内432例(13.1%)、プラセボ群で3,305例の内558例(16.9%)で発生し、プラセボ群に対するエンパグリフロジン群のハザード比は、[HR 0.72(0.64-0.82); p<0.001]となった。
ゆえに、エンパグリフロジン群の「心血管死または腎疾患の進行」に対する有意な効果が示された。
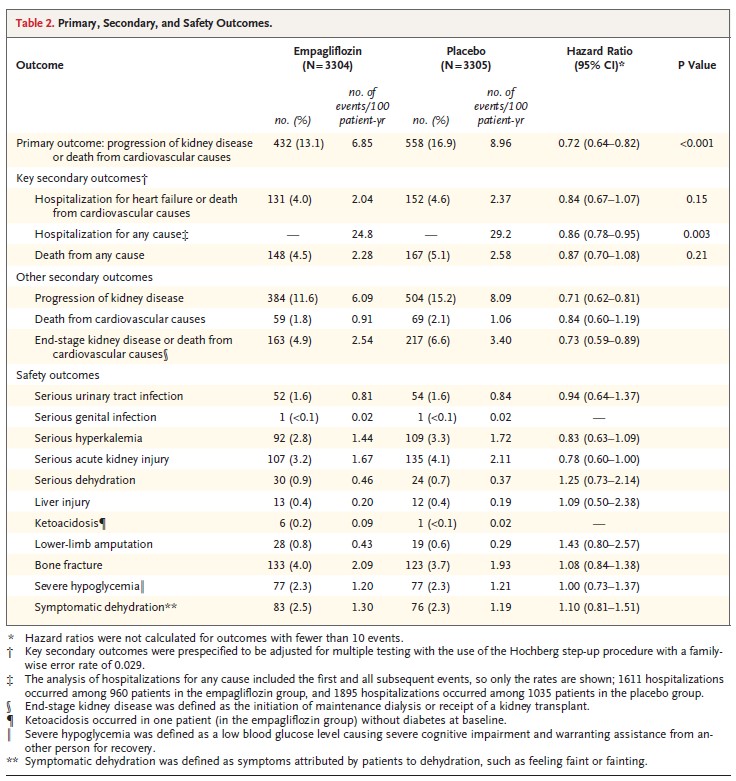
主要な副次アウトカムである「心不全による入院または心血管死」、「全ての原因による入院(初発と再発を含む)」、「全死亡」のプラセボ群に対するエンパグリフロジン群のハザード比は、それぞれ、[0.84 (0.67–1.07); p=0.15]、[0.86 (0.78–0.95); p=0.003]、[0.87 (0.70–1.08); p=0.21]となった。
ゆえに、エンパグリフロジン群の「全ての原因による入院(初発と再発を含む)」に対する有意な効果が示された。
その他の副次アウトカムである「腎疾患の進行」、「心血管死」、「ESKDまたは心血管死の複合」のプラセボ群に対するエンパグリフロジン群のハザード比は、それぞれ、[0.71 (0.62–0.81)]、[0.84(0.60–1.19)]、[0.73 (0.59–0.89)]となった。
<安全性と有害事象>
ケトアシドーシスは、エンパグリフロジン群で6例、プラセボ群で1例に発生した(それぞれ、年間100例あたり0.09および0.02イベント)。
下肢切断は、エンパグリフロジン群で28例、プラセボ群で19例に発生した(それぞれ、年間100例あたり0.43および0.29イベント)。
重篤な尿路感染症、高カリウム血症、急性腎障害、重篤または症候性の脱水、肝障害、骨折の発生率は、両群でほぼ同等であった(表2および表S7)。
エンパグリフロジンの投与により、全体として重篤な有害事象の発現率が増加したという明らかなエビデンスは認められず、また、国際医薬用語集(MedDRA第20.1版)においても、特定の臓器クラスにおける重篤な有害事象の発現率が増加したという明らかなエビデンスは認められなかった。
<臨床測定と検査評価>
エンパグリフロジン群とプラセボ群の平均体重(±SE)の加重平均差は-0.9±0.1kg、収縮期血圧(SBP)は-2.6±0.3mmHg、拡張期血圧(DBP)は-0.5±0.2mmHg、糖化ヘモグロビン(HbA1c)値は-0.39mmol/モルであった(表S9)。
uACR(尿中アルブミン/クレアチニン比)は、エンパグリフロジン群でプラセボ群より19%(95%CI 15~23)低かった。
表S10は、18ヵ月目に患者のサブグループで評価した、ヘマトクリット値とヘモグロビン値で観察された群間差の詳細と、血中カルシウム値、リン酸値、ナトリウム値に臨床的に意味のある差がなかったことを示す。
N Engl J Med. 2023 Jan 12;388(2):117-127.
<第三次および探索的アウトカム>
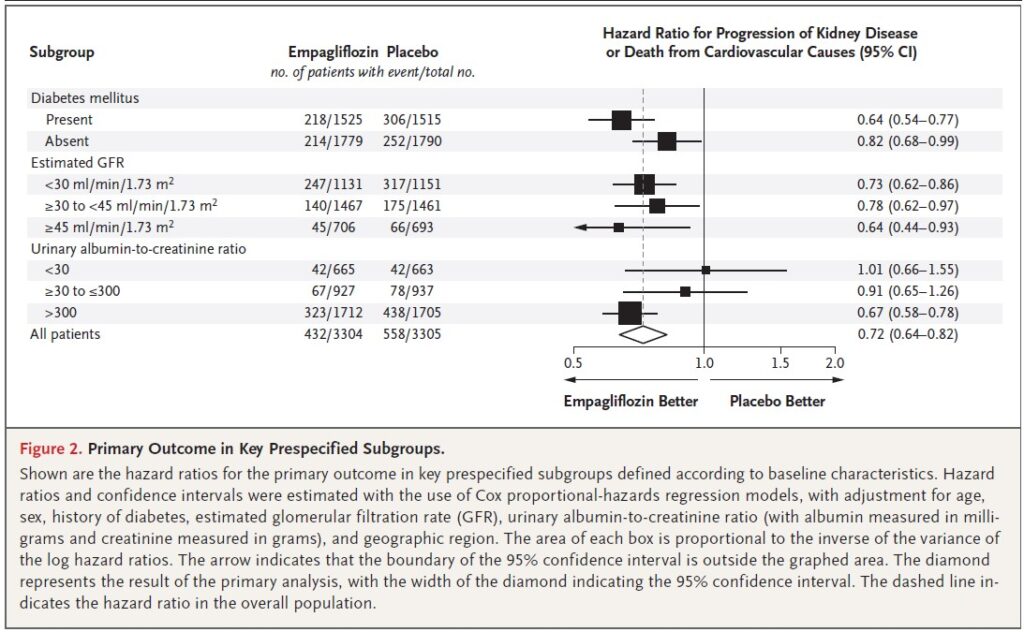
事前に指定された主要評価項目のサブグループ分析は、「ベースラインの糖尿病状態、eGFR、
尿中アルブミン/クレアチニン比」により層別化された。
「心血管死または腎疾患の進行」におけるプラセボ群に対するエンパグリフロジン群のハザード比は、それぞれ、
ベースラインで糖尿病あり:0.64 (0.54–0.77)
ベースラインで糖尿病なし:0.82 (0.68–0.99)
eGFR<30:0.73 (0.62–0.86)
30≦eGFR<45:0.78 (0.62–0.97)
eGFR≧45:0.64 (0.44–0.93)
尿中アルブミン/クレアチニン比<30:1.01 (0.66–1.55)
30≦尿中アルブミン/クレアチニン比<45:0.91 (0.65–1.26)
尿中アルブミン/クレアチニン比>300:0.67 (0.58–0.78)
となり、エンパグリフロジン群の治療効果は、特に、「無作為化時のeGFR、糖尿病の有無」に関わらず、一貫した結果が示された。
尿中アルブミン/クレアチニン比に関しては、その比が高いほど、エンパグリフロジン群の治療効果が高くなる傾向が示された。
N Engl J Med. 2023 Jan 12;388(2):117-127.
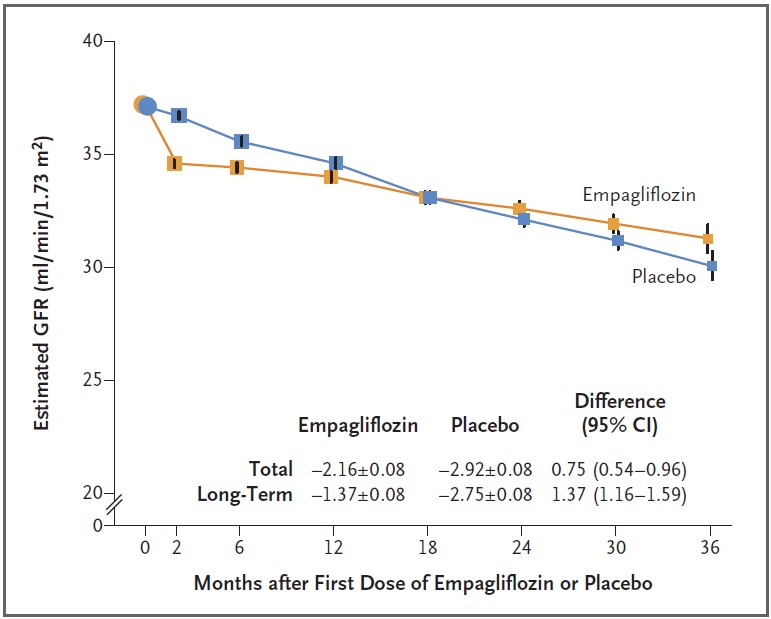
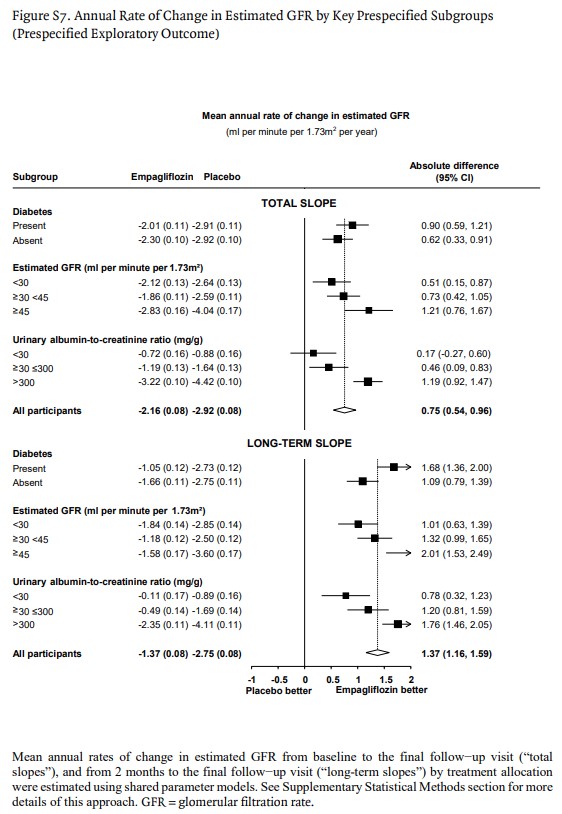
eGFR推定年間低下速度(mL/min/1.73㎡/year)におけるプラセボ群(–2.92±0.08)とエンパグリフロジン群(–2.16±0.08)の差を無作為化から最終フォローアップ時(Total期間)で検討したところ、0.75 (0.54–0.96) mL/min/1.73㎡/yearとなり、エンパグリフロジン群のベネフィットが示された。
また、SGLT2阻害薬投与による初期eGFR低下(イニシャルディップ)後の無作為化2ヶ月後から最終フォローアップ時(Long-Term期間)のeGFR推定年間低下速度(mL/min/1.73㎡/year)におけるプラセボ群(–2.75±0.08)とエンパグリフロジン群(–1.37±0.08)の差を検討したところ、1.37 (1.16–1.59) mL/min/1.73㎡/yearとなり、エンパグリフロジン群のより大きなベネフィットが示された。
また、eGFR推定年間低下速度(mL/min/1.73㎡/year)の群間差は、Total期間とLong-Term期間においても、年間低下速度が速い患者のサブグループ(無作為化時におけるeGFRと尿中アルブミン/クレアチニン比が高い患者)で大きいことが示された。
特定の死因、主要心血管イベント(ハザード比、0.93;95%CI、0.76~1.12)、患者報告による痛風のエピソード、新規発症糖尿病の発症に関して、エンパグリフロジンの有意な効果は観察されなかった。

N Engl J Med. 2023 Jan 12;388(2):117-127.
考察:
様々なGFR、アルブミン尿レベル、CKDの原因を有する患者集団において、エンパグリフロジンは、プラセボと比較して、腎疾患の進行または心血管死(心血管系の原因による死亡)のリスクを28%低下させ、安全性に大きな懸念はなかった。
エンパグリフロジンによる治療は、糖尿病の有無に関わらず、eGFR 20mL/min/1.73㎡までの幅広い腎機能のCKD患者に有効であった。
全ての原因による入院のリスクは、エンパグリフロジンは、プラセボと比較して、14%低下させた。
今回の試験で示されたSGLT2阻害薬による腎疾患の進行または心血管死に対する効果は、CKD患者を対象とした他の2つの大規模臨床試験で示された効果と定量的に類似している。
カナグリフロジンのCREDENCE試験では、対象患者は全例2型糖尿病であり、uACR 300mg/gCr以上であることを条件とし、eGFR 30mL/min/1.73㎡未満の患者は除外した。
ダパグリフロジンのDAPA-CKD試験では、対象患者はuACR 200mg/gCr以上、eGFR 25~75ml/min/1.73㎡であることが条件とした。
DAPA-CKD試験には、糖尿病の無い患者1,398例とeGFR 30ml/min/1.73㎡未満の患者624例が含まれた。
EMPA-KIDNEY試験は、糖尿病の無い3,569例(54.0%)とeGFR 30ml/min/1.73㎡未満
の患者において、一貫した有益性を示したことにより、既存のエビデンスに含まれるより幅広い患者像に対するエビデンスを追加した。
uACR 300mg/gCr未満の患者3,192例(48.3%)が含まれていたにも関わらず、これらの患者のCKD進行速度は、uACR 300mg/gCr以上の患者よりも遅かったため、主要評価項目のイベント数は限られていた。
事前に指定したeGFR推定年間低下速度(mL/min/1.73㎡/year)の探索的データ解析では、
uACR 300mg/gCr未満の患者(uACR 30mg/gCr未満の患者を含む)において、eGFR推定年間低下速度を遅延させることが示された。
本試験の主な長所は、大規模で広範な適格基準、試験レジメンに対する高いアドヒアランス、ほぼ完全な追跡調査である。
心血管系イベントの発生件数は、予想より少なかったため、二次および三次の心血管系アウトカムを評価する統計的検出力が低下した等の限界があるが、心血管系アウトカムのハザード比は、これまでのエビデンス全体の結果と一致していた。
メタアナリシスにおいて、SGLT2阻害薬は、心血管死の相対リスクを14%低下させ[HR 0.86(95%CI 0.81〜0.92)]、心不全による入院または心血管死の相対リスクを23%低下させた[HR 0.77(95%CI 0.74〜0.81)]。
結論:
eGFR 30 mL/min/1.73㎡未満、非糖尿病、uACR(尿中アルブミン/クレアチニン比)が低い患者を多く含むCKD進行リスクの幅広い患者において、エンパグリフロジンによる治療は、プラセボよりも腎疾患の進行または心血管死のリスクを低下させた。
