PubMed URL:https://pubmed.ncbi.nlm.nih.gov/38816204/
タイトル:Kidney outcomes of SGLT2 inhibitors among older patients with diabetic kidney disease in real-world clinical practice: the Japan Chronic Kidney Disease Database Ex
<概要(意訳)>
序論:
糖尿病性腎臓病(DKD)は2型糖尿病(T2DM)を有する高齢患者において重大な医療上の懸念事項です。
DKDの診断は2つの基準に依存しています:推定糸球体濾過量(eGFR)の低下(60 mL/min/1.73 m²未満)と、T2DM患者におけるアルブミン尿またはタンパク尿の存在です。
しかし、これらの臨床的意義は患者の年齢によって異なる可能性があります。
加齢に伴い、多くの患者はGFRの進行性低下を示し、年齢層間でのeGFRの低下はアルブミン尿やタンパク尿の発生率と比較してより顕著です。
このため、若年患者と比較して、T2DMを有する高齢患者は非アルブミン尿性または非タンパク尿性DKDに分類される割合が高くなります。
基礎病理はアルブミン尿やタンパク尿の有無によってDKD患者間で異なることが示されており、eGFRの低下率にも相違が存在します。
SGLT2阻害薬は、当初T2DMの治療において血糖降下作用のみを目的として承認されましたが、T2DMの有無に関わらず慢性腎臓病(CKD)患者における腎保護および心血管保護効果が次第に認識されるようになっています。
いくつかの臨床試験では年齢に関係なくSGLT2阻害薬の有益性が示されていますが、高齢DKD患者のみに焦点を当てた研究はほとんど報告されていません。
この状況が、若年患者と比較して高齢患者におけるSGLT2阻害薬の処方率が低いことの一因となっている可能性があります。
さらに、タンパク尿の有無によるDKDを有する高齢患者間での効果の潜在的な差異については不明確なままです。
本研究は、日本慢性腎臓病データベース(J-CKD-DB-Ex)を用いて、SGLT2阻害薬と他の血糖降下療法を開始したDKDを有する高齢患者におけるeGFRの変化と腎アウトカムの比較に焦点を当てました。
さらに、異なる患者サブグループにおけるSGLT2阻害薬の使用に関連する腎アウトカムの変動を評価しました。
方法:
J-CKD-DB-Exは、21の日本の大学病院からの電子健康記録(EHR)に基づく広範な多施設共同レジストリで、慢性腎臓病(CKD)患者の大規模データを蓄積したものであり、詳細は先行研究に記載されています。
簡潔に述べると、このレジストリは2014年12月に開始され、診断から治療に至るまでの広範な患者データを収集しています。
参加施設はすべて、標準化された構造化医療情報交換システム2(Standardized Structured Medical record Information eXchange 2)のストレージと転送システムを含む、先進的なEHR基準の遵守が義務付けられています。
患者データが匿名化されていることを踏まえ、各参加大学病院のウェブサイトでオプトアウト方式を用いて、「人を対象とする医学系研究に関する倫理指針」に従ってインフォームドコンセントを実施しました。
J-CKD-DB-Exデータベースの5つの病院が、2014年1月1日から2020年12月31日までの進行中の前向き縦断研究に参加することに同意しました。
75歳以上のT2DM患者で、SGLT2阻害薬または他の血糖降下薬を新たに開始した患者の医療記録を選択しました。
治療開始の基準日(index date)は、適応に従って患者が最初に処方を受けた、または調剤を受けた時点としました。
SGLT2阻害薬にはルセオグリフロジン、イプラグリフロジン、ダパグリフロジン、カナグリフロジン、エンパグリフロジン、トホグリフロジンが含まれ、一方、他の血糖降下薬にはDPP-4阻害薬、ビグアナイド、α-グルコシダーゼ阻害薬(aGI)、グリニド、スルホニル尿素薬、チアゾリジン、インスリン、およびGLP-1受容体作動薬が含まれ、これらは初期治療または追加治療として使用されました。これらの薬剤には配合剤も含まれます。
患者にとって治療が新規であることを確認するため、過去1年間にその薬剤クラスの処方がなかった症例のみを対象としました。
選択基準として、各薬剤の開始用量に関する推奨投与量と投与方法に従いました。
開始用量は各薬剤によって異なりますが、適応外使用はすべて除外しました。
SGLT2阻害薬は単独で開始された場合のみ、新規開始として含めました。
他の血糖降下薬が新たに開始された場合は、単剤または配合剤のいずれかを含めました。
基準日前180日以内に少なくとも1回のeGFR測定値があるT2DM患者の記録のみを含めるよう選択を絞りました。
治療開始前のeGFR変化を確実に推定するため、基準日前181~365日の期間から少なくとも1回のeGFR測定値を必要としました。
また、基準日後120日以内に少なくとも1回のeGFR測定値も必要としました。
さらに、選択基準には基準日後の最初のeGFR測定日から180日以上経過した後に少なくとも1回の追加eGFR測定値があることも含まれていました。
患者を基準日から、基準治療の終了時(オントリートメント解析のみ)、診療やデータベースからの移動または離脱、死亡、またはデータ利用可能な最終日まで追跡しました。
血清クレアチニンは酵素法により採取・測定されました。
eGFRは日本人係数で修正されたChronic Kidney Disease Epidemiology Collaboration方程式を用いて算出しました。
尿検査はスポット尿検体に対してディップスティック法を適用しました。
日本臨床検査標準協議会(JCCLS)の方針では、すべての尿ディップスティック検査は、異なる検査ストリップメーカー間で比較可能な結果が得られるよう製造されるべきとされています。
具体的には、尿ディップスティック結果の(1+)、(2+)、(3+)はそれぞれ尿中タンパク質レベル30、100、250~500 mg/dLに相当します。
本研究では、尿ディップスティック結果が(1+)以上の場合をタンパク尿と定義しました。治療開始前のeGFR急速低下(イニシャルディップ)は、年間3.0 mL/min/1.73 m²以上のeGFR低下と定義しました。
主要アウトカムは、追跡期間中のSGLT2阻害薬または他の血糖降下薬開始からのeGFR変化率の有効性を比較することでした。
副次アウトカムは、両群間での複合腎イベントおよび個別腎イベントの発生率(1000人年あたり)を比較することでした。
末期腎臓病(ESKD)はeGFR 15 mL/min/1.73 m²未満と定義され、その診断はその後の測定によっても確認されました。
複合腎エンドポイントは、eGFRの40%以上の持続的低下(その後の測定で確認)またはESKD発症(その後の測定で確認)と定義されました。
複合エンドポイント解析では、患者に複数のイベントが発生した場合、最初のイベントをアウトカムとして記録しました。
感度分析では、エンドポイント特異的分析を実施しました。
これらの分析では、患者が経験したすべての腎イベントを個別にアウトカムとして記録しました。
例えば、最初にeGFRが40%以上低下し、その1か月後にESKDと診断された患者の場合、複合エンドポイント解析ではeGFR低下40%以上のみをアウトカムとして記録しました。エンドポイント特異的分析と感度分析では、eGFR低下40%以上とESKD診断を別々のアウトカムとして記録しました。
結果:
傾向スコアマッチング前には、SGLT2阻害薬による治療を開始した368名の患者と、他の血糖降下薬による治療を開始した899名の患者が適格基準を満たしていることを確認しました。
SGLT2阻害薬新規開始群は、他の血糖降下薬群と比較して若年であり、HbA1c値が高値でした。
基準日前の年間平均eGFR変化率および基準日におけるタンパク尿の有病率については、両群間に有意差はありませんでした。
SGLT2阻害薬群では降圧薬の使用頻度が高く、特にARB、ACE阻害薬、および利尿薬が多く処方されていた一方、DPP-4阻害薬、α-グルコシダーゼ阻害薬、インスリン、およびグリニドの処方は少なかったです。
傾向スコアマッチングに基づき、本研究ではSGLT2阻害薬を新たに処方された348名の患者と、同数の他の血糖降下薬を新たに処方された患者を分析しました。
傾向スコアマッチング後の群間では、すべての変数において標準化差が10%未満でした。
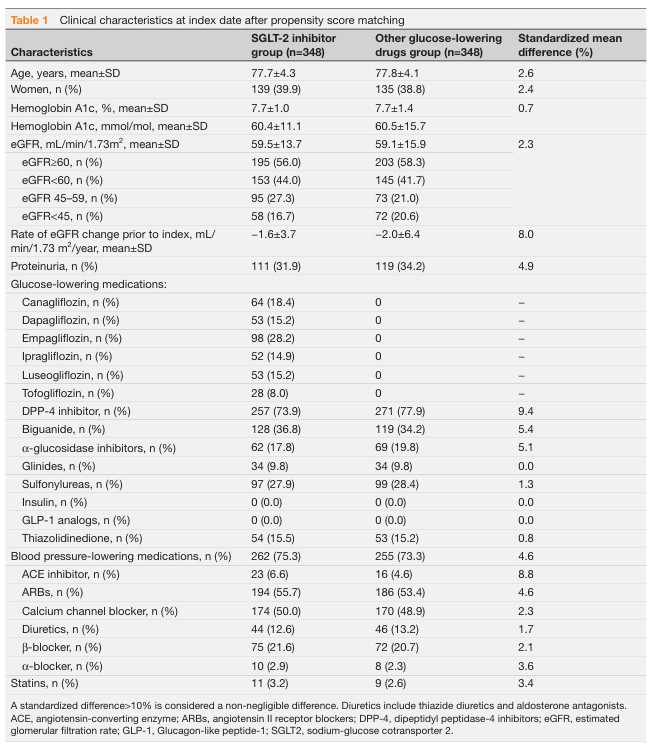
全696名の患者において、治療開始時の平均年齢は77.7歳、274名(39.4%)が女性、平均eGFRは59.3 mL/min/1.73 m²、298名(42.8%)がeGFR 60 mL/min/1.73 m²未満、平均HbA1cは60 mmol/mol(7.7%)であり、230名(33.0%)の患者にタンパク尿が認められました。
基準日時点で、409名(58.8%)の患者がACE阻害薬またはARBで治療されていました。
表1は傾向スコアマッチング後の基準日における特性を示しています。
DPP-4阻害薬が最も頻繁に処方された他の血糖降下薬でした。
BMJ Open Diabetes Res Care. 2024 May 30;12(3):e004115.
主要分析におけるフォローアップ期間の平均(±標準偏差)は、SGLT2阻害薬群で31.1±16.6ヶ月、他の血糖降下薬群で29.6±18.6ヶ月でした。
追跡期間中、eGFR測定回数の中央値はSGLT2阻害薬群で18回(四分位範囲10~25回)、他の血糖降下薬群で15回(9~27回)でした。
基準日前後の各月におけるeGFR測定値の推移はオンライン補足表S3に示されています。
本研究は実臨床データの解析を含むため、月ごとの症例数にばらつきがあります。
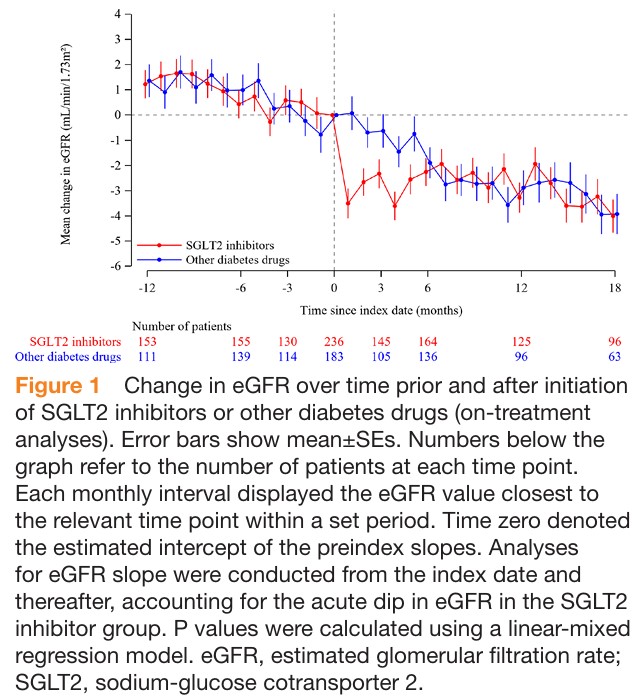
OTT解析では、基準治療開始前のeGFR年間変化率の平均(±標準誤差)はSGLT2阻害薬群で1.47±0.15 mL/min/1.73 m²、他の血糖降下薬群で1.10±0.18 mL/min/1.73 m²でした(図1)。
SGLT2阻害薬および他の血糖降下薬の新規処方後のeGFR変化率はそれぞれ−0.80 mL/min/1.73 m²/年(95%信頼区間−1.05~−0.54)および−1.78 mL/min/1.73 m²/年(95%信頼区間−2.08~−1.49)でした。
両群間のeGFR低下率の差は0.99 mL/min/1.73 m²/年(95%信頼区間0.5~1.38)で、SGLT2阻害薬が優位でした(p<0.001)。
SGLT2阻害薬群では、フォローアップ期間の最初の5~6ヶ月間にeGFRが急性に低下(初期ディップ)し、その後安定化しました。
初期ディップには2つのピークがあるように見受けられました(図1、オンライン補足表S3)。
BMJ Open Diabetes Res Care. 2024 May 30;12(3):e004115.
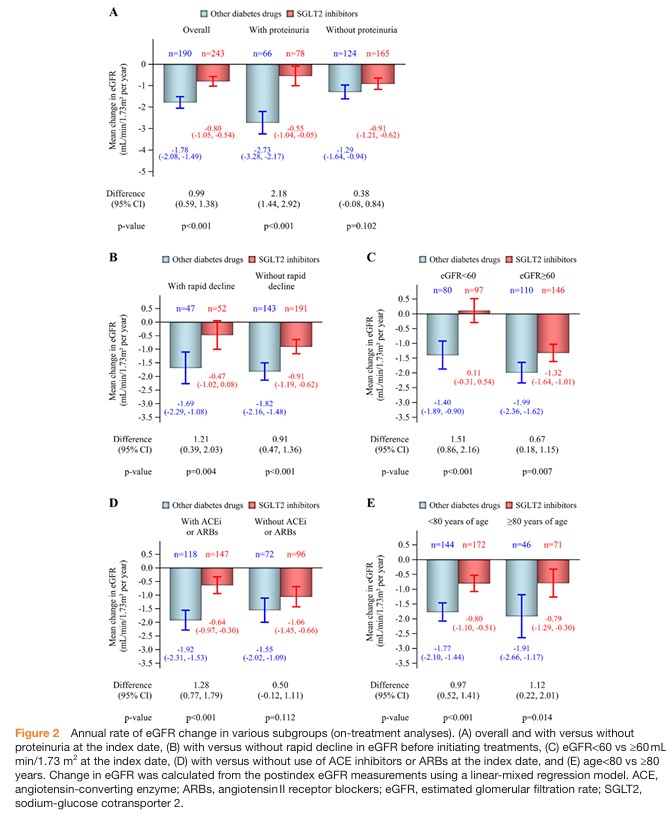
事前に規定されたサブグループにおけるeGFR年間変化率を図2に示します。
SGLT2阻害薬とタンパク尿、eGFR(60 mL/min/1.73 m²未満 vs 60以上)、基準日時点でのACE阻害薬またはARB使用の有無との間に交互作用が認められ、eGFR低下との関連が示されました(交互作用のp値はそれぞれp<0.001、p=0.019、p=0.048)。
しかし、SGLT2阻害薬使用と治療開始前のeGFR急速低下、および年齢(80歳未満 vs 80歳以上)との間には交互作用はありませんでした。
ITT集団では、両群ともeGFR変化の軌跡はOTT集団のものと類似していました(オンライン補足図S3)。
SGLT2阻害薬使用と基準日時点でのACE阻害薬またはARB使用との間には、eGFR低下との関連において交互作用の傾向があり(交互作用のp=0.050)、他のサブグループ解析でも同様の結果が得られました(オンライン補足図S4)。
BMJ Open Diabetes Res Care. 2024 May 30;12(3):e004115.
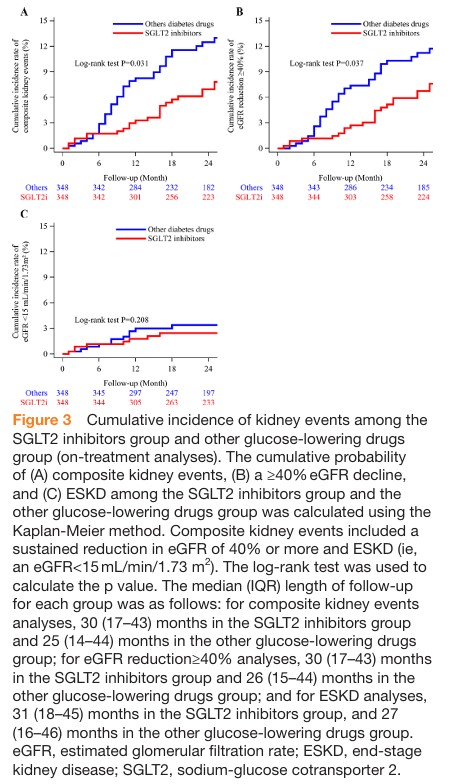
腎イベントの累積発生率を図3に示します。
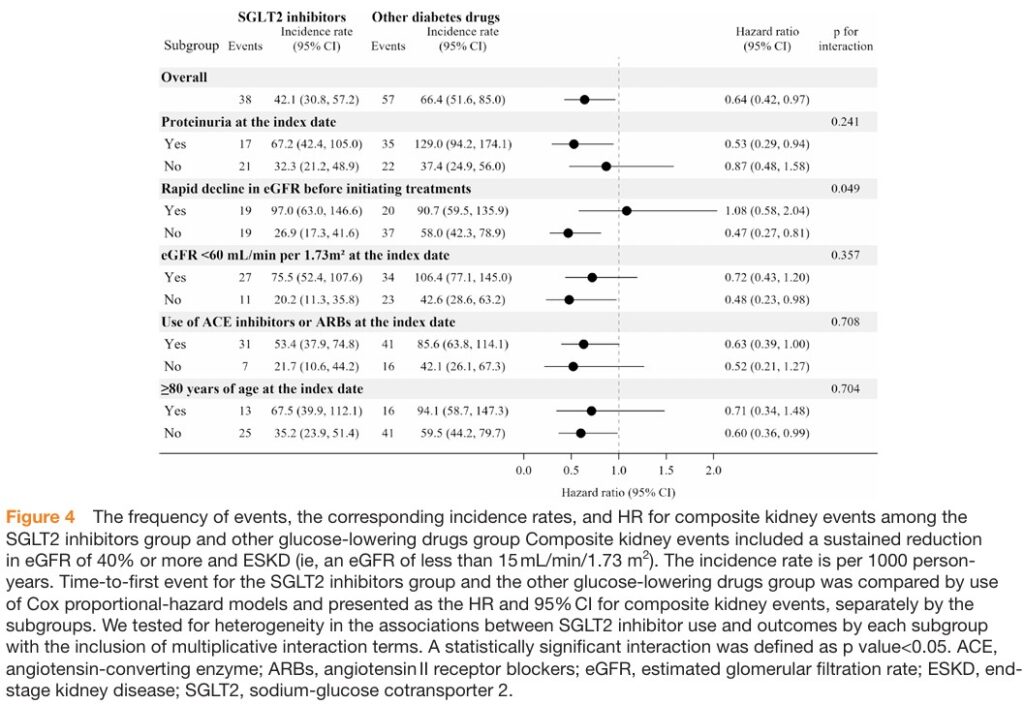
eGFR40%以上低下とESKDの複合イベントは、SGLT2阻害薬群で38例、他の血糖降下薬群で57例発生しました。
発生率は他の血糖降下薬群で1000人年あたり66.4イベント、SGLT2阻害薬群では1000人年あたり42.1イベントでした。
観察期間中、SGLT2阻害薬群ではeGFR40%以上の低下が38例、ESKDが10例発生しました。
比較すると、他の血糖降下薬群ではそれぞれ56例と17例が発生しました。
Coxモデルによる解析では、SGLT2阻害薬群は他の血糖降下薬群と比較して複合イベントのリスクが低いことが示されました(ハザード比0.64、95%信頼区間0.42~0.97)。
BMJ Open Diabetes Res Care. 2024 May 30;12(3):e004115.
治療開始前のeGFR急速低下の有無に関して、SGLT2阻害薬群と他の血糖降下薬群の腎イベントリスクには不均一性が認められました(交互作用のp=0.049)。
基準日時点でのタンパク尿の有無、eGFR(60 mL/min/1.73 m²未満 vs 60以上)、ACE阻害薬またはARB使用の有無、または年齢(80歳未満 vs 80歳以上)に基づくサブグループ解析では、複合イベントの発生率に群間差はありませんでした(図4)。
BMJ Open Diabetes Res Care. 2024 May 30;12(3):e004115.
フォローアップ期間中、SGLT2阻害薬群ではeGFR50%以上の低下が19例、30%以上の低下が72例発生した一方、他の血糖降下薬群ではそれぞれ35例と90例が発生しました。
考察:
本研究では、全国規模の多施設CKD患者レジストリと実臨床の電子健康記録に基づき、75歳以上のDKD患者においてSGLT2阻害薬による治療を開始した群が、他の血糖降下薬と比較してeGFR低下率が有意に緩やかであるという証拠を見出しました。
SGLT2阻害薬のeGFR低下抑制効果は、タンパク尿を有する患者、eGFRが60 mL/min/1.73 m²未満の患者、および基準日時点でACE阻害薬またはARBを服用している患者でより大きいことが示されました。
さらに、SGLT2阻害薬による治療開始は、他の血糖降下薬と比較して、eGFR40%低下または新規ESKD発症という複合エンドポイントのリスクを低減しました。
SGLT2阻害薬の腎イベントに対する有益性は、タンパク尿の有無、eGFR値(60 mL/min/1.73 m²未満)、基準日時点でのACE阻害薬またはARBの使用、および年齢区分(80歳以上)に関わらず、すべてのサブグループで一貫して観察されました。
T2DMを有するCKD患者に関する過去の報告と同様に、SGLT2阻害薬の開始後には初期ディップが観察されました。
本研究では、初期ディップに2つのピークがあるように見受けられました。
考えられる説明の一つとして、75歳以上の患者では不均一な臨床特性のため、初期ディップの大きさや持続時間が患者間で異なる可能性があります。
この知見は、高齢患者でSGLT2阻害薬を開始後、最初の6ヶ月間は腎機能のモニタリングが必要であることを示唆しています。
高齢者は多様な集団であり、臓器機能の能力、自己管理能力、サルコペニア、および全体的な依存度において大きな個人差があります。
高齢T2DM患者の薬物療法選択においては、治療の複雑さ、副作用、および潜在的な薬物相互作用の考慮が極めて重要です。
エンパグリフロジンのEMPA-REG OUTCOME試験とダパグリフロジンのDECLARE-TIMI 58試験の解析では、T2DM患者の3つの年齢コホート(65歳未満、65~74歳、75歳以上)において、SGLT2阻害薬の腎保護効果と安全性プロファイルが同等であることが示されました。
SGLT2阻害薬投与後の事前に規定された有害事象の報告を評価するグローバル市販後調査では、高齢患者においてより頻繁に報告された有害事象はありませんでした。
本研究の解析では、80歳以上の患者においてもSGLT2阻害薬開始からのeGFR変化率の有効性が観察され、年齢サブグループ間で複合イベントに差はありませんでした。
さらに、SGLT2阻害薬開始前のeGFR変化率によって影響を受ける腎機能に対するSGLT2阻害薬の影響を調査した研究は不足しています。
この考察は臨床的に重要な意義を持ちます。
なぜなら、eGFRの急速な低下を経験している個人は、差し迫った腎不全の高リスク群を構成するためです。
本研究の解析では、SGLT2阻害薬開始前にeGFRの急速な低下を経験したDKDを有する高齢患者では、そのような低下のなかった患者と比較して、SGLT2阻害薬使用に関連する複合腎イベントの減少が比較的少ないことが観察されました。
一方で、治療開始前のeGFR急速低下とSGLT2阻害薬使用の間に統計的に有意な差はなく、治療開始前にeGFRの急速な低下を経験した患者では数値的にeGFR低下の緩和がより大きかったです。
この変動は平均への回帰によって説明できるかもしれません。
これは、治療の種類にかかわらず、以前に急速な低下を示した患者群はその後eGFR低下がより緩やかになる傾向があることを示唆しています。
本研究の堅牢性は、治療開始前後の複数のeGFR測定値の利用可能性と様々なサブグループ間での一貫性分析によって裏付けられています。
大規模なJ-CKD-DB-Exデータリポジトリにより、SGLT2阻害薬または他の血糖降下薬の投与前の腎機能低下率に基づいた患者の層別化が可能となりました。
傾向スコアマッチングや複数の感度分析などの厳格な統計手法の適用により研究結果は強化されていますが、本研究は観察研究デザインであるため、血圧や社会経済的状況などの未測定の交絡因子の可能性を完全に排除することはできません。
しかしながら、日本では全国民に対して国民皆保険制度を提供しているため、SGLT2阻害薬と他の血糖降下薬のどちらで治療を開始するかという意思決定プロセスに経済的要因が大きく影響する可能性は低いでしょう。
データベースはネットワーク内のすべての医療記録の収集を可能にしましたが、ネットワーク外のデータへのアクセスはできませんでした。
本研究では尿タンパクの評価にディップスティック法を用いました。
ディップスティック法は費用対効果が高く標準化に有用ですが、尿中アルブミン/クレアチニン比や尿タンパク/クレアチニン比と比較して感度と特異性に限界があります。
また、血圧低下だけではSGLT2阻害薬の腎機能に対する観察された有益性をすべて説明することはできません。
先行試験と同様に、eGFRの傾きは線形モデルを用いて計算されました。
しかし、SGLT2阻害薬治療開始後のeGFR軌跡を正確に描写するには線形モデルが最適なアプローチではない可能性があることに注意すべきです。
本研究では腎アウトカムのみに焦点を当て、抽出データは電子医療記録情報の一部であったため、安全性パラメータは未探索のままでした。
したがって、特にDKDを有する高齢患者におけるSGLT2阻害薬の安全性側面、機能状態、生活の質に関する指標を精査するためにさらなる研究が不可欠です。
また、マッチングや患者除外のプロセス中に選択バイアスが発生した可能性もあります。
さらに、eGFR評価には治療開始前後の特定の観察回数が必要なため、バイアスが生じる可能性があります。このアプローチは先行研究で評価された手順と一致しています。
最後に、SGLT2阻害薬の長期効果を評価するためには、観察研究から延長フォローアップデータを確保することが不可欠です。
本研究は先行ランダム化研究からの知見を補完するものであり、臨床試験で示されたSGLT2阻害薬の腎機能と腎イベントへの肯定的な影響がDKDを有する高齢患者にも適用される可能性があることを示唆しています。
