PubMed URL:https://pubmed.ncbi.nlm.nih.gov/40343436/
タイトル:Dapagliflozin vs empagliflozin in patients with chronic heart failure: a registry analysis
<概要(意訳)>
序論:
欧州心臓病学会(ESC)が発行する心不全患者管理に関する現行ガイドラインでは、ナトリウム・グルコース共輸送体2阻害薬(SGLT2i)であるダパグリフロジンとエンパグリフロジンの2剤が、左室駆出率(LVEF)の全範囲にわたる慢性心不全(CHF)において、疾患修飾効果を有する唯一の薬物治療選択肢として位置づけられています。
したがって、駆出率が低下した心不全(HFrEF, LVEF≤40%)、軽度低下した心不全(HFmrEF, LVEF 41%-49%)、または維持された心不全(HFpEF, LVEF≥50%)の患者には、これらの薬剤による治療が強く推奨されています。
方法:
研究概要
本解析は、クロアチアのザグレブにあるDubrava大学病院で管理されているCHF患者レジストリ(CaRDレジストリ、NCT06090591)において、日常診療で収集されたデータに基づいており、当施設の倫理委員会の承認(2022/1403-01)を得て実施されました。
当施設は教育機関であり、全患者が自身の匿名化されたデータを研究および出版目的で使用することに同意しています。
2022年1月1日から2023年7月31日までの期間に、ダパグリフロジンまたはエンパグリフロジンによる治療を開始した患者を解析対象としました。
CHF治療における両薬剤の規制承認時期の違いから、一部の患者(既存患者)では、他のCHF治療開始後、最低1か月から最長10か月の遅れをもってSGLT2iが開始されました 。 一方、他の患者(新規患者)では、CHF診断と同時に、他のCHF治療と共にSGLT2iが開始されました。
第一段階として、これら2つの患者群(「研究1」:既存患者、「研究2」:新規患者)を個別に解析しました。
研究1と研究2で得られた推定値が概ね同様であったため、データを統合して解析を行いました(既存患者+新規患者)。
最後に、慢性腎臓病(CKDまたは腎機能正常)およびベースラインのLVEF(HFrEFまたはHFm/pEF)が、ダパグリフロジンとエンパグリフロジンの治療効果に与える影響(効果修飾)を検討しました 。
アウトカム
研究期間は、追跡期間中のイベント(特に治療中止や薬剤変更)による影響を最小限に抑えるため、6か月に限定しました。
主要アウトカムは、この6か月間における全死亡と主要心血管イベント(MACE)の複合としました。これは、競合イベントによるバイアスを避けるためです。
また、実臨床環境、特に院外死亡例において死因特定が困難な場合があるため、誤分類バイアスを避ける目的で、原因特異的死亡ではなく全死亡を採用しました。
院内死亡はイベントと発生時期を直接特定し、院外死亡は近親者への連絡と死亡診断書によって確認しました。
MACEは、(i)心不全悪化(心不全による入院または救急外来受診、症状増悪による予定外受診)、(ii)急性心筋梗塞/急性冠症候群、(iii)脳血管イベント/一過性脳虚血発作、(iv)肺塞栓症、(v)深部静脈血栓症と定義しました。
MACEのイベントと発生時期は、直接または病院情報システムを通じて確認しました。 MACEの発生率は、1回以上のMACEを経験した患者の割合としました。
副次アウトカムは、6か月時点の評価におけるNew York Heart Association(NYHA)心機能分類としました。
選択バイアスを避けるため、研究期間中に死亡した患者にはNYHA分類Vを割り当てました。
これは、死亡確率が割り当てられたSGLT2iによって影響を受ける可能性を考慮し、生存者のみを対象とした場合に生じうるバイアス(死亡率の高い治療群でNYHA分類が良好に見える可能性)を避けるためです。
その他のアウトカム(NT-proBNP値、LVEF、eGFR)は、6か月時点の評価で生存していた患者のみで記録しました。
統計学的考察
サンプルサイズの計算は実施しませんでしたが、手元のデータから両SGLT2iの相対的有効性について有意義な知見が得られると考えました。
LVEF値が広範囲にわたる患者が含まれていたため、6か月間の主要アウトカム発生率は10~15%程度と予想され、両群で同等であると見込まれました。
特に研究1(既存患者)および全体では、これにより推定値が比較的安定すると考えられました。
研究1と研究2それぞれにおいて、ダパグリフロジン群とエンパグリフロジン群の患者背景を均等にするため、最適化ベースの重み付けを用い、平均治療効果(ATE)を推定しました。
この手法は、事前に設定した基準を満たすように、観察された共変量の経験分布を調整する最小分散の重みを見つけます。
Rのoptweightパッケージを使用し、標準化平均差(SMD)が0.1未満であることをバランスが取れている指標としました。
人口統計学的情報、CHF特性、併存疾患、併用薬など、41の共変量を調整対象としました 。 いずれの共変量にも欠測値はありませんでした 。
一次解析は研究1と研究2で個別に実施しました。
二次解析では、統合データを(i)単純統合(ナイーブアプローチ)、(ii)固定効果1段階個別患者データメタ解析、(iii)混合効果メタ解析として分析しました。
CKDとLVEFによる効果修飾を検討するため、CKDの有無、HFrEF/HFm/pEFの別で患者を層別化し、各層で共変量のバランスを取りました。
解析モデルには、治療と各層(CKD/LVEF)との交互作用項を含めました。
感度解析
観察研究に固有の残存交絡の可能性を考慮し、どちらかの治療に不利な強いバイアス(主要アウトカムのRR=1.40、NYHA分類のOR=1.50)を仮定し、観察された効果推定値を補正する感度解析を計画しました。
また、治療間に差が見られた場合、その差を打ち消すために必要な交絡効果の大きさを示すE値を算出しました。
結果:
患者の適格性と特性
合計961人の患者が解析対象となり、その多くは研究1に含まれました。
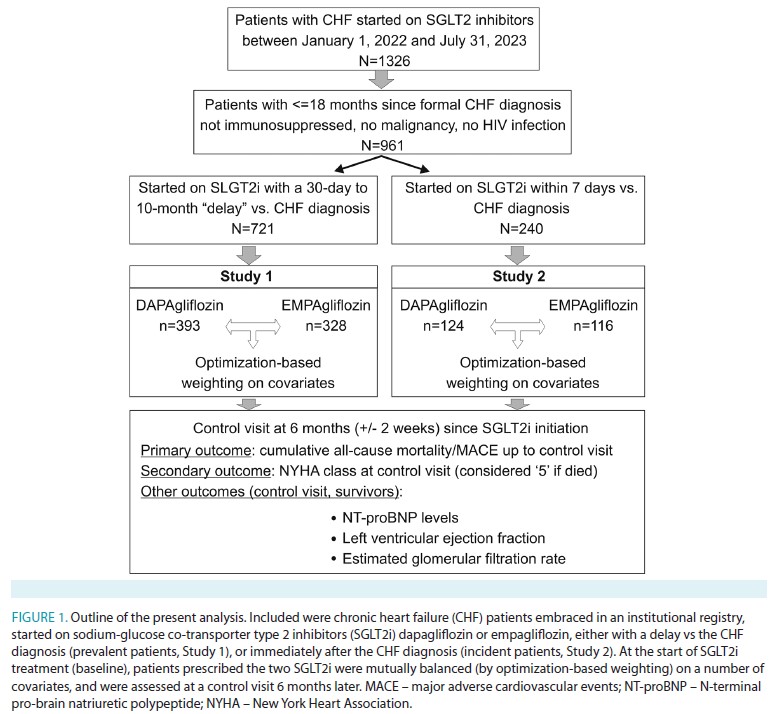
ダパグリフロジン群とエンパグリフロジン群の患者数は、両研究において同程度でした[ダパグリフロジン(研究1で393人、研究2で126人)とエンパグリフロジン(研究1で328人、研究2で114人)が処方された患者数は同程度でした(Figure 1)]。
Croat Med J. 2025 May 7;66(2):135-152.
重み付け前、両群の患者背景には多くの項目で差が見られましたが 、重み付けにより、両研究においてすべての共変量で適切なバランス(SMD < 0.1)が得られました(Table 1、Table 2)。
主要および副次アウトカム:一次解析
6か月時点の評価は、SGLT2i開始から183~184日の範囲で実施されました。
研究1では、82人(11.4%)が主要アウトカムを経験し(38人死亡、53人MACE)、MACEの多くは心不全悪化でした。
主要アウトカムの発生率は、エンパグリフロジン群(重み付け後9.2%)よりもダパグリフロジン群(同12.8%)でやや高い傾向が見られました。
また、ダパグリフロジン群は、より重症なNYHA分類を示す傾向がありました。
研究2でも、主要アウトカムの発生率はダパグリフロジン群(重み付け後11.3%)の方がエンパグリフロジン群(同5.2%)よりも高く 、NYHA分類も同様の傾向を示しました。
調整後の相対リスク(RR)の点推定値は、両研究で1.0を超えましたが(RR > 1.28)、信頼区間(CI)は広いものでした(Table 3)。
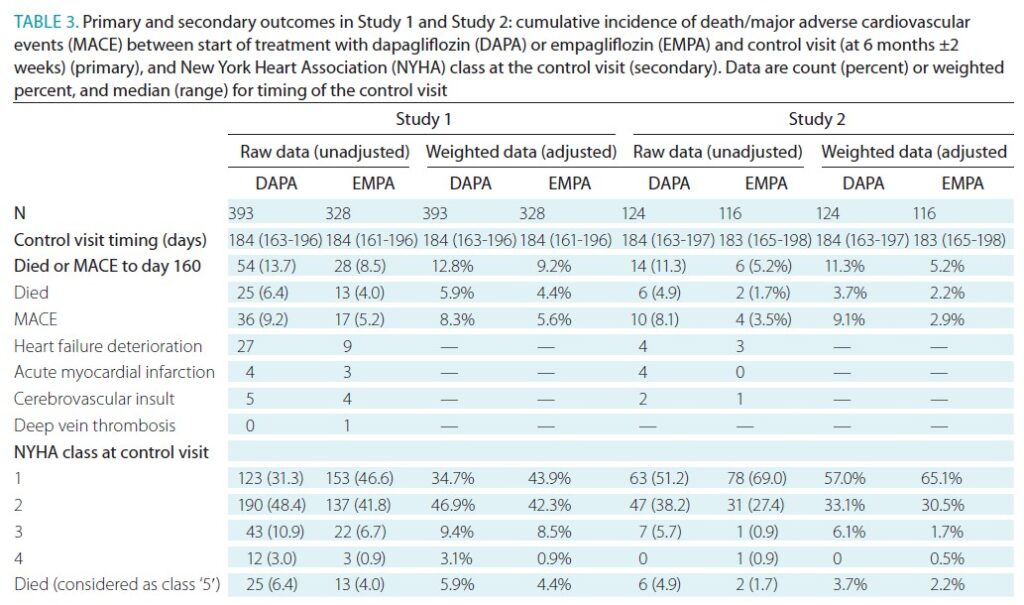
Croat Med J. 2025 May 7;66(2):135-152.
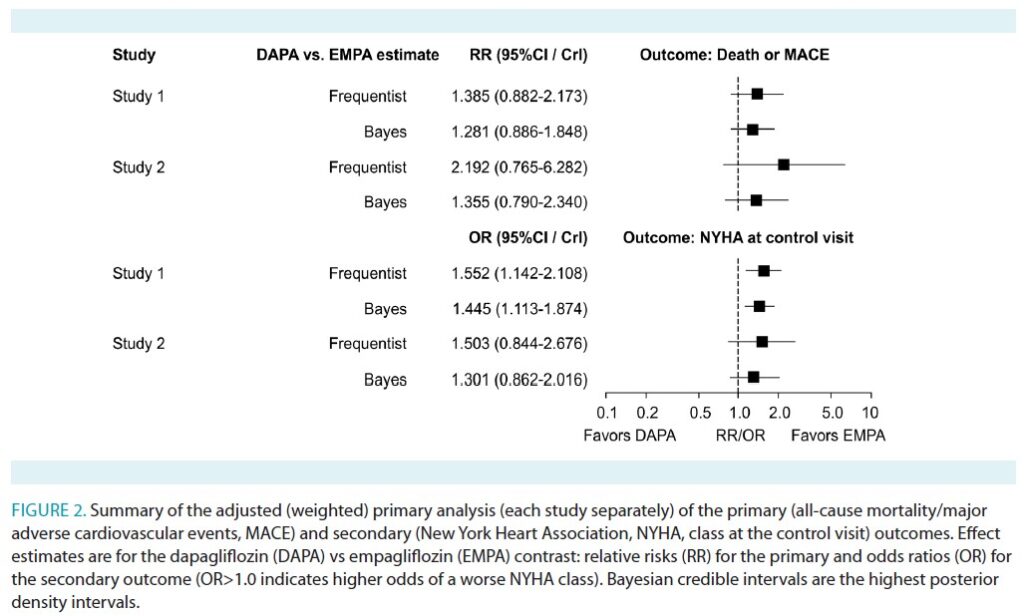
副次アウトカム(NYHA分類)について、研究1では、ダパグリフロジン群でより重症なNYHA分類を示すオッズが高いことが示唆されました(頻度論的OR=1.552, 95%CI 1.142-2.108; ベイズOR=1.445, 95%CrI 1.113-1.874)。
研究2でも同様の傾向が見られましたが、CIは1.0をまたぎました (Figure 2)。
Croat Med J. 2025 May 7;66(2):135-152.
主要および副次アウトカム:二次解析と感度
統合・重み付けデータでは、両群の患者背景は適切にバランスされていました。
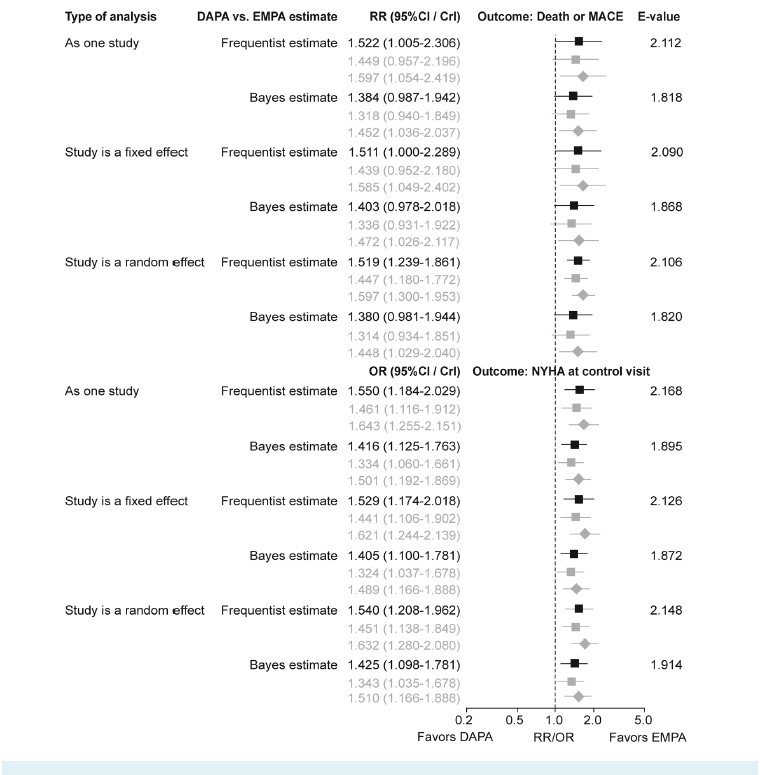
統合解析の結果、主要アウトカムに関して、頻度論的推定値はダパグリフロジン群で約51%高いリスクを示唆しました(RR=1.519, 95%CI 1.239-1.861)。
ベイズ推定値はやや低いものの、同様の傾向を示しました。
副次アウトカムに関しても、ダパグリフロジン群でより重症なNYHA分類を示すオッズが高いことが示唆されました(頻度論的OR=1.540, 95%CI 1.208-1.962; ベイズOR=1.425, 95%CrI 1.098-1.781)。
感度解析では、ダパグリフロジンに不利な強い交絡バイアスを仮定しても、推定値は依然として1.0を超える傾向を維持しました。
E値の計算結果は、観察された差を打ち消すには、かなり強い交絡因子(RR/OR 1.820~2.168)が必要であることを示唆しました(Figure 3)。

その他のアウトカム
6か月時点でのNT-proBNP値、LVEF、eGFR値(生存者のみ)は、両研究において群間で類似していました(Supplemental Material 1)。
慢性腎臓病と駆出率による効果修飾の探索
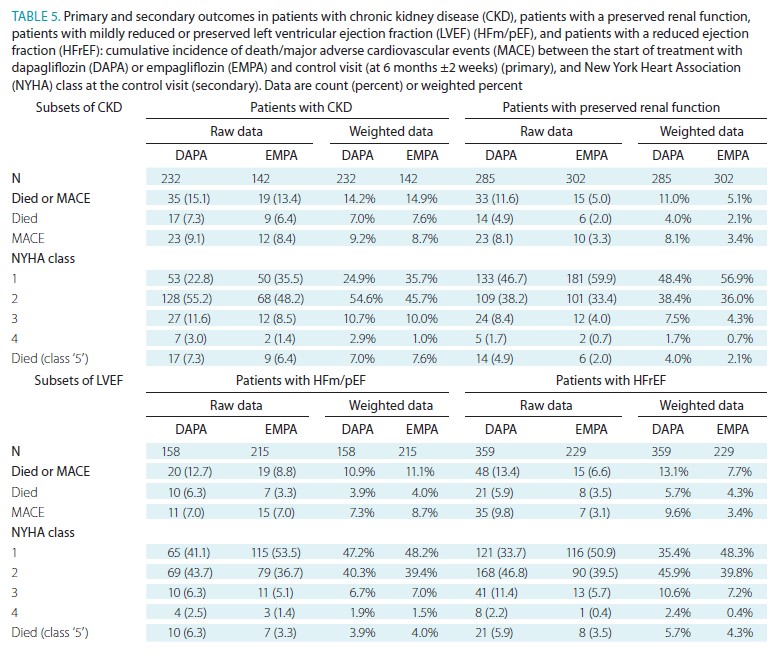
CKD患者(ダパグリフロジンn=232、エンパグリフロジンn=142)やHFm/pEF患者(ダパグリフロジンn=158、エンパグリフロジンn=215)は、腎機能正常患者(ダパグリフロジンn=285、エンパグリフロジンn=302)やHFrEF患者(ダパグリフロジン359、エンパグリフロジンn=229)よりも少数でした。
CKD患者およびHFm/pEF患者では、重み付け後のデータでは両群間に明確な差は見られませんでした。
一方、腎機能正常患者およびHFrEF患者では、ダパグリフロジン群でアウトカムが不良である傾向が示されました(Table 5)。
Croat Med J. 2025 May 7;66(2):135-152.
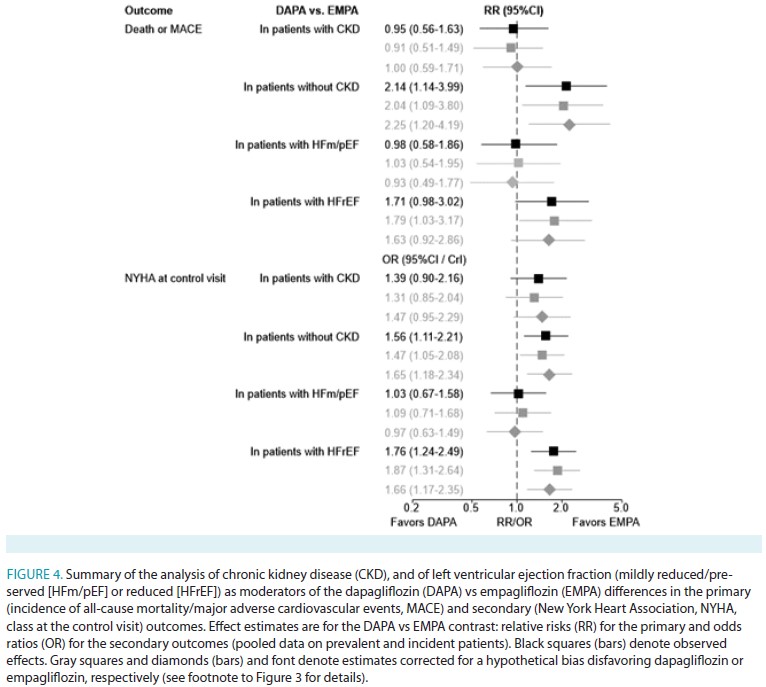
調整後解析(Figure 4)では、
:i)主要アウトカムは、CKD患者(RR=0.95、95%CI 0.56-1.63)およびHFm/pEF患者(RR=0.98、0.58-1.86)では2つの治療間で類似していましたが、腎機能正常患者(RR=2.14、1.14-3.99)およびHFrEF患者(RR=1.71、0.98-3.02)ではダパグリフロジンで著明に高くなりました
;ii)CKD患者(OR=1.39、0.90-2.16)および腎機能正常患者(1.56、1.11-2.21)の両方で、ダパグリフロジン処方患者はエンパグリフロジン処方患者よりもより悪いNYHA分類のオッズが高くなりました。
HFm/pEF患者では、治療間に差はありませんでした(OR=1.03、0.67-1.58)が、HFrEF患者では、より悪いNYHA分類のオッズはエンパグリフロジンよりもダパグリフロジンで高くなりました(OR=1.76、1.24-2.49)。
Croat Med J. 2025 May 7;66(2):135-152.
考察:
本解析は、ITT(Intention-to-Treat)解析に基づき、ダパグリフロジンを処方されたCHF患者が、エンパグリフロジンを処方された患者と比較して、治療開始後6か月間における全死亡/MACEの複合リスクが高く、NYHA分類も不良である可能性を示唆しました。
これらの結果は、既存患者と新規患者の両群で一貫していました。
探索的解析では、腎機能正常患者やHFrEF患者において、治療効果に差が見られる可能性が示唆されました。
これらの結果は我々の当初の期待とは異なったため、潜在的なバイアスを慎重に検討しました。
本研究は単一施設・限定サンプルという限界はあるものの、患者背景やアウトカム発生率が既存のピボタル試験や薬剤疫学研究 と概ね一致していること、アウトカム定義の妥当性 、イベント数の観点から、結果の方向性はある程度信頼できると考えています。
観察研究としての限界を考慮し、交絡因子の調整や感度解析を行いましたが、結果の方向性は変わりませんでした。
E値は、観察された差を覆すには非常に強い交絡が必要であることを示唆しています。
したがって、推定値の大きさには議論の余地があるものの、その方向性は有効であると考えられます。
この結果は、クレームデータを用いた最近の大規模研究で、エンパグリフロジンがダパグリフロジンよりも良好なアウトカムを示したという報告と一致しています 。
ピボタル試験では両薬剤の効果は類似していると報告されていますが、本研究や先行研究 のようなリアルワールドデータでは差が見られる可能性があり、これは体系的誤差だけでは説明が難しいかもしれません。
特に、腎機能が治療効果に与える影響については、さらなる検討が必要です。
SGLT2とSGLT1への選択性の違いなど、作用機序上の差異が臨床的な違いを生む可能性も考えられますが、現時点では明確ではありません。
ネットワークメタ解析では薬剤間の差異が示唆されており、本研究のような直接比較は、その可能性を検証する上で重要です。
本解析の結果から、ダパグリフロジンを処方された患者は、エンパグリフロジンを処方された患者と比較して、治療開始後6か月間における全死亡・主要心血管イベント(MACE)の発生率、および複合エンドポイント(主に心不全悪化)のリスクが高いことが示唆されました。
また、6か月後のNYHA分類も悪化する傾向が認められました(ITT解析)。
この結果は、新規診断群と既治療群の両サブセットで一致しており、統合解析の妥当性を裏付けています。
探索的解析では効果修飾の可能性が示されました。
腎機能正常患者(eGFR>60 mL/min/1.73 m²)およびHFrEF患者では治療薬間の差が明確でしたが、慢性腎臓病(CKD)患者やHFmrEF/HFpEF患者では差が認められませんでした。ただし、これらのサブグループの症例数は限定的でした。
予想に反する結果であったため、まず潜在的なバイアスの可能性を慎重に検討しました。
理論的には、単一施設での限られたサンプルサイズという制約から、偶然による結果の可能性も否定できません。
しかし、以下の点から本研究の外的妥当性は支持されると考えられます:
1) 本研究に含まれた患者の基本特性、併存疾患、治療内容(SGLT2阻害薬以外)は、ダパグリフロジンとエンパグリフロジンの主要臨床試験や最近の薬剤疫学研究で報告されたものと一致していました。
2) 主要アウトカムには、臨床試験で一般的に用いられる心血管死亡や心不全入院といった特定のエンドポイントではなく、全死亡とMACEを採用しました。
MACEの内訳は主に「心不全悪化イベント」でした。
実臨床では、原因特定が困難な疾患特異的死亡よりも全死亡の方が適切なアウトカムと考えられ、誤分類バイアスを受けにくく、臨床的意義も明確です。
したがって、本解析の主要アウトカムは無作為化試験と同等の特性を捉えており、定義によるバイアスの可能性は低いと考えられます。
3) 6か月間の全体的な粗発生率10.6%(102イベント/961患者)は、臨床試験におけるHFpEF、HFmrEF、HFrEF混合集団での期待値と合致していました。
4) 統合データにおける主要アウトカムの重み付け発生率(ダパグリフロジン12.5% vs エンパグリフロジン8.2%)は64対36イベントに相当し、多少のイベント数の変動では結果の方向性は変わらないと考えられます。
5) NYHA分類の結果も主要アウトカムと同じ傾向を示しました。
以上から、少なくとも全体集団においては、本データは妥当で堅牢なものと判断できます。
本解析は観察研究に固有の主要なバイアスから適切に保護されていたと考えます:
1) アウトカムや交絡因子の差別的誤分類は、すべての評価が客観的基準に基づき経験豊富な心臓専門医によってリアルタイムで行われ、本解析とは独立していたため可能性が低いです。
2) 患者選択基準は、比較的短い心不全既往歴(既治療患者)と、無作為化試験でも除外される併存疾患の不在のみでした。
NYHAアウトカムの定義とITT解析により、ベースライン後の選択バイアスのリスクは最小化されました。
3) すべての解析で、両群は広範な交絡因子について適切にバランスされていました。
それでも残存交絡の可能性は考慮しました。
これには、バランスされた交絡因子における小さな差の累積効果、SGLT2阻害薬以外の治療の投与量やコンプライアンスの差、その他の仮説的な交絡源が含まれます。
バイアス補正後の推定値は観察値とわずかに異なるのみで、依然としてダパグリフロジンでより悪いアウトカムを示しました。
E値解析では、点推定値を1.10まで減少させるには相当な効果を持つ交絡因子が必要であることが示されました。
推定値の大きさについては議論の余地があるものの、その方向性は妥当と考えられます。
この観察結果は、エンパグリフロジン処方患者で12か月間の心不全入院と全死亡のリスクが約10%低いことを示した最近の行政データ研究と一致しています。
方法論の違いから定量的比較は適切ではありませんが、両研究とも同じ方向性を示しています。
それぞれの主要プラセボ対照試験では、両SGLT2阻害薬はHFrEF患者とHFmrEF/HFpEF患者の両方で心不全入院/心血管死亡リスクの同程度の減少を示しました。
Modzelewskiらの薬剤疫学研究では、HFrEF患者、HFmrEF/HFpEF患者、および全体(66%がHFrEF)でエンパグリフロジンの優越性が示唆されました。
一般的に、質の高い無作為化試験と観察研究の結果の不一致は後者の系統的誤差で説明されますが、報告された観察データには明らかなバイアスは認められません。
本解析の全体集団およびHFrEF患者(全体の60%)においても同様と考えます。
HFmrEF/HFpEF患者で両薬剤間に差がないという所見は、無作為化試験の結果と一致しますが、症例数が非常に限られているため解釈は慎重にすべきです。
腎機能正常患者(全体の60%)では差が観察されたものの、CKD患者では観察されなかったことについても同様です。
主要試験では、両SGLT2阻害薬の利益はeGFR≤60 mL/min/1.73m²の患者と腎機能正常患者で同等でした。
エンパグリフロジンはダパグリフロジンよりもSGLT2に対する選択性が高く(SGLT1は心臓にも発現)、異なるグリフロジン間で臨床的に意味のある差が生じる可能性は興味深い仮説です。しかし、現時点でそのような顕著な特性は特定されていません。
異なる臨床状況(糖尿病、CKD、慢性心不全)での各グリフロジンの無作為化試験のネットワークメタ解析による間接比較は、心血管アウトカムが化合物間で異なる可能性を示唆しています。
本研究および既報の観察的直接比較は、慢性心不全における両薬剤の有効性が臨床的に意味のある程度まで異なる可能性を支持しており、今後の適切な評価が必要と考えられます。
結論:
本単一施設レジストリ分析では、ダパグリフロジンを処方された新規診断または既治療のCHF患者は、エンパグリフロジンを処方された患者よりも、治療開始後6か月間の全死亡/MACE複合リスクが高く、NYHA分類も不良である可能性が示されました。
本研究はサンプルサイズや追跡期間に限界があるものの、内的妥当性は比較的高く、報告された推定値は、請求データに基づく大規模な薬剤疫学研究で最近報告された慢性心不全治療におけるエンパグリフロジン対ダパグリフロジンの優越性と一致しています。
これらの知見は、CHF患者におけるエンパグリフロジンとダパグリフロジンの有効性を直接比較する無作為化比較試験の必要性を強く示唆するものです 。
