PubMed URL:https://pubmed.ncbi.nlm.nih.gov/39899304/
タイトル:Age and Sex Differences in Efficacy of Treatments for Type 2 Diabetes: A Network Meta-Analysis
<概要(意訳)>
序論:
最近の糖尿病治療薬の発展と背景
過去20年間で、新たな血糖降下薬は2型糖尿病の管理に大きな変革をもたらしました。SGLT2阻害薬(SGLT2i)やGLP-1受容体作動薬(GLP1ra)などの薬剤が心血管系および腎臓の転帰を改善する有効性は確立されており、臨床現場で広く使用され、臨床ガイドラインにも組み込まれています。
しかし、治療効果が患者の特性によって異なる可能性から、高齢者や女性など臨床試験での代表性が低い人々への試験結果の適用について疑問が生じています。
高齢糖尿病患者の実態と特有のリスク
世界的な推計によれば、65歳以上の5人に1人が糖尿病を抱えており、2型糖尿病患者のほぼ半数が65歳以上です。
さらに、加齢に関連する機能制限やフレイル(虚弱)などの状態は、2型糖尿病患者ではより早期に現れる傾向があります。
糖尿病合併症のリスクは年齢とともに増加し、治療による絶対的な利益が増大する可能性があります。
一方で、高齢者は強化血糖コントロールによる低血糖に対してより脆弱である可能性もあります。
性差による糖尿病の影響と管理の違い
女性における2型糖尿病と心血管疾患の絶対リスクは男性より低いものの、糖尿病は女性において男性よりも心血管リスクの相対的な増加が大きいという特徴があります。
また、女性患者は心血管合併症のパターンが異なり、心血管リスク因子の管理が男性患者よりも集中的でない傾向があります。
そのため、治療効果が年齢や性別によって異なるかどうかを判断することが重要です。
現在の臨床ガイドラインと研究の目的
現在の臨床ガイドラインでは、男性患者と女性患者、あるいは異なる年齢層に対して異なる糖尿病治療を推奨していません。
しかし、臨床試験における女性参加者や高齢者の過少代表による不確実性が強調されています。
私たちは、集約データと個別参加者試験データの両方の系統的レビューとメタ分析を実施し、SGLT2i、GLP1raおよびDPP4i治療の有効性が年齢と性別によって異なるかどうかを推定することを目的としました。
研究方法
系統的レビューとネットワークメタ分析の概要
本系統的レビューとネットワークメタ分析は、事前に指定されたプロトコル(PROSPERO:CRD42020184174)に従って実施されました。
このプロトコルは、ネットワークメタ分析を地域集団サンプルに較正する広範なプロジェクトの一部であり、代表的なサンプルを反映した有効性の推定値の提供を目指しています。本論文は、較正前の年齢および性別と治療の相互作用の評価結果を提示しています。
研究結果は、系統的レビューとメタ分析のための優先的報告項目(PRISMA)ガイドラインに従って報告されています。
適格性基準と検索戦略
適格と判断された研究は、18歳以上の2型糖尿病と診断された成人を登録し、SGLT2阻害薬(SGLT2i)、GLP-1受容体作動薬(GLP1ra)、またはDPP4阻害薬(DPP4i)の血糖(HbA1c)または主要心血管イベント(3P-MACE:心血管死、非致死的心筋梗塞または非致死的脳卒中と定義)に対する有効性を、プラセボまたは他の薬剤クラスの実薬対照と比較した無作為化試験でした。
同一クラス内の比較および登録されていない試験は除外しました。
優越性または非劣性を評価したかどうかに関わらず、試験は含めました。
クロスオーバーデザインの試験では、クロスオーバー前のデータのみを含めました。
キーワードとMedical Subject Headings(検索用語の詳細は補足資料に記載)を使用して、2つの電子データベース(MedlineとEmbase)および米国と中国の臨床試験登録機関を、開始から2022年11月まで検索しました。
すべてのタイトルと抄録をスクリーニングし、潜在的に適格と思われる研究をすべて全文レビュー用に保持しました。
スクリーニングのすべての段階は、2名のレビュアーが独立して実施し、不一致は合意によって解決し、必要に応じて第三のレビュアーを関与させました。
2024年8月に検索を更新し、初回検索日以降に発表された適格な登録試験の結果を含めました。
すべての適格試験について、Vivliリポジトリを通じて第三者研究者による分析のために個別参加者データが利用可能かどうかを評価し、独立運営委員会にアクセスを申請しました。
データ抽出方法
治療薬と患者基本情報の抽出
薬剤名、用量、投与レジメンは、clinicaltrials.govおよび公開文書(論文や臨床研究報告書)から得られたテキスト文字列から抽出しました。
ベースライン時の年齢と性別は、集約データ試験では公開文書から、または個別参加者データから取得しました。
HbA1c結果はclinicaltrials.govまたは公開文書から抽出しました。
個別参加者データのある試験では、ベースライン時および主要評価項目の時点でのHbA1c値を抽出しました。
評価項目の値が欠損している場合は、最後に利用可能な観測値を使用しました。
感度分析として、ベースライン観測値を使用する分析も行いました。
MACEデータの抽出と定義の標準化
主要心血管イベント(MACE)の結果は、公開文書(年齢別・性別サブグループを含む)から手動で抽出しました。
3P-MACEは心血管死、非致死的心筋梗塞、または非致死的脳卒中と定義されました。
個別参加者データのある試験では、この定義は判定されたイベントを使用して試験間で統一されました。
集約データについては、研究間の一貫した比較を可能にするために3P-MACEの結果が抽出されました。
個別レベルの試験データはVivliリポジトリでクリーニングおよび統一化されました。
有害事象データの抽出
有害事象に関するデータも個別参加者データから抽出され、重篤な有害事象および各薬剤クラスとの確立された関連性のあるイベントに焦点を当てました。
各試験について、発生した重篤な有害事象、消化器系有害事象、尿路感染症、低血糖エピソード、切断、およびケトアシドーシスが特定されました。
標準化された定義がないため、集約試験では有害事象は評価されませんでした。
各研究のバイアスリスクはコクランのバイアスリスク評価ツールを用いて評価されました。
統計解析方法
基本的な解析アプローチ
統計解析の詳細については、電子付録(Supplement)のeMethodsに記載されています。
まず、各試験の年齢および性別分布について、可能な場合は個別参加者データ(IPD)を用いて、それ以外は公表された要約統計量から要約しました。
次に、以前に記述したように、Rのmultinmaパッケージを使用してHbA1cとMACE(主要心血管イベント)に対するマルチレベルネットワークメタ回帰モデルを適合させました。このモデリングアプローチは、無作為化を乱さず、標準的なネットワークメタ分析よりも厳格でない仮定を採用し、(集計バイアスを引き起こすことなく)個別参加者データ、集計レベルの試験データ、サブグループレベルの試験データを、治療と共変量の相互作用を推定するモデルに組み込むことができるために選択されました。
HbA1cとMACEの分析モデル
HbA1cのネットワークメタ分析では、対象薬剤の異なる適応を反映して、単剤療法、二剤併用療法、三剤併用療法の試験ごとに個別にモデルを適合させました。
MACE試験はすべて、参加者が心血管リスクに基づいて選択されていたため、一緒に分析されました。
2つ以上の治療の併用効果を評価する治療群は除外されました。
SGLT2i、GLP1ra、DPP4i、およびメトホルミンについては、治療群は薬剤と用量によって分類されました。
インスリンは単一カテゴリとしてモデル化されました。
残りの薬剤クラスについては、同じ試験内で用量は異なるが同じ薬剤の群は、単一の群に統合されました。すべてのモデルで、プラセボを対照治療としました。
交互作用の評価方法
個別参加者データのある試験については、年齢、性別、治療による各アウトカムの試験レベル回帰モデルを適合させ、年齢と治療および性別と治療の相互作用を評価しました。
HbA1cについては、ベースラインのHbA1cを共変量として含む線形回帰モデルを適合させました。
試験を完了しなかった参加者については、最後に記録された値を使用しました。
MACE転帰にはCox回帰モデルを適合させました。
MACE転帰の分析では、非心血管死を競合イベントとして扱い、原因特異的ハザード比を提示しました。
また、非心血管死亡率(最初のMACE発生前に死亡が発生した場合と定義)についても、競合イベントの原因特異的ハザード比を推定しました。
モデルの検証と結果の解釈
Coxモデルでは比例ハザード仮定をスケール化されたSchofield残差をプロットすることでチェックしました。
HbA1cおよびMACE転帰の非線形性については、残差プロットと年齢の制限付き三次スプラインを検査しました。
個別参加者データの推定値は、試験転帰および各試験の年齢・性別分布に関する集計試験レベルデータと(MACEについては)サブグループレベルデータとともにメタ分析されました。
有害事象データについては、個別参加者データ内の発生イベントに準ポアソンおよび負の二項回帰モデルを適合させ、結果をメタ分析しました。
プラセボを対照カテゴリとして使用しました。
モデルは、主効果および年齢-治療と性別-治療の相互作用について、事後平均と95%信頼区間を用いて要約されました。
95%信頼区間は値の妥当な範囲を示します。
したがって、95%信頼区間がnull(HbA1c比較ではゼロ、MACE比較では1)を含む場合、「効果なし」または「交互作用なし」が妥当な解釈の一つとなります。
転帰間の比較を可能にするために、HbA1cとMACEの両方について個別レベルまたは集計データを持つ14の試験にデータを制限して主要分析を繰り返しました。
いずれの分析も、多重検定のための正式な調整を行いませんでした。
個別参加者データの要約および集計レベルのデータは、プロジェクトのGitHubリポジトリで入手可能です。
研究結果
系統的レビュー結果
適格な687試験を特定し、そのうち601試験をネットワークメタ分析に含めました(図1)。これらのうち、592試験がHbA1cアウトカムを報告し、23試験がMACE(主要心血管イベント)アウトカムを報告し、14試験が両方を報告していました。
集計レベルの498試験には303,311人の参加者が含まれ、個別参加者データのある103試験には92,182人の参加者が含まれていました。
試験レベルの詳細とバイアスリスクはオンラインプロジェクトリポジトリに示されています。
表1は、各薬剤クラスについてHbA1cを報告している含まれた試験の総数と集計ベースライン特性を示しています。
個別参加者データのある試験と集計データのある試験の特性は類似していました。
MACEを報告する試験については、試験レベルの詳細が表2に示されています。
女性参加者よりも男性参加者の方が多く、高齢者を対象とした試験を含め、ほぼすべての試験参加者の年齢範囲は40~80歳でした(eFigure1、eTable1、補足資料)。
主要な治療効果
各治療とプラセボを比較したHbA1cに対する主要な治療効果は、共変量のない標準的なネットワークメタ分析にてeFigure 2に示されています。
治療によるHbA1cの絶対的減少範囲は-0.5%から-1.5%でした。
MACEに対する主要な治療効果は、プラセボと比較してSGLT2iとGLP1raでMACEのハザードが減少し、DPP4iでは有意な結果が見られませんでした(eFigure3)。
年齢-治療および性別-治療の交互作用
図2は、年齢-治療および性別-治療の相互作用を示し、HbA1cとMACEに対する治療の有効性の年齢および性別による違いを評価しています。
補足:
図2で言及されている「固定効果」と「変量効果」は、ネットワークメタ分析における統計モデルの構築方法に関連しています。
固定効果(Fixed Effects)
- 意味: 固定効果モデルでは、すべての試験における真の治療効果は同一であると仮定しています。つまり、異なる試験間で観察される治療効果の違いは、サンプリング誤差(偶然)のみによるものと考えます。
- 具体例: 例えば図2では、同じ薬剤(カナグリフロジン300mg)についての治療効果が、すべての研究で基本的に同じであると仮定したモデル推定値が固定効果として示されています。
- グラフでの表示: 図2では固定効果が赤色の点で表示されています。
変量効果(Random Effects)
- 意味: 変量効果モデルでは、真の治療効果が研究間で変動する可能性を考慮します。つまり、各試験には独自の真の効果があり、これらの効果は共通の分布から抽出されると考えます。
- 具体例: 同じカナグリフロジン300mgでも、異なる研究間で患者集団、診療環境、併用薬などが異なるため、治療効果に真の違いがあると仮定したモデル推定値です。
- グラフでの表示: 図2では変量効果が青色の点で表示されています。
実際のデータでの意味
- 図2では、薬剤クラス内での治療効果を推定する際、固定効果と変量効果の両方のモデルが使用されています。
- 固定効果と変量効果の推定値が近い場合、研究間の異質性(ばらつき)が少ないことを示唆します。
- 両者の推定値が大きく異なる場合、研究間の異質性が大きいことを示唆し、変量効果モデルの方がより適切かもしれません。
このように、図2では各薬剤クラスについて、年齢や性別による効果の変化を、異なる統計モデルのアプローチで評価した結果を比較して示しています。
これにより、結果の頑健性(robustness)や一貫性を確認できます。
SGLT2阻害薬は年齢の増加とともに絶対的なHbA1c低下効果が減少しました(30歳高齢化するごとに、単剤療法で0.24%、95%信頼区間0.10-0.38、二剤併用療法で0.17%、95%信頼区間0.10-0.24、三剤併用療法で0.25%、95%信頼区間0.20-0.30のHbA1c低下効果の減少)。
年齢-治療相互作用の非線形性の証拠はありませんでした(eFigure 4)。
追跡期間が6ヶ月以上の試験に分析を限定した場合も結果は同様でした(eFigure5)。
GLP1受容体作動薬は、単剤療法および二剤併用療法において、年齢の増加とともにHbA1c低下に対するより大きな絶対的効果を示しました(30歳増加ごとにそれぞれ-0.18%、95%信頼区間-0.31~-0.05および-0.24%、95%信頼区間-0.40~-0.07のHbA1c低下)が、三剤併用療法では示しませんでした(30歳増加ごとに0.04%、95%信頼区間-0.02~0.11)。
DPP-4阻害薬は、高齢者の二剤併用療法においてわずかに良好な絶対的HbA1c低下効果を示しましたが(30歳増加ごとに-0.09%、95%信頼区間-0.15~-0.03のHbA1c低下)、単剤療法または三剤併用療法での有効性変動の証拠はありませんでした(それぞれ30歳増加ごとに-0.08%、95%信頼区間-0.18~0.01および-0.01%、95%信頼区間-0.06~0.05のHbA1c低下)。
三剤併用療法のみでSGLT2阻害薬の有効性に男性有利の小さな差異(-0.06%、95%信頼区間-0.18~0.06)があったことを除き、性別による有効性の変動はありませんでした。
年齢・性別による心血管イベントへの治療効果の差異
年齢による心血管イベント(MACE)への影響
高齢者ではSGLT2阻害薬によるMACEの相対的リスク減少がより大きく(30歳年齢増加ごとにHR 0.76、95%信頼区間0.62-0.93)、GLP1受容体作動薬によるMACEの相対的リスク減少は小さくなりました(30歳年齢増加ごとにHR 1.47、95%信頼区間1.07-2.02)。DPP-4阻害薬の信頼区間はnull値を含んでいました(HR 0.73、95%信頼区間0.52-1.00)。
MACE試験における性別-治療相互作用をモデル化すると、DPP-4阻害薬は男性参加者でより効果が低いことが示されました(男性対女性でHR 1.65、95%信頼区間1.25-2.21)。
ただし、この関連性は分析に性別サブグループデータを含めた後(HR 1.22、95%信頼区間1.04-1.42)、および個別参加者データを持つ唯一のDPP-4阻害薬試験を除外した後には弱まり、信頼区間はnull値を含みました(eFigure 6)。
GLP1受容体作動薬(男性対女性でHR 1.17、95%信頼区間0.87-1.58)およびSGLT2阻害薬(男性対女性でHR 0.95、95%信頼区間0.86-1.06)については、性別-治療相互作用の証拠はありませんでした。
追加モデルでは、試験に含まれる年齢範囲内での年齢-治療相互作用の非線形性は示されませんでした(eFigure7)。

JAMA. 2025 Feb 3:e2427402.
感度分析の結果
モデルに年齢および性別サブグループデータを含めるか除外するかの感度分析は、個別参加者データを持つ4つのSGLT2阻害薬試験のうち1つを除外した分析を除いて、SGLT2阻害薬を服用している高齢者のHbA1c結果に影響を与えませんでした(eFigure6)。
高齢者でのMACEリスクのより大きな相対的減少はすべての感度分析で維持または増大しました。
HbA1cとMACEの両方について個別レベルデータを持つ14の試験にデータを制限した分析でも同様の結果が得られました(eFigure8)。
MACEの分析結果は、個別参加者データを持つGLP1受容体作動薬およびDPP-4阻害薬の単一試験の包含または除外、およびサブグループデータの包含または除外によって異なりました(eFigure6)。
有害事象との交互作用
いかなる薬剤クラスと消化器系有害事象、低血糖、または尿路感染症との間にも年齢または性別による治療交互作用はありませんでした(eFigure9)。
SGLT2阻害薬、GLP1受容体作動薬、またはDPP4阻害薬での重篤な有害事象にも年齢または性別による治療交互作用はありませんでした(eFigure9)。
死亡は試験全体で稀でした(eFigure10)、また非心血管死亡に対する年齢-治療または性別-治療相互作用の証拠はありませんでした(eFigure11)。
切断またはケトアシドーシスのモデルを適合させるには、個別参加者試験データ内のイベント数が少なすぎました(eTable2)。
MACE試験における年齢別・性別特異的効果
SGLT2阻害薬の効果
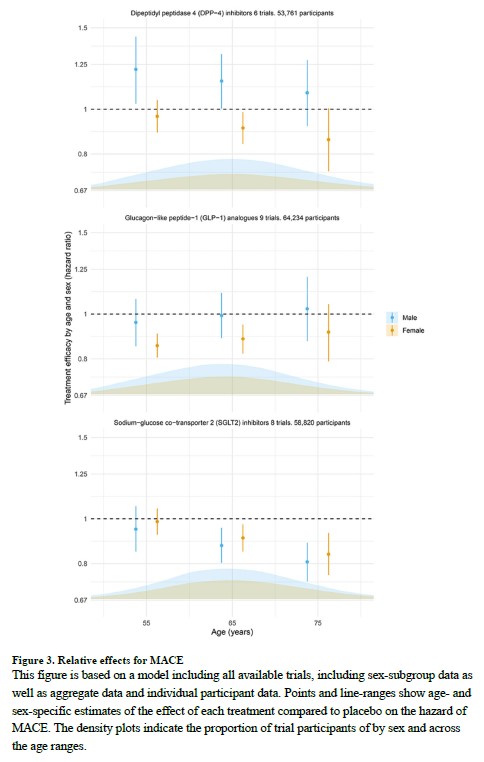
図3は、年齢-治療および性別-治療の相互作用と、各クラスのプラセボと比較した全体的な年齢別・性別特異的相対的有効性との関連を示しています。
SGLT2阻害薬は性別に関わらず高齢者でMACEの減少と関連していました(75歳女性でHR 0.84、95%信頼区間0.76-0.93;75歳男性でHR 0.81、95%信頼区間0.73-0.89;65歳女性でHR 0.91、95%信頼区間0.85-0.97;65歳男性でHR 0.88、95%信頼区間0.80-0.96)。
GLP1受容体作動薬の効果
GLP1受容体作動薬については、男性参加者(例えば65歳男性でHR 0.99、95%信頼区間0.89-1.11)および高齢者(75歳女性でHR 0.91、95%信頼区間0.79-1.05;75歳男性でHR 1.03、95%信頼区間0.87-1.20)ではMACEの有意な減少との関連はありませんでした。
しかし、若年女性参加者では(55歳女性でHR 0.85、95%信頼区間0.81-0.91;65歳女性でHR 0.88、95%信頼区間0.82-0.95)MACEリスクの減少が見られました。
結果の解釈に関する注意点
これらの知見は慎重に解釈する必要があります。
GLP1受容体作動薬クラスは全体としてMACEに対する有益性を示しましたが(eFigure 3)、このクラス内の一部の薬剤については、MACEへの効果がnullでした(eFigure 12)。同様に、DPP4阻害薬の年齢および性別による有効性の差異もありましたが、これらの薬剤はMACEに対する全体的な効果がnullであったため、慎重に解釈すべきです。
すべての相互作用の推定値は、特定の試験の包含に敏感でした。
補足資料のeTable2は、すべてのランダム効果モデルの異質性推定値を提供しています。
JAMA. 2025 Feb 3:e2427402.
考察
主要な研究結果の要約
本ネットワークメタ分析は、103試験からの個別参加者データ(IPD)を含む601試験を対象に、2型糖尿病患者における3つの新しい薬剤クラス(SGLT2阻害薬、GLP1受容体作動薬、DPP4阻害薬)の有効性が年齢や性別によって異なるかどうかを評価しました。
HbA1cに関しては、SGLT2阻害薬は年齢の増加とともに効果がわずかに低下し、45歳と比較して75歳では、プラセボと比較した治療効果が約0.25%減弱しました。
対照的に、SGLT2阻害薬によるMACE(主要心血管イベント)の減少は、若年者と比較して高齢者でより大きいことが示されました。
GLP1受容体作動薬については、高齢者でのHbA1c低下効果がより大きく、一方で心血管有効性は若年女性参加者でより高いというエビデンスが一部ありました。
先行研究との比較
年齢や性別による2型糖尿病治療の有効性の異質性(交互作用)を評価した先行研究は、一般に無作為化対照試験の集計データやサブグループデータを使用するか、または観察研究(非無作為化)データに依存していました。
SGLT2阻害薬とGLP1受容体作動薬の有効性における男女間の差異に関するメタ分析では、心血管アウトカムに対する有効性に統計的に有意な差は見られませんでしたが、女性患者群の推定値における統計的不確実性が大きいため、女性患者間での心血管有効性の低下の可能性が推測されていました。
私たちの分析は、より大規模かつ包括的な研究群を含み、個別参加者データを取り入れることで、より高い精度を提供し、性別がこれらの薬剤クラスの有効性の差異と関連していないことをより明確に示しました。
関連する最近のメタ分析との関係
最近のネットワークメタ分析は、心不全、末期腎疾患、および本分析に含まれていない薬剤関連有害事象を含む、さまざまな臨床アウトカムにわたる2型糖尿病治療の有効性を評価しました。
この最近のネットワークメタ分析では、MACEに加えて、SGLT2阻害薬とGLP1受容体作動薬が心不全による入院リスクと末期腎疾患のリスクを低減し、末期腎疾患の低減においてはSGLT2阻害薬の方が優れた有効性を示すことが明らかになりました。
治療による有害事象は一般的にクラス特異的であり、SGLT2阻害薬での性器感染症やGLP1受容体作動薬での消化器系合併症などが含まれていました。
しかし、この先行分析では年齢や性別による異質性を評価しておらず、IPDの分析も含まれていませんでした。
年齢によるSGLT2阻害薬の効果差異:腎機能の影響と臨床的示唆
年齢と腎機能低下による血糖降下効果への影響
SGLT2阻害薬の血糖降下効果が高齢者で減弱する理由として、最も考えられるのは年齢関連の腎機能低下です。
例えば、最近のDPP4阻害薬とSGLT2阻害薬を比較した二重盲検3群クロスオーバー研究では、推定糸球体濾過量が60~90 ml/min/1.73m²の参加者は、90 ml/min/1.73m²超の参加者と比較して、SGLT2阻害薬服用時よりもDPP4阻害薬服用時の方が低いHbA1cを示しました。
この文脈において、血糖降下効果が低いにもかかわらず、高齢者ではSGLT2阻害薬によるMACE(主要心血管イベント)の減少がより大きかったことは注目に値します。
HbA1c以外の心血管リスク因子の重要性
この結果は、MACEのリスク決定における代替指標(HbA1cなど)の限界を浮き彫りにしています。
MACEにおいては、高血糖よりも高血圧や脂質異常症がより重要なリスク因子となります。また、この知見は、高血糖を特徴としない心不全や慢性腎臓病などの糖尿病以外の疾患における心血管転帰の改善にもSGLT2阻害薬が有効であることと一致しています。
高齢患者治療への臨床的示唆
現在の臨床ガイドラインでは、複数の長期的疾患やフレイル(虚弱)を持つ高齢者に対して、有害事象のリスクが高いため、より緩やかな血糖コントロール目標を推奨しています。
今回の結果は、高齢者を治療する際に、安全性、忍容性、患者の優先事項に加えて、治療の心臓保護効果を考慮する必要性を強調しています。
本研究の結果は、対象試験に含まれる高齢者間で同等またはより良好な心血管有効性を示していますが、臨床試験では80歳以上の人々はほとんど登録されていません。
また、試験参加者と日常診療で治療を検討される人々の間には測定されていない差異が存在する可能性が高いです。
例えば、心血管イベントと合併症の両方のリスクを増加させるフレイルなどの年齢関連状態は、これらの試験では定量化されていません。
したがって、本分析では、かなり高齢(80歳以上)またはフレイルを有する人々での有効性が同様であるかどうかは評価されていません。
これは、リスクとベネフィットのバランスが最も不確実なグループです。
将来の研究への提言
さらに、治療効果に対する年齢の影響は、腎機能や併存疾患の有無と程度などの他の測定可能な年齢関連特性を通じて調整されている可能性が高いです。
将来の研究でこのような特性を考慮することで、より特定の特性に応じた治療のベネフィットについてより細かな理解が可能になるかもしれません。
これにより、高齢者全体での治療効果だけでなく、異なる生理学的・臨床的特性を持つ高齢者における効果も特定できるでしょう。
高齢者やフレイルを持つ人々を募集・維持し、機能状態を明示的に測定・報告する臨床試験が必要です。
研究の限界点と結論
研究限界
データの可用性と代表性
- 本分析の主な強みは個別参加者データ(IPD)を使用して年齢・性別と治療の相互作用を推定したことですが、すべての対象試験でこれが利用可能ではありませんでした(601試験中103試験、17%のみ)。
- IPDの利用可能性は治験スポンサーのデータ共有体制に依存していたため、含まれたIPDは無作為サンプルではありません。
- 研究者らは直接的な研究著者への接触による追加IPDの入手は試みませんでした。
方法論的制約
- マルチレベルネットワークメタ回帰の使用により、個別レベルデータの有無に関わらず、すべての治療比較(クラス内、クラス間、プラセボとの比較)を交互作用の推定に使用できました。
- クラス内の薬剤効果は独立して推定されましたが、相互作用推定においては同一クラス内の薬剤間で相互作用が共通であると仮定しており、実際には各クラスで少なくとも一部の個別レベルデータを持つ試験が必要です。
アウトカムと分析の範囲
- 多数の試験を含めましたが、心血管アウトカムを評価した試験の割合は比較的小さいものでした。
- 複数の薬剤クラスを持つ試験群は、ソフトウェアが群内の成分の明示的モデル化を許可しないため除外し、クラスレベルの相互作用に焦点を当てました。
- 臨床的に関連性の高い血糖および心血管有効性を評価しましたが、他の臨床エンドポイント(腎臓イベントなど)は含まれていません。
有害事象と絶対リスクの評価
- これらの薬剤と確立されたリスクとの関連が年齢や性別によって異なるかどうかを評価しましたが、試験データ内のイベント数が少ないために分析は制限されました。
- より希少なイベントの特定がより容易な日常的医療データの活用が理想的である特定の有害事象との新規関連の特定は試みませんでした。
- MACEを絶対リスクの観点から提示しませんでした。
多くの状況では、年齢とともにMACEのリスクが高まる可能性が高く、これは治療の絶対的利益を増加させる傾向がありますが、競合リスク(非心血管死亡など)も年齢とともに高まる可能性があります。
したがって、高齢者における治療の絶対的利益は、相対的治療効果だけでなく、標的集団におけるMACEと競合イベントの発生率にも依存します。
結論
SGLT2阻害薬、GLP1受容体作動薬、およびDPP4阻害薬は、年齢および性別グループ全体でHbA1c低下と関連していました。
SGLT2阻害薬とGLP-1受容体作動薬は、MACEのリスク低下と関連していましたが、その中でもSGLT2阻害薬はHbA1c低下効果が小さいにもかかわらず若年者よりも高齢者でより心臓保護的である一方、GLP-1受容体作動薬は若年者でより心臓保護的であることが示唆されました。
