PubMed URL:https://pubmed.ncbi.nlm.nih.gov/37466813/
タイトル:eGFR slope as a surrogate endpoint for clinical study in early stage of chronic kidney disease: from The Japan Chronic Kidney Disease Database
<概要(意訳)>
序論:
慢性腎臓病(CKD)は世界的な問題であり、患者数の増加と医療経済への影響が深刻化しています。
CKD患者は死亡、心血管疾患(CVD)、末期腎不全(ESKD)のリスクが高いことが知られています。
臨床研究では「死亡」、「心血管疾患」、「末期腎不全」などの「ハードエンドポイント」が確立されていますが、これらの真のエンドポイントは以下の問題があります:
- 発生頻度が低い
- 大規模なサンプルサイズが必要
- 長期の観察期間が必要
このため、研究コストが高くなり実現可能性が低下するので、腎臓病の臨床試験実施の障壁となっています。
そこで、腎臓の重要なアウトカムを予測する「代替エンドポイント」の研究が進められてきました。
進行したCKD(CKDステージG3b-G5)では、2017年にKDIGO(国際腎臓病予後改善機構)によって、「eGFRの30~40%低下」または「血清クレアチニン値の倍加」がESKDの代替エンドポイントとして確立されました。
これらの代替エンドポイントは日本人集団でも検証され、慢性腎臓病の臨床評価ガイドラインとして発表されています。
2018年には、米国腎臓財団(NKF)、米国食品医薬品局(FDA)、欧州医薬品庁(EMA)が共催した科学ワークショップで、早期CKDにおける代替エンドポイントが推奨されました。
この推奨では、「eGFR勾配の変化」が代替エンドポイントとして評価され、「eGFR勾配の減少が0.5~1.0 mL/分/1.73 m²/年」がESKDリスク減少を予測するカットオフ値とされています。
しかし、日本と他国との間で透析導入時のeGFRに無視できない差があることを考慮すると、同じ値が日本人患者にも適用できるかどうかを確認する必要があります。
本研究の目的は、NKF-FDA-EMAワークショップで推奨された代替エンドポイントが日本のCKD患者にも同様に適用できるかどうか、その外部妥当性を検証することです。
日本のCKD患者のリアルワールドデータセットであるJ-CKD-Database(J-CKD-DB)を用いて、eGFR勾配の変化とESKDとの関連を調査しました。
方法:
本研究のデータ出典はJ-CKD-DBデータベースで、これは国内大学病院のCKD患者の実世界データを収集するために設計されました。
要約すると、このデータベースはSS-MIX2標準ストレージを使用して、電子カルテからCKD症例のデータを自動的に抽出しています。
J-CKD-DBにCKD患者を登録する基準は次のとおりです:
- 年齢18歳以上
- 研究期間中に、尿タンパク≥1+(試験紙法)および/またはeGFR < 60 mL/分/1.73 m²
本研究では、複数年にわたる縦断的データを含むJ-CKD-DBの発展版であるJ-CKD-DB-Exを使用しました。
2014年から2018年の間にデータベースに登録されたすべての患者から、以下の除外基準に該当する参加者を除外しました:
- ベースライン測定を含む2回未満のeGFR測定値しかない参加者(eGFR勾配計算に必要)
- 1〜3年のeGFR勾配計算期間後にデータがない参加者
- 共変量データが欠損している参加者(共変量データの欠損がある場合は分析から除外)
- 透析開始または死亡に関するデータがない参加者
- ベースラインeGFRが30 mL/分/1.73m²未満の参加者
この研究は早期CKDの代替エンドポイントを確立することを目的としているため、eGFR < 30 mL/分/1.73m²の参加者は進行したCKDとして除外されました。
さらに、探索的分析として、より進行した腎不全(eGFRが20~30 mL/分/1.73 m²の範囲)の集団でも分析を行いました。
<アウトカムの定義と観察期間>
本研究のアウトカム(結果指標)は「末期腎不全(ESKD)」と定義されました。
- 主要分析:ESKDは「透析開始」と定義
- 副次分析:ESKDは「CKDステージG5の発生」(eGFR < 15 mL/分/1.73 m²)と定義
観察期間は、eGFR勾配計算後からアウトカム発生または最終eGFR測定までの期間と定義されました(図1参照)。
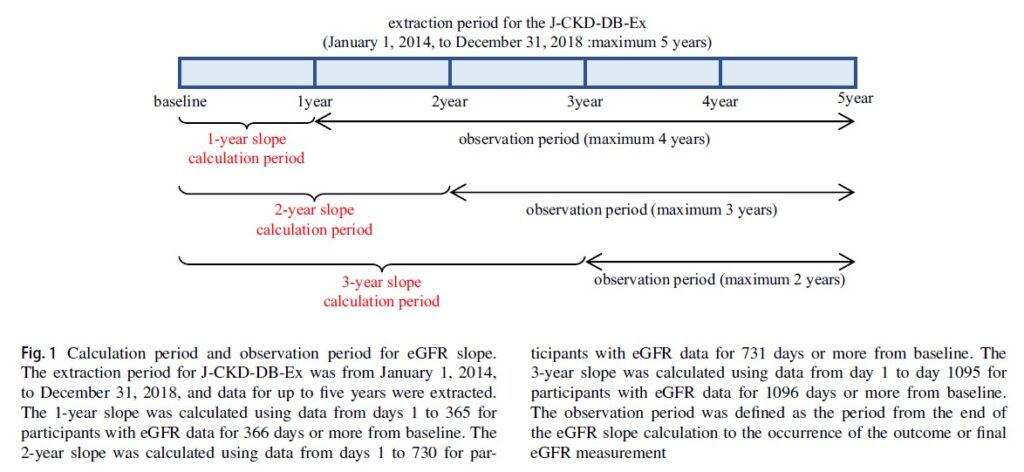
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
<eGFR勾配の計算方法>
- eGFR値は血清クレアチニン値に基づく日本人GFR推算式を用いて計算
- 各症例の最も古いeGFR測定ポイントをベースラインとして使用
- 計算期間中にベースラインを含む2回以上のeGFR測定を受けた参加者については、計算期間内のすべてのeGFR値を使用してeGFR勾配を計算
<勾配計算の手法>
- 最小二乗法:eGFR値とモデルの間の残差二乗和を最小化する線形近似モデルの傾きをeGFR勾配として使用
- 混合効果モデル:ランダム切片および傾きを持つ線形混合効果モデルを使用して各個人の勾配を推定
<勾配の種類>
ベースライン後の1年、2年、3年のeGFR値を使用して3種類のeGFR勾配を計算し、説明変数として使用しました。平均値±3SDの範囲から逸脱した参加者は分析から除外されました。
<統計分析>
基本情報の表示
- 連続変数:平均値±標準偏差または中央値(四分位範囲)で表示
- 二値変数:数値とパーセンテージで表示
多変量解析
死亡イベントと競合する透析開始およびCKDステージG5の発生の両方について、Fine-Grayの比例ハザード回帰モデルを用いて多変量解析を実施。
eGFR勾配の各変化に対するアウトカム発生のハザードリスクを推定しました。
サブグループ分析
以下のサブグループについて分析を実施:
- ベースラインeGFR ≥ 45 mL/分/1.73 m²(CKDステージG1-G3a)
- ベースラインeGFR ≥ 60 mL/分/1.73 m²(CKDステージG1-G2)
- ベースラインeGFRが20~30 mL/分/1.73 m²の範囲
結果:
<研究対象者の選定>
一部の参加施設では死亡と透析開始の真のエンドポイントを収集できなかったため、これらの施設からの参加者は除外されました。
そのため、データベースに152,815人が登録されていましたが、本研究に含まれた人数は31,616人でした。
そのうち、以下の理由で参加者が除外されました:
- eGFR勾配計算に必要な複数回のeGFR測定がない参加者
- 1年勾配:18,713人
- 2年勾配:19,972人
- 3年勾配:22,293人
- 共変量データが欠損している参加者
- ヘモグロビン:1,575人
- 血清アルブミン:2,356人
- 血清CRP:6,930人
- ベースラインeGFRが30 ml/分/1.73 m²未満の参加者:2,793人
<分析対象者の特性>
1~3年のeGFR勾配を計算するために分析された参加者数は、それぞれ7,768人、6,778人、5,219人でした。表1は参加者の背景情報を示しています。
平均観察期間は以下の通りでした:
- 1年勾配:877±491日
- 2年勾配:706±346日
- 3年勾配:495±215日
観察期間中の死亡者数は以下の通りでした:
- 1年勾配:827人(10.7%)
- 2年勾配:533人(7.9%)
- 3年勾配:317人(6.1%)
透析開始の発生率は非常に低く、以下の通りでした:
- 1年勾配:28人(0.4%)
- 2年勾配:24人(0.4%)
- 3年勾配:14人(0.3%)
CKDステージG5の発生率は以下の通りでした:
- 1年勾配:186人(2.4%)
- 2年勾配:129人(1.9%)
- 3年勾配:71人(1.4%)
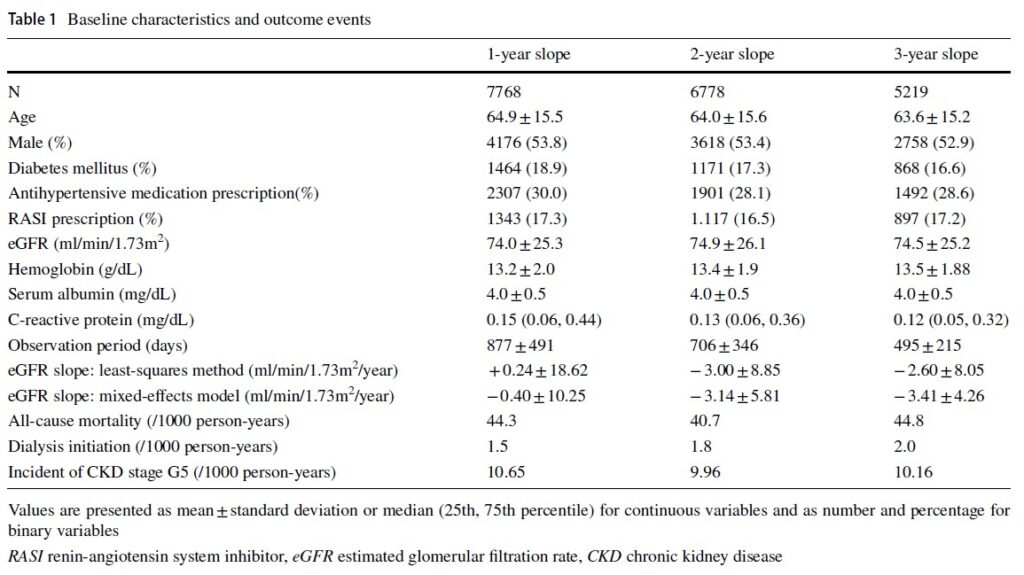
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
<サブグループの特性>
ベースラインeGFRが60 ml/分/1.73 m²以上(CKDステージG1-G2)の参加者に限定した場合、透析開始の発生率はそれぞれ6人(0.1%)、6人(0.1%)、4人(0.1%)でした。
ベースラインeGFRが45 ml/分/1.73 m²以上(CKDステージ1-3a)の参加者に限定した場合も、透析開始の発生率は低く、それぞれ11人(0.2%)、11人(0.2%)、8人(0.2%)でした。
そのため、CKDステージに基づく透析開始のサブグループ分析を実施することは不可能でした。
しかし、CKDステージG5の発生を判定するためにCKDステージに応じたサブグループ分析が実施されました。
<eGFR勾配とESKDリスクの関係>
eGFR勾配の分布特性
図2はeGFR勾配の分布を示しています。
混合効果モデルと最小二乗法の両方において、1年勾配は2年および3年勾配よりも変動範囲が大きいことが確認されました。
さらに、混合効果モデルで推定されたeGFR勾配と比較して、最小二乗法で推定されたeGFR勾配は変動範囲が大きい傾向がありました。
<eGFR勾配とESKDのリスク関係>
eGFR勾配とESKDの部分分布ハザード比(SHR)の関係を調査しました。
1~3年の各計算期間について、eGFR勾配の変化の大きさに応じて、透析開始としてのESKD(図3A)およびCKDステージG5の発生としてのESKD(図3B)の調整済みSHRをプロットしました。
透析開始としてのESKD定義時
eGFR勾配が+0.5から+1.0 ml/分/1.73 m²/年と緩やかに減少した場合の調整済みSHRは以下の通りでした:
最小二乗法による推定:
- 1年勾配:0.986~0.972
- 2年勾配:0.951~0.905
- 3年勾配:0.970~0.941
混合効果モデルによる推定:
- 1年勾配:0.979~0.959
- 2年勾配:0.931~0.867
- 3年勾配:0.872~0.760
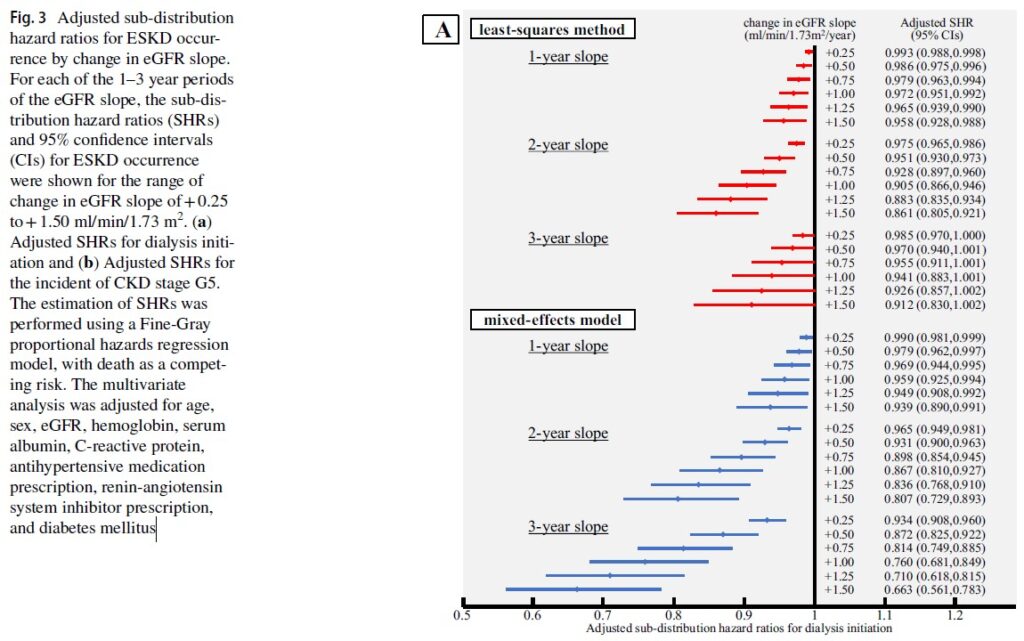
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
<CKDステージG5の発生としてのESKD定義時>
eGFR勾配が+0.5から+1.0 ml/分/1.73 m²/年と緩やかに減少した場合の調整済みSHRは以下の通りでした:
最小二乗法による推定:
- 1年勾配:0.990~0.981
- 2年勾配:0.963~0.927
- 3年勾配:0.958~0.917
混合効果モデルによる推定:
- 1年勾配:0.985~0.971
- 2年勾配:0.950~0.902
- 3年勾配:0.896~0.802
<主な観察結果>
- 混合効果モデルで推定されたeGFR勾配ではSHRの減少が観察され、eGFR勾配の計算期間が長くなるにつれてSHRがさらに減少する傾向が見られました。
- 同様に、最小二乗法で推定されたeGFR勾配も、1年と比較して2~3年の計算期間でSHRの減少が大きくなりました。
- 透析開始としてのESKDのSHRに関しては、2年勾配は3年勾配よりもわずかに大きな減少を示し、これは混合効果モデルを使用して得られた結果とは異なっていました。
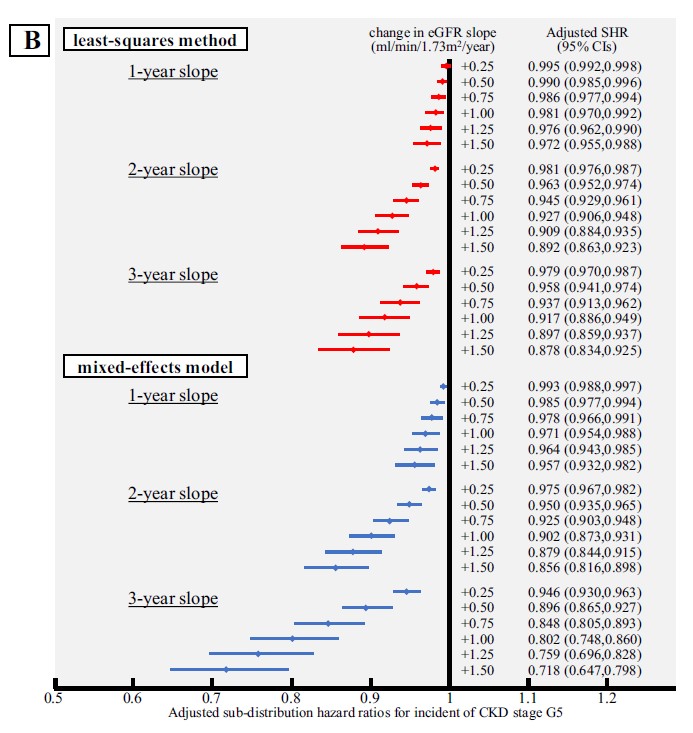
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
<サブグループ分析結果>
CKDステージ別の分析
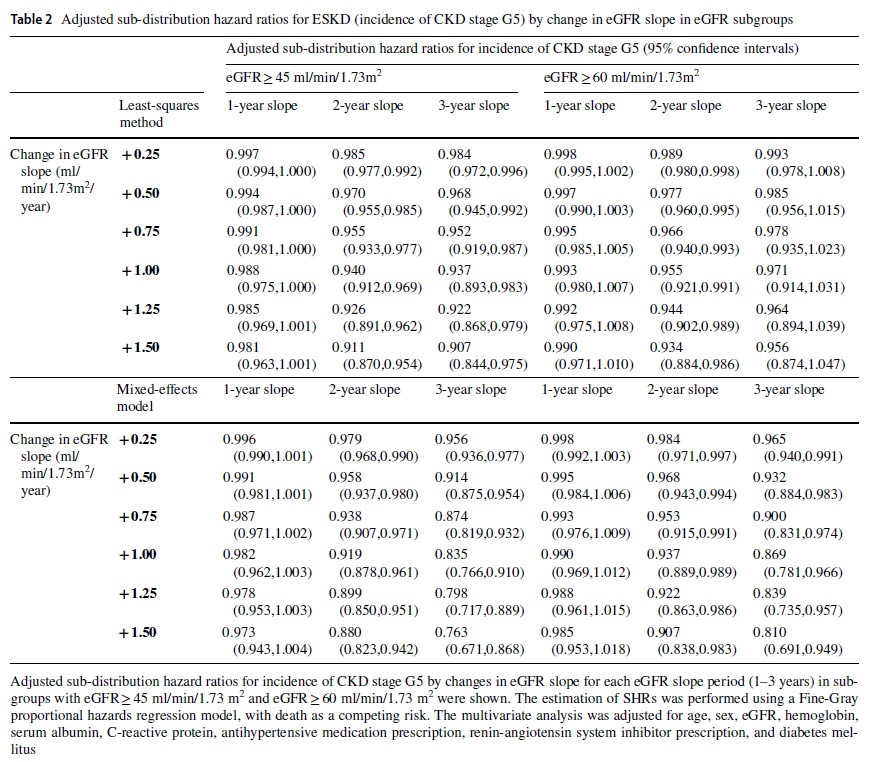
表2は、CKDステージ1-3a(eGFR ≥ 45 ml/分/1.73 m²)またはG1-G2(eGFR ≥ 60 ml/分/1.73 m²)別に、eGFR勾配の変化に対する調整済みSHR(部分分布ハザード比)を示しています。この分析ではESKDのアウトカムをCKDステージG5の発生と定義しました。
混合効果モデルでの結果
- eGFR ≥ 60 ml/分/1.73 m²(より早期のCKD)をターゲットにした場合、SHRの減少はわずかに小さくなりました。
- 2年勾配と比較して、3年勾配ではSHRの減少がより大きくなりました。
最小二乗法での結果
サブグループ間やeGFR勾配計算期間によるSHRの有意差は認められませんでした。
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
<より進行した腎不全における分析>
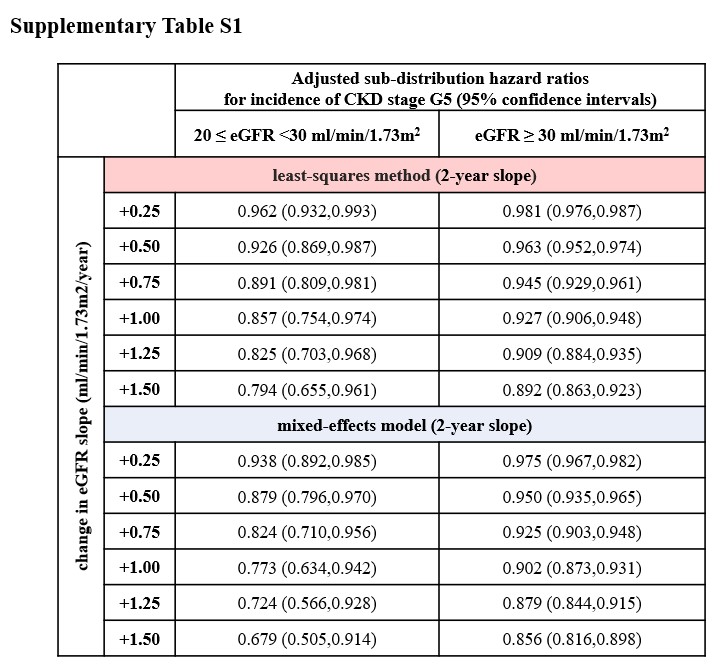
ベースラインeGFRが20~30 ml/分/1.73m²の範囲(より進行した腎不全)の集団において、2年勾配とCKDステージG5の発生との関連を分析しました。
主な結果
ベースラインeGFR ≥ 30 ml/分/1.73m²の集団と比較して、ベースラインeGFRが20~30 ml/分/1.73m²のサブグループでは、SHRの減少がより大きいことが観察されました(補足表S1参照)。
この結果は、より進行した腎不全の患者ではeGFR勾配の変化がESKDリスクにより顕著な影響を及ぼす可能性を示唆しています。
Clin Exp Nephrol. 2023 Oct;27(10):847-856.
考察:
本研究の主な知見
本研究では、早期CKDの日本人患者に焦点を当て、eGFR勾配とESKD(末期腎不全)の部分分布ハザード比(SHR)との関係を検討しました。
分析の結果、以下の重要な知見が得られました:
- eGFR勾配が緩やかになるほど(減少するほど)、ESKDのリスクが低下する傾向が観察されました
- eGFR勾配を計算する際は、1年間よりも2~3年間のeGFR値を使用する方が適切であることが示唆されました
eGFR勾配計算期間に関する考察
本研究でのeGFR勾配の計算期間は1年、2年、3年でした。
図2に示されるように、1年間のeGFR値から勾配を計算すると、2年または3年のデータを使用した場合よりも、多くの参加者でより大きな変動が観察されました。
これには以下の理由が考えられます:
- 勾配の計算期間が短いと、eGFR測定回数が減少する
- 短期的な測定値の変動の影響を受けやすくなる
- 急性腎障害や筋肉量の変化の影響を受けやすくなる
NKF-FDA-EMAワークショップでも、eGFR勾配の信頼性の高い計算のためには2~3年の追跡期間からのデータを使用することが推奨されており、本研究の結果からも、2~3年間のeGFRに基づくeGFR勾配の使用は1年よりも適切と考えられました(図2および3参照)。
最適な計算期間に関する考慮事項
eGFR勾配の最適な計算期間は、研究対象集団の特性によって異なる可能性があります。eGFR勾配の計算期間を設定する際には、基礎疾患としてのCKDやベースラインGFRなどの要因を考慮する必要があります。
SGLT2阻害薬によるeGFRの初期低下など、急性効果を生じる介入研究では、そのような効果の存在や大きさを事前に予測できない場合があり、介入開始からの総合的な勾配を用いて評価することが適切です。
ただし、計算期間が短いと、急性効果による治療効果の過小評価のリスクがあり、少なくとも2~3年の観察期間が望ましいと考えられます。
したがって、2年、3年、あるいはそれ以上の期間のどれが最適かを決定する課題に対処するためには、さらなる研究が必要です。
分析手法と結果に関する詳細考察
一次分析と二次分析の相違点
一次分析(ESKDを透析開始と定義):
- 混合効果モデルでは、2年勾配と比較して3年勾配で変化量が増加するにつれてSHRが減少する傾向がありました
- 一方、最小二乗法で計算されたeGFR勾配ではそのような傾向は見られませんでした
二次分析(ESKDをCKDステージG5の発生と定義):
- 混合効果モデルと最小二乗法の両方において、2年勾配よりも3年勾配でSHRの減少が大きくなりました(図3参照)
手法間の違いの理由
これらの違いは以下の理由によると考えられます:
- 分散の違い:
- 混合効果モデルでは推定値による補正のため分散が小さくなった
- 最小二乗法では個々の参加者のeGFR値の変動の影響により変動性が増加した
- eGFR勾配の変動性がSHR推定に影響:
- eGFR勾配の変動性がSHRの推定に影響を与えた可能性があり、各モデルから得られたSHRに差異が生じた可能性がある
- SHRを推定する際に、eGFR勾配の変動性が結果に影響を与え、2つのモデル間の差異につながった可能性がある
- どちらの方法がより適切かは、分析対象のデータの性質と研究目的に依存します
アウトカム発生率の影響
透析開始の発生率はCKDステージG5の発生率と比較して相対的に低く(約0.2~0.4%対約1.4~2.4%)、これにより両モデルでSHR推定のばらつきが大きくなり、推定精度が低下した可能性があります。
特に、3年間のeGFR勾配は、1年勾配(877±491日)および2年勾配(706±346日)と比較して、平均観察期間が短く(495±215日)、これも影響を与えた可能性があります。
先行研究との比較
本研究の結果を先行研究と比較しました。
NKF-FDA-EMAワークショップでは、eGFR勾配の減少が0.5~1.0 ml/分/1.73 m²/年であると、ESKDリスクの低下に関連する可能性があることが示唆されています。
本研究では、2年および3年勾配がより緩やかになるにつれて、ESKDリスクが低下する傾向が観察されました。
この傾向は特に3年勾配で強く、eGFR勾配の緩やかな減少がESKDリスクの低下と関連するというNKF-FDA-EMAワークショップの知見と一致していました。
今後の課題
ただし、本研究で使用された集団が一般的なCKD集団と比較して腎アウトカムが悪化する可能性などの後述の制限を考慮すると、NKF-FDA-EMAワークショップの結果を早期CKDの一般的な日本人集団に外挿するには、複数のコホートでの検証を含む更なる調査が必要です。
さらに、最新の研究では、アルブミン尿の変化とeGFR勾配を組み合わせることでエンドポイント推定の精度が向上することが報告されており、この分野でのさらなる研究の可能性が示されています。
研究の限界と結論
本研究の限界
- 観察研究の限界
- 電子カルテ情報に基づくデータベースを用いた観察研究であり、測定されない交絡因子を考慮できませんでした
- 以下のような腎予後と密接に関連すると考えられる情報がデータベースから収集されていませんでした:
- 心血管疾患の既往歴
- 血圧
- 喫煙歴
- 身体活動
- CKD進行に関連する因子(アルブミン尿や蛋白尿など)が欠損していることが多く、共変量として調整されていませんでした
- そのため、交絡調整が不十分である可能性があります
- 外部妥当性の制限
- J-CKD-DB-Exの中で、死亡率と透析開始に関する情報を含む施設からのデータのみが分析されたため、分析結果の外部妥当性は限定的でした
- データ期間と症例数の制限
- J-CKD-DB-Exのデータ期間は最大5年間でした
- eGFR勾配計算期間を除いて、観察期間中の透析開始参加者は少数でした
- 特にベースラインeGFRが45 ml/分/1.73 m²超または60 ml/分/1.73 m²超の参加者に限定すると、アウトカム数は稀でした
- より早期のCKD集団に限定した場合に同様の結果が得られるかどうかを判断するには、さらなる調査が必要です
- 選択バイアス
- J-CKD-DB-Exは日本の大学病院を対象としており、一般的なCKD集団よりもCKDの重症度が高いと考えられます
- そのため、分析対象集団の腎予後は、CKDを持つ一般的な日本人集団よりも悪いと予想されます
- J-CKD-DB-Exの患者登録基準に関連した選択バイアスもありました:
- 登録基準:(1)年齢18歳以上 および (2)研究期間中のいずれかの時点で蛋白尿≥1+(試験紙法)および/またはeGFR<60 ml/分/1.73 m²
- そのため、ベースラインeGFRが60 ml/分/1.73 m²以上の参加者の中で、eGFR<60 ml/分/1.73 m²または蛋白尿≥1+を発症した患者のみが選択され、必然的に腎予後が悪い集団となります
本研究では、NKF-FDA-EMAワークショップで引用されたGramsらの研究の各群の平均eGFR勾配と本研究の平均eGFR勾配を比較しました。
その結果、本研究で分析された参加者のベースラインにおける腎機能低下率は、先行研究で報告されたものから大きく逸脱していませんでした。
結論:
日本のCKD患者の実世界データベースであるJ-CKD-DB-Exを用いて、NKF-FDA-EMAワークショップで提示された「緩やかなeGFR勾配とESKDリスク減少の関連性」が日本の早期CKD患者にも適用されるかどうかを調査しました。
本研究の一般化可能性にはいくつかの限界がありますが、2年または3年にわたるeGFR値から計算された緩やかなeGFR勾配がESKDリスクの減少と関連していることが示唆されました。
【補足情報】
◎最小二乗法と混合効果モデルという2つの異なる統計手法を用いる主な目的は、それぞれの手法の特性を活かした分析結果の頑健性を高めるためです。
最小二乗法の特徴
- 単純さ: 計算が比較的簡単で理解しやすい基本的な統計手法です
- 直接的なアプローチ: 各患者の実測データポイントだけを使用して直線を当てはめます
- 個別分析: 各患者ごとに独立して勾配を計算します
- 欠点: 外れ値や測定誤差の影響を受けやすく、データポイントが少ない場合は特に不安定になりがちです
混合効果モデル(線形混合モデル)の特徴
- 複雑さ: より高度な統計モデルです
- 集団と個人の情報を統合: 全患者の傾向(固定効果)と個々の患者の変動(ランダム効果)を同時に考慮します
- 借用効果: 少ないデータポイントしかない患者のeGFR勾配推定を、全体の集団データを利用して「借用」(収縮推定)することで安定化させます
- 利点: 外れ値や測定誤差の影響を受けにくく、少ないデータポイントでもより安定した推定が可能です
両手法を使用する理由
- 結果の頑健性の確認: 異なる統計手法でも同様の結果が得られれば、発見された関連性がより信頼できると考えられます
- データ特性への対応:
- 本研究では測定回数が少ない患者も多く含まれているため、混合効果モデルはより安定した推定を提供できます
- 一方、最小二乗法は単純で直接的なアプローチを提供します
- 方法論的バイアスの評価: 異なる統計手法による結果の違いを評価することで、方法論的バイアスの影響を把握できます
- 先行研究との比較可能性: 過去の研究で使われている様々な手法と比較できるようにするためです
◎部分分布ハザード比(Subdistribution Hazard Ratio: SHR)の解説
部分分布ハザード比(SHR)は、競合リスク(competing risk)が存在する状況で用いられる統計手法であり、特に医学研究で重要な役割を果たします。
基本的な概念
- 競合リスク:
- 研究対象の主要アウトカム(例:末期腎不全の発生)以外に、別のアウトカム(例:死亡)が起こることで、主要アウトカムの観察が妨げられる状況
- 標準的なハザード比との違い:
- 通常のCox比例ハザードモデルでは、競合する事象が発生した場合、その後のフォローアップが打ち切り(censoring)として扱われます
- しかし、この打ち切りは「ランダム」ではなく(死亡した患者は末期腎不全になることができない)、バイアスを生じる可能性があります
- 部分分布ハザード比の特徴:
- 競合事象を打ち切りとして扱わず、リスク集団に留めたまま分析します
- 主要アウトカムの累積発生率(cumulative incidence)を直接モデル化します
本研究での適用
この研究では:
- 主要アウトカム:末期腎不全(ESKD)の発生(透析開始またはCKDステージG5への進行)
- 競合リスク:死亡(患者が死亡すると、もはや透析を開始することや末期腎不全に進行することはできない)
- 分析手法:Fine-Grayの比例ハザード回帰モデルを使用して部分分布ハザード比を計算
解釈の仕方
SHRの解釈:
- SHR < 1:説明変数(本研究ではeGFR勾配の変化)が増加すると、主要アウトカム(ESKD)の発生リスクが減少
- SHR = 1:説明変数がアウトカム発生リスクに影響を与えない
- SHR > 1:説明変数が増加すると、アウトカム発生リスクが増加
この研究では、eGFR勾配がより緩やかになる(+0.5〜+1.0 ml/分/1.73 m²/年の変化)ほど、SHRが1より小さくなり(例:0.96、0.90など)、ESKDのリスクが低下することが示されています。
死亡という競合リスクを適切に考慮することで、eGFR勾配とESKD発生の関連性をより正確に評価することができました。
