PubMed URL:https://pubmed.ncbi.nlm.nih.gov/37540060/
タイトル:Mineralocorticoid receptor antagonist use and the effects of empagliflozin on clinical outcomes in patients admitted for acute heart failure: Findings from EMPULSE
<概要(意訳)>
目的:
ミネラルコルチコイド受容体拮抗薬(MRA)は、慢性心不全で駆出率が低下(HFrEF)した患者における心不全入院と死亡を減少させ、慢性心不全で駆出率が維持(HFpEF)されている特定の患者では心不全入院を減少させる可能性がある。
そのため、MRAは非代償性心不全で入院した患者に頻繁に使用されている。
慢性心不全において、SGLT 2阻害薬が臨床転帰に及ぼす有益な効果は、バックグラウンドでのMRAの使用とは無関係であるように思われる。
さらに、SGLT2阻害薬はMRAを使用しているHF患者における著しい高カリウム血症のリスクを抑制し、MRA治療の実施と継続を容易にするかもしれない。
EMPULSE(A Study to Test of Effect of Empagliflozin in Patients Who Are In Hospital for Acute Heart Failure; NCT04157751)試験では、エンパグリフロジンを急性心不全(AHF)で入院中の患者に投与開始したところ、プラセボよりも高い臨床効果が得られた。
しかし、AHFにおけるSGLT2阻害薬とMRAの交互作用はまだ報告されていない。
本研究では、EMPULSE試験のデータを用いて、MRAの使用に関連する患者特性を調査し、ベースライン時のMRA使用の有無におけるエンパグリフロジンの有効性と安全性(対プラセボ)を評価することを目的とした。
方法:
<試験デザイン>
EMPULSE試験は、AHFにおけるエンパグリフロジン経口投与の臨床的有用性、安全性、忍容性に関するプラセボと比較した有用性を評価するためにデザインされた多国籍、多施設、無作為化、二重盲検試験である。
試験では、初期安定化後(入院後24時間から5日の間)にAHFで入院した患者を、エンパグリフロジン(1日1回10mg)またはプラセボのいずれかを90日間投与する群に1:1で無作為に割り付けた。
研究デザインの詳細と主要な研究結果は別のところで発表されている。
簡単に述べると、AHFと診断され入院し、フロセミド40mg(日本人は20mg)以上の静脈内投与または同等の治療を受けた患者である。
主な除外基準は、「肺塞栓症、脳血管障害、急性心筋梗塞、1型糖尿病、無作為化前90日間のSGLT1阻害薬またはSGLT2阻害薬による治療、eGFR<20ml/分/1.73m2または透析が必要なAHF」であった。
入院中、対象となる患者は、収縮期血圧(SBP)が100mmHg以上で低血圧の症状がなく、利尿薬の静脈内投与量が増加せず、血管拡張薬および/または強心薬の静脈内投与がないことで定義される初期安定後(入院から24時間~5日目)、試験に無作為に割り付けられた。
主要アウトカムは、「全死亡、HFイベント数、初発のHFイベントまでの期間、90日後のKansas City Cardiomyopathy Questionnaire total symptom score(KCCQ-TSS:総合症状スコア)のベースラインからの変化における5ポイント以上の差を含む階層的複合における臨床的有用性」と定義され、win ratio(WR)法を用いて評価された。
<エンドポイント>
この解析では、「全死亡、HFイベント数、初発のHFイベントまでの期間、90日後のKCCQ-TSSスコアのベースラインからの変化における5ポイント以上の差」という、当初の主要な階層的複合アウトカムをWR法により評価した。
さらに、(i)主要アウトカムの各要素、(ii)(初発の)心血管死またはHFイベントの複合、(iii)HF入院の総数、(iv)全ての原因による入院、(v)呼吸困難、起座呼吸、疲労の点数(0~3点)の合計として算出される臨床的うっ血スコアについても検討した。
MRAサブグループにおける臨床的有用性の主要な階層的複合エンドポイントに対する治療効果を評価するため、ベースライン時のMRA使用者と非使用者でエンパグリフロジンとプラセボをWR法で比較した。
結果:
<ベースライン時にMRAを使用していた患者の特性>
EMPULSE試験で無作為化された530例の内、ベースライン時にMRAを使用していたのは276例(52%)で(ほとんどがスピロノラクトン25mg/日)、使用していなかったのは254例(48%)であった。
ベースライン時にMRAを使用していた患者は若く、ヨーロッパ出身者が多く、HFの持続期間が長く、血圧が低く、左室駆出率が低く、虚血性HFの頻度が高く、腎機能が良好で、KCCQスコア(健康状態)が高く、アンジオテンシン変換酵素阻害薬(ACE阻害薬)/アンジオテンシン受容体拮抗薬(ARB)/アンジオテンシン受容体ネプリライシン阻害薬(ARNI)およびβ遮断薬による治療を受けている頻度が高かった。
血清カリウム値はMRAの使用有無に関わらず、同程度であった(表1)。
<ベースライン時のMRA使用有無におけるアウトカム>
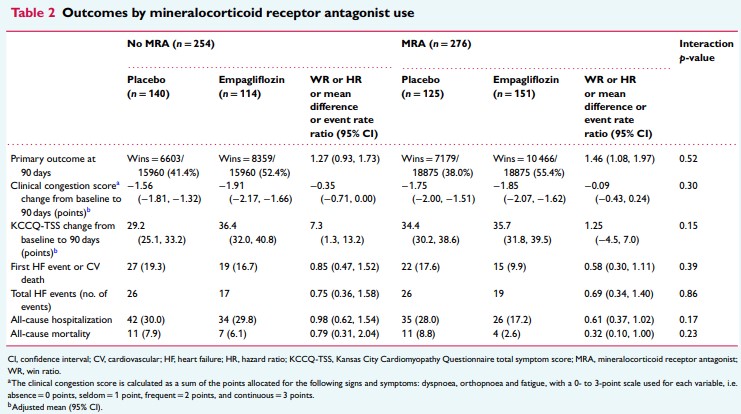
主要評価項目である階層的複合アウトカムは、ベースラインのMRA使用状況に関わらず、プラセボに対するエンパグリフロジンの有用性を示した[MRA使用群でWR 1.46(95%CI 1.08-1.97)、MRA非使用群でWR 1.27(95%CI 0.93-1.73)、交互p値=0.52]。
心血管死またはHF入院、HF入院の総数、全死亡の複合転帰は、ベースラインのMRA使用率にかかわらず、エンパグリフロジンのほうがプラセボよりも発生頻度が低く、健康状態(KCCQスコア)および臨床的うっ血スコアは、ベースラインのMRA使用率にかかわらず、エンパグリフロジンのほうがプラセボよりも改善した(全交互p値>0.1)。
全ての原因による入院に対するエンパグリフロジンの効果は、ベースラインのMRA使用による有意差は認められなかった[MRA使用者のHR 0.61(95%CI 0.37-1.02)、MRA非使用者のHR 0.98(95%CI 0.62-1.54)、交互p値=0.17](表2)。
Eur J Heart Fail. 2022 Oct;24(10):1844-1852.
<ベースライン時のMRA使用有無におけるバイタルサインとバイオマーカーの変化>
体重、ヘモグロビン、尿酸、NT-proBNP、ナトリウムの変化は、ベースラインのMRA使用量に関係なく同様であった(全交互p値>0.1)(表3)。
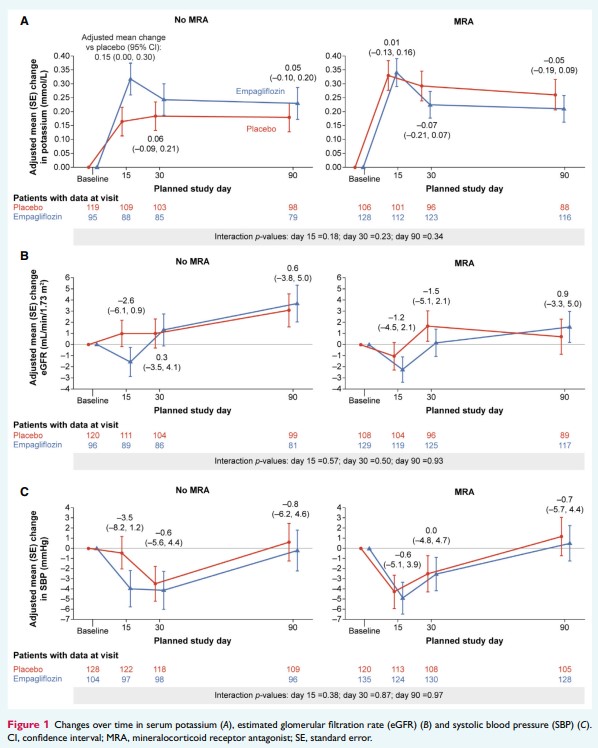
血清カリウム、eGFR、SBPの経時的変化もベースライン時のMRA使用有無で有意な差はなかった(図1)。

Eur J Heart Fail. 2022 Oct;24(10):1844-1852.
<ベースライン時のMRA使用有無における有害事象>
エンパグリフロジンの安全性プロファイルは、ベースライン時のMRA使用有無に関わらず良好であった。
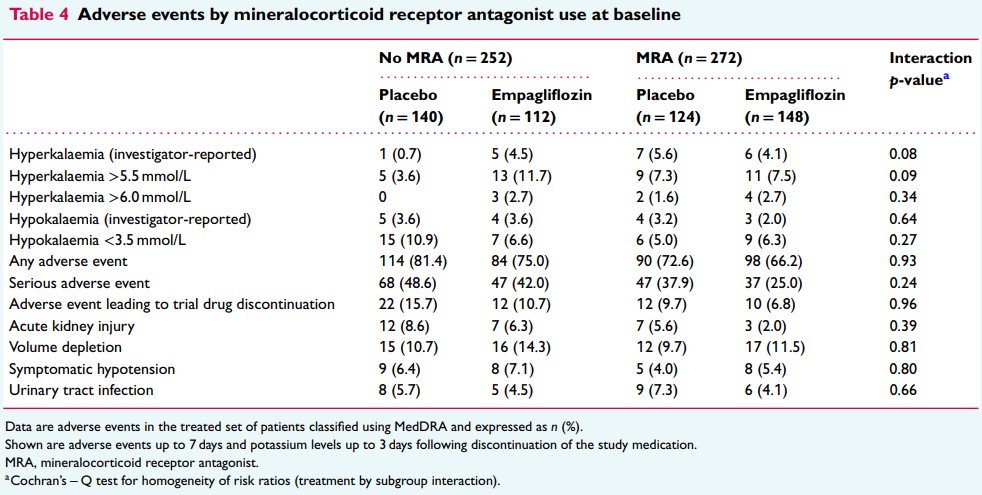
治験責任医師が報告した高カリウム血症および重篤な高カリウム血症は頻度が低く(6%未満)、ベースライン時のMRA使用有無による差は認められなかった。
すべての有害事象[高カリウム血症、低カリウム血症、あらゆる有害事象、重篤な有害事象、
治験薬投与中止に至った有害事象、急性腎障害、体液量減少、症候性低血圧、尿路感染症]は、ベースライン時のMRA使用有無に関わらず、有意な差はなかった(表4)。
Eur J Heart Fail. 2022 Oct;24(10):1844-1852.
<試験期間中におけるMRA治療の開始と中止>
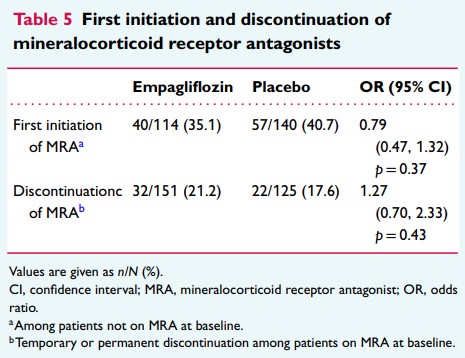
ベースライン時、エンパグリフロジン投与群ではより多くの患者がMRAを受けていた[エンパグリフロジン群 n/N=151/265(57.0%)、プラセボ群 n/N=125/265(47.2%)、p= 0.024](表5)。
入院中にMRAの新規治療が開始されたのは、プラセボ群で24例(前治療歴のない患者140例の内17.1%)、エンパグリフロジン群で19例(前治療歴のない患者114例の内16.7%)であった。
入院中にMRAを開始した患者において、血清カリウムはベースラインから90日目まで0.6 mmol/L増加し、プラセボ群とエンパグリフロジン群の絶対差はわずか(0.1~0.2mmol/L)であった(オンライン補足表S1)。
90日時点では、エンパグリフロジン群168例(63.4%)プラセボ群152例(57.4%)がMRA治療を受けていた。
Eur J Heart Fail. 2022 Oct;24(10):1844-1852.
考察:
このEMPULSE試験の事後解析では、ベースラインのMRA使用の有無で患者特性に差があることが示され、前者はより若く、より良好な腎機能を有し、虚血性HFが多く、より重度に左室駆出率が低下していた。
MRA使用の有無で患者特性に相違があったが、エンパグリフロジンはMRA使用の有無に関わらず、同様の臨床的有用性を示した。
ベースライン以後の血清カリウム、eGFR、血圧、有害事象は、ベースラインのMRA使用の有無で、エンパグリフロジンとプラセボの間に大きな差は認められなかった。
MRAとエンパグリフロジンによる治療を同時に開始しても、MRAとプラセボを投与開始した場合と比較して、臨床的に意味のあるカリウムの変化は認められなかった。
43例(入院中にMRAの新規治療が開始されたプラセボ群24例、エンパグリフロジン群19例)の小さなサブグループに基づくものではあるが、これらの所見は、HF治療にSGLT2阻害薬がルーチンに使用される前に行われたSTRONG-HF試験を発展させ、入院中にMRAとエンパグリフロジンを併用した治療を開始することを支持するものである。
これらの所見を総合すると、エンパグリフロジンはMRA治療に加えて有益であり、忍容性も良好であることが示唆された(図1)。
90日間の追跡期間におけるMRAの開始および中止に関するデータは、エンパグリフロジン群とプラセボ群との間に有意差を示さなかった。
EMPEROR-Reduced試験およびEMPEROR-Preserved試験では、エンパグリフロジン投与群ではMRAの開始および中止が少なかったが、これはエンパグリフロジン投与により良好な臨床状態が得られたためと考えられる。
とはいえ、有益性のメカニズムが異なっており、かつ重複していないことから、臨床現場では、SGLT2阻害薬の使用に関わらず、臨床的適応がある場合にはいつでもMRA治療を継続することが望ましい。
EMPULSE試験では、ベースライン時にMRAを使用していた患者は50%強であり、これらの患者は殆どが(新規のAHFイベントではなく)、除脈を経験した慢性のHFrEF患者であった。
使用されたMRAの用量[スピロノラクトンまたはエプレレノン(カリウム保持性利尿薬)の中央値25mg/日]は、利尿用量ではなく、アルドステロン遮断作用、抗リモデリング作用、抗線維化作用をもたらすものであった。
エンパグリフロジン10mg/日は、初期にナトリウム利尿作用と利尿作用がみられ、その後、抗酸化ストレス抑制作用とオートファジー促進作用がみられ、これらはベースラインのMRAの使用とは無関係に作用するようであることから、これらの薬剤の作用機序は異なるが相補的であることが支持される。
SGLT2阻害薬とMRAは、共に心臓や腎臓以外にも多面的な効果を示し、入院や死亡率を減少させる可能性がある。
EMPEROR-Reduced試験、EMPEROR-Preserved試験、DAPA-HF試験、DELIVER試験に登録された幅広い駆出率の慢性心不全患者において、SGLT2阻害薬はベースラインのMRA使用の有無に関わらず、一般的に有効であり、これらの薬剤の独立した効果をさらに支持した。
重要なことは、慢性心不全において、SGLT2阻害薬に無作為に割り付けられ、ベースライン時にMRAを服用していた患者では、高カリウム血症の発生率が有意に低かったことである。
このことは、SGLT2阻害薬がMRAの忍容性を高め、慢性心不全における治療アドヒアランスを向上させる可能性を示唆している。
EMPULSE試験において、高カリウム血症(治験責任医師報告、カリウム>5.5mmol/L、カリウム>6mmol/Lのいずれか)の絶対数は稀であり、いずれの高カリウム血症の定義においても、MRA使用の有無に関わらず、有意な交互作用は示されなかった。
この結果から、エンパグリフロジンとMRAの併用は、MRA単独と比較して過剰な高カリウム血症を引き起こさないことが示唆された。
AHF患者は、「高カリウム血症」を含む副作用を引き起こす可能性のある薬剤や用量の変更を頻繁に経験するため、これは臨床的に重要である。
エンパグリフロジンとMRAの併用は、高カリウム血症を含む過剰な有害事象をもたらさなかった。
AHFにおいて考慮すべき他の重要なパラメータは、「腎機能と血圧」である。
SGLT2阻害薬とMRAは共に、初期(±4~8週間)にeGFR低下(イニシャルディップ)を引き起こす可能性があるが、その後eGFRは回復する。
この点に関して、我々の研究では、エンパグリフロジンとMRAの併用で過剰なeGFRの低下は認められなかったことを示している。
さらに、ベースライン時にエンパグリフロジンとMRAを服用している患者間で、SBPの変化や症候性低血圧の過度のリスクに差は認められなかった。
本研究には、いくつかの限界があることを認識すべきである。
エンパグリフロジンと異なり、MRAの使用は患者に無作為に割り付けられたものではなく、その結果、MRAの使用者と非使用者では患者プロファイルが大きく異なるため、ベースラインのMRAの使用とエンパグリフロジンの潜在的な効果修飾との間の因果関係を推論することができないなどである。
ここで使用されたMRAの用量は、慢性心不全の用量(すなわち、利尿薬の用量ではない)であり、これらの所見はAHFでより高用量のMRA(例えば、スピロノラクトン100mg/日)を使用している患者に一般化することはできない。
無作為化前のMRA治療期間は記録されていないが、MRAの用量は慢性心不全で使用された用量と一致しており、患者は本試験に組み入れられる前からMRA治療を受けていたことが示唆される。
本研究では、HFのサブタイプ間におけるMRA治療の効果の差を検出するための検出力は限られている。
結論:
エンパグリフロジンは、ベースラインのMRA(ミネラルコルチコイド受容体拮抗薬)使用の有無に関わらず有益であり、忍容性も良好であった。
これらの所見は、AHF(急性心不全)で入院した患者において、エンパグリフロジンをバックグラウンドのMRA治療に加えて使用することを支持するものである。
【参考情報】
STRONG-HF試験
Journal_Club_20221121.pdf (chiba-u.jp)
治療最適化のベネフィットに重点を置いた STRONG-HF 試験 – Cardio ThinkLab
急性心不全症状の対応
