PubMed URL: https://pubmed.ncbi.nlm.nih.gov/35379060/
タイトル:Safety and effectiveness of empagliflozin according to body mass index in Japanese patients with type 2 diabetes: a subgroup analysis of a 3-year post-marketing surveillance study
<概要(意訳)>
背景:
2型糖尿病の適応を取得した血糖降下薬であるエンパグリフロジン(SGLT2阻害薬)は、日本の市販後調査(PMS)で全体的に忍容性と有効性を実証したが、BMI(体格指数)における影響は不明である。
本研究では、このPMSデータをサブ解析することにより、日本の実臨床におけるエンパグリフロジンの安全性プロファイルと有効性に対するBMIの潜在的な影響を評価した。
方法:
本研究は、2015年6月から2020年12月の間に日本の1,103の施設で実施され、患者1人あたり3年間の観察を実施した。
研究対象集団は、以前にエンパグリフロジンによる治療を受けたことがない2型糖尿病患者であるが、以前に別のSGLT2阻害薬による治療を受けた患者も適格患者とした。
患者データは、エンパグリフロジンによる治療開始後3、12、24、36ヶ月の時点で電子症例報告フォームによって収集される前に匿名化された。
「主なアウトカム評価」は、研究者とスポンサーのいずれか、または両者がエンパグリフロジン治療による有害事象として定義されたADR(薬物有害反応)の発生率であった。
「その他の安全性のアウトカム評価」には、重篤なADR[生命を脅かすもの、死亡に至るもの、入院が必要または長期入院にわたるもの、持続的または重大な障害をもたらすもの、または先天異常/先天性欠損症]および特に関心のある事前に指定されたADR[ケトン体の増加、骨折、心血管イベント、糖尿病性ケトアシドーシス、生殖器感染症、低血糖、肝障害、悪性腫瘍、腎障害、尿路感染症、多尿/頻尿、尿量減少に関連する有害事象]が含まれていた。
ADRの分類には、MedDRAバージョン23.1が使用された。
「事前に指定された有効性のアウトカム評価」は、HbA1cとFPG(空腹時血糖値)レベルの変化であった。
また、体重、血圧、脈拍数、ヘマトクリット、ヘモグロビン、脂質、クレアチニン、eGFRのパラメータ変化も評価された。
結果:
8,145例の患者が登録され、8,059例の電子症例報告書が収集された。
ベースラインでは、7,931例の内、1,138例(14.35%)のBMIデータが欠落していた。
全体の平均BMIは28.12 kg/m2であり、BMI<20 kg/m2は163例(2.06%)、BMI 20~<25 kg/m2は1,688例(21.28%)、BMI 25~<30 kg/m2は2,962例(37.35%)、BMI≧30 kg/m2は1,980例(24.97%)であった。
全体の平均体重は75.56 kgであり、BMI<20で47.27 kg、BMI 20~<25で61.49 kg、BMI 25~<30で73.97 kg、BMI≧30で92.48 kgであった。
平均年齢は58.7歳で、年齢とBMIサブグループの間には反比例の関係があり、平均年齢は低BMIのサブグループの方が高かった。
全体として、4,996例(62.99%)は男性であり、女性は高BMIサブグループよりも低BMIサブグループに含まれている割合が高かった。
2型糖尿病の罹病期間は平均8.23年、平均HbA1cは8.02%、平均FPGは160.2 mg/dlであった。
ほとんどの患者(84.13%)に併存症があり、高血圧(58.18%)と脂質異常症(57.51%)が最も一般的であり、いずれも高BMIサブグループでより一般的であった。
有病率の傾向がBMIサブグループで異なる他の併存疾患には、肝機能障害(全体の24.83%)および痛風/高尿酸血症(10.64%)が含まれ、高BMIサブグループで一般的であった。
一方で、骨粗鬆症(1.73%)と悪性腫瘍(1.16%)は、低BMIサブグループで一般的であった。
少なくとも1つの血糖降下薬(76.85%)を併用している患者(全体の76.85%)では、DPP-4阻害薬(52.94%)とα-グルコシダーゼ阻害薬(7.65%)の使用は、低BMIサブグループでより一般的であった。
一方で、メトホルミン(41.66%)を含むビグアニド系抗糖尿病薬およびGLP-1受容体作動薬(4.75%)の使用は、高BMIサブグループでより一般的でした。
スタチン(35.25%)と降圧薬の使用も、高BMIサブグループでより一般的であった。
エンパグリフロジンによる平均治療期間は、28.10ヶ月(中央値36.53ヶ月)であった。
全体として59.54%の患者[BMI <20 kg/m2の48.47%、BMI 20〜<25 kg/m2の59.00%、BMI 25〜<30 kg/m2の61.41%、BMI≥30 kg/m2の59.49%]が、36ヶ月以上の間、エンパグリフロジンによる治療を受けた。
エンパグリフロジンによる治療を中止した全体の主な理由は、患者の希望(n=601、7.58%)、有害事象(n=516、6.51%)、変化なし/疾患の進行(n=263、3.32%)、改善/寛解(n=157、1.98%)でった。
有害事象と患者の希望でエンパグリフロジンによる治療の中止は、BMI<20 kg/m2の患者グループで最も一般的な理由であった。
7,931例の内、1,024例(12.91%)は、エンパグリフロジンによる治療中に1つ以上のADR(薬物有害反応)を経験した[BMI <20 kg/m2の11.66%(19例)、BMI 20〜<25 kg/m2の12.03%(203例)、BMI 25〜<30 kg/m2の13.88%(411例)、BMI≥30 kg/m2の14.90%(295例)]。
過度な排尿/頻尿は、BMI 25〜<30 kg/m2を除く、すべてのBMIサブグループ[BMI <20 kg/m2の1.84%、BMI 20〜<25 kg/m2の0.95%、BMI 25〜<30 kg/m2の1.59%、BMI≥30 kg/m2の1.31%]で特に関心のある最も一般的なADRであった。
BMI 20〜<25 kg/m2の患者では、特に関心のある最も一般的なADRは、尿路感染症(1.07%)であった[BMI <20 kg/m2では0%、BMI 25〜<30 kg/m2の1.11%、BMI≥30 kg/m2の1.31%]。
筋力低下は、BMI 25〜<30 kg/m2の1例で発生したが、深刻ではなかった。
深刻なADRは、全体の166例(2.09%)で報告され、BMI <20 kg/ m2の5例(3.07%)、BMI 20〜<25 kg/ m2の42例(2.49%)、BMI 25〜<30 kg/ m2の61例(2.06%)、BMI≥30 kg/ m2の43例(2.17%)で発生した。
個々の重篤なADRの発生率は、すべてのBMIサブグループで1%未満であった。
全体で13例(0.16%)の死亡がADRとして報告され、BMIサブグループでは、BMI <20 kg/ m2の0例、BMI 20〜<25 kg/ m2の6例(0.36%)、BMI 25〜<30 kg/ m2の3例(0.10%)、BMI≥30 kg/ m2の1例(0.05%)、BMI不明で3例(0.26%)発生した。
全体的なADRもベースラインの体重カテゴリ間で比較された[体重≦50 kgの15.25%(43例)、>50-70 kgの13.71%(363例)、>70-90 kgの12.44%(394例)、90<の14.27%(171例)、体重不明で8.32%(53例)]。
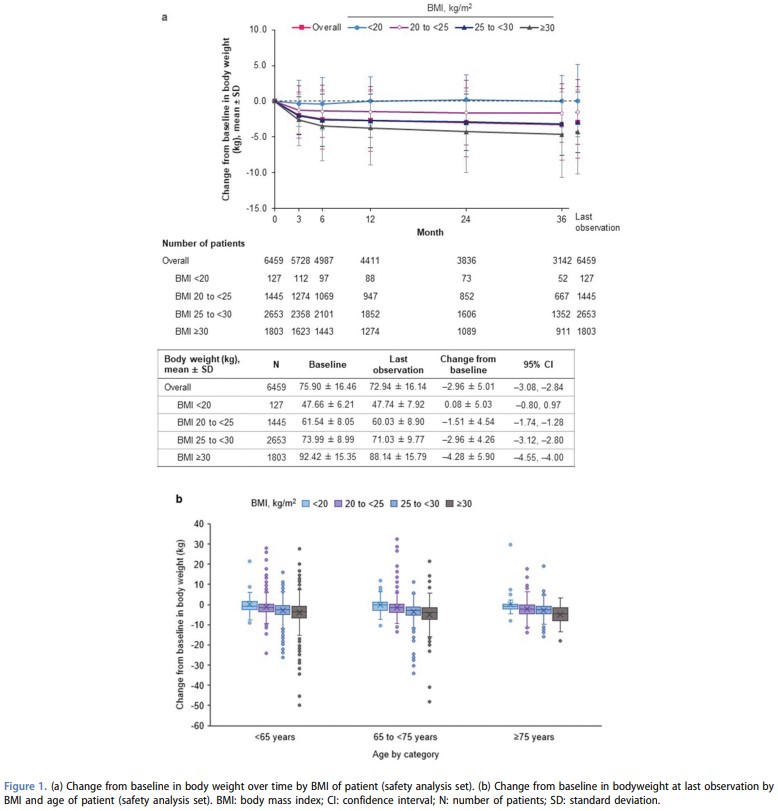
安全性解析対象の患者群では、エンパグリフロジン治療により、時間の経過とともにベースラインからの全体的な体重の大幅な減少が見られた。
最終観察では、全体で平均 -2.96(95%CI -3.08 ~-2.84) kgの体重を減少させることが示された。
しかし、体重減少の大きさとBMの間には、正の相関があり、ベースラインの高BMIサブグループでは体重減少が大きく、BMI BMI <20 kg/ m2の患者では体重変化がほとんどなかった。
この関連性は、65歳未満、65~75歳未満、75歳以上のサブグループ間で一致していた。
Expert Opin Drug Saf. 2022 Nov;21(11):1411-1422.
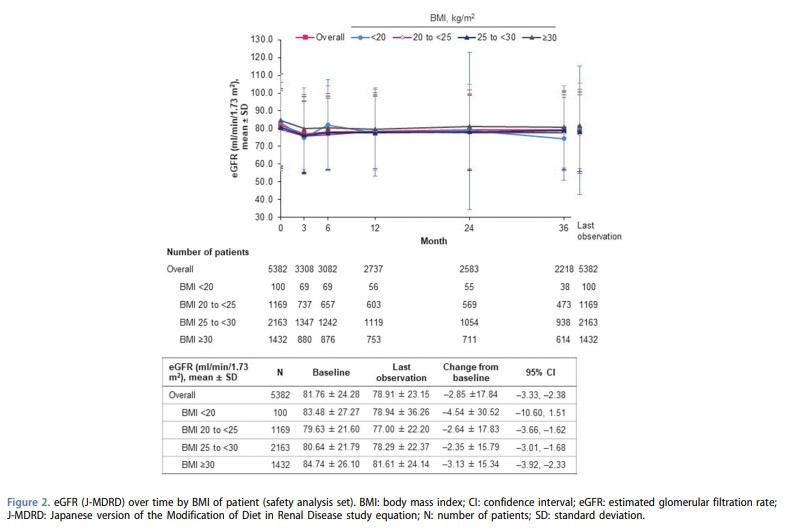
全体のeGFRはベースラインの平均81.76 ml/分/1.73 m2から、最終観察時には、平均-2.85(95%CI -3.33~-2.38)ml/分/1.73 m2まで減少した。
eGFRの平均変化量は、BMI 20〜<25、25〜<30、≥30 kg/m2の患者では同様[それぞれ、-2.64、-2.35、-3.13 ml/分/1.73 m2]であったが、BMI <20の患者では、-4.54 ml/分/1.73 ml/分/1.73 m2と大きかった。
ベースラインから3カ月時点までの平均変化量は、全体で-3.54 ml/分/1.73 m2[BMI <20 kg/ m2で–3.78、BMI 20〜<25 kg/ m2で–3.00、BMI 25〜<30 kg/ m2で–3.46、BMI≥30 kg/ m2で–3.67、BMI不明で–4.92]であった。
3カ月から36ヶ月時点までの平均変化量は、全体で-1.04 ml/分/1.73 m2[BMI <20 kg/ m2で–2.82、BMI 20〜<25 kg/ m2で0.40、BMI 25〜<30 kg/ m2で1.75、BMI≥30 kg/ m2で0.76、BMI不明で0.58]であった。
Expert Opin Drug Saf. 2022 Nov;21(11):1411-1422.
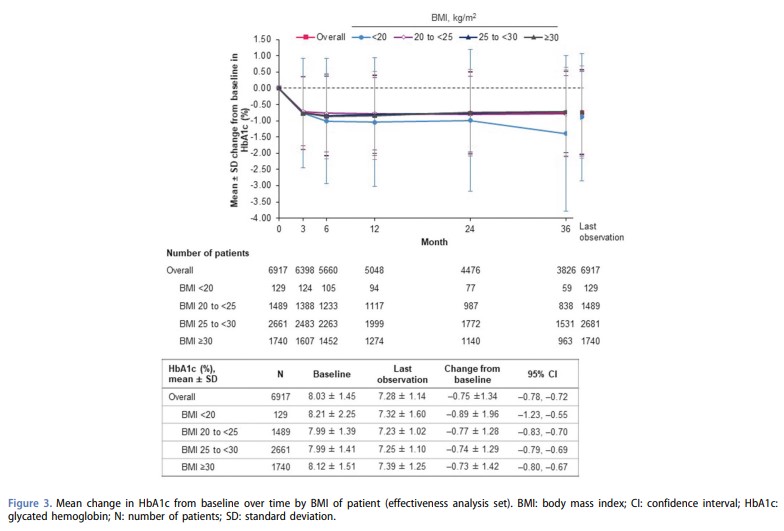
全体のHbA1cはベースラインの平均8.03%から、最終観察時には、平均-0.75% (95% CI: -0.78~-0.72) の減少が示された。
HbA1cの減少はBMI <20 kg/m2で最も大きく減少したが、ベースラインの平均HbA1cも他のBMIサブグループよりも高かった。
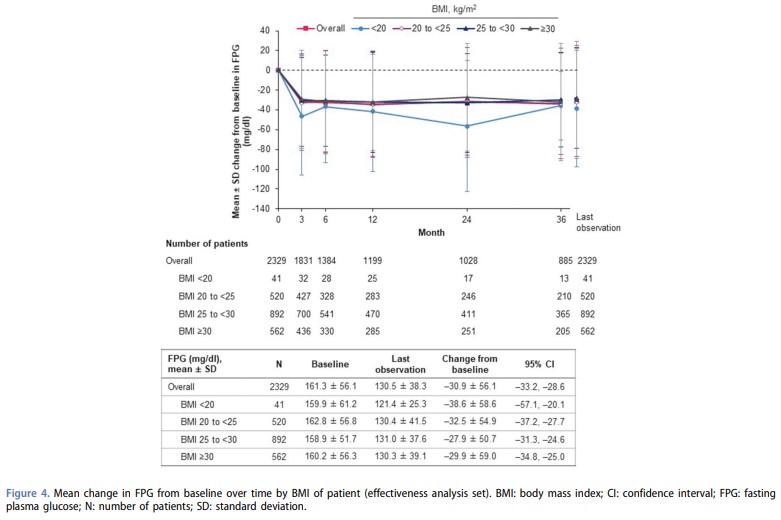
同様に、ベースラインから最終観察時における全体の平均空腹時血糖値(FPG)の減少[-30.9(95%CI -33.2~-28.6)mg/dl]はBMI <20 kg/m2で最も大きく減少したが、ベースラインの平均FPGはBMIサブグループ間で同様であった。
Expert Opin Drug Saf. 2022 Nov;21(11):1411-1422.
結論:
この3年間の市販後調査で、エンパグリフロジン(SGLT2阻害薬)は、BMIに関わらず、日本の実臨床において忍容性が高く、長期にわたり有効であることが示された。
ADR(薬物有害反応)は、これまでの研究および日本におけるエンパグリフロジンの使用実態と一貫しており、新たな安全性の懸念は示されなかった。
さらに、すべてのBMIサブグループにおいて、臨床的に意義のある血糖コントロールの改善が3年間の観察期間にわたり維持された。
BMI<20 kg/m2の患者における平均体重に大きな変化はなかったが、BMIが高い患者では平均して体重がわずかに減少した。
これらの所見は、エンパグリフロジンがBMIに関わらず、低BMIを含むアジア人の心腎リスクと死亡リスクを低下させることを示したEMPA-REG OUTCOME試験のサブグループ解析を補完する。
