PubMed URL:https://pubmed.ncbi.nlm.nih.gov/37164523/
タイトル:Efficacy of Empagliflozin in Patients With Heart Failure Across Kidney Risk Categories
<概要(意訳)>
目的:
心不全(HF)と慢性腎臓病(CKD)は同時に発症する慢性疾患であり、一方の症候群が他方の症候群の発症と進行のリスクを高める。
HFとCKDを併発する患者は、いずれかの疾患を有する患者と比較して、罹患率と死亡率のリスクが高い。
HFは腎灌流を減少させ、腎うっ血を増加させCKDの進行を促進し、逆にCKDは利尿薬や基礎薬物療法の有効性を制限する可能性がある。
HFrEF患者またはHFpEF患者においてCKDがSGLT2阻害薬の有効性に影響を及ぼすかどうかは明らかではない。
EMPEROR(Empagliflozin Outcome Trial in Patients with Chronic Heart Failure)プログラムでは、慢性心不全患者9,718例を対象に、駆出率が低下した患者を登録した試験(EMPEROR-Ruced試験)と、駆出率が維持された患者を登録した試験(EMPEROR-Preserved試験)の2試験が実施された。
これらの試験は、eGFRが20mL/min/1.73m2と低い患者も適格とし、アルブミン尿は除外基準としていない為、両試験のプールデータは、KDIGOのリスク分類におけるエンパグリフロジンの心血管および腎臓への影響を検討する機会を提供することが可能とする。
方法:
EMPEROR-Reduced試験とEMPEROR-Preserved試験の2試験から構成されたEMPERORプログラムは、同じ実行委員会によって実施、イベントは同じエンドポイント判定委員会によって判定、試験は同じ独立データモニタリング委員会によって監督された。
対象患者の条件は18歳以上の男性または女性で、慢性心不全を有し、NYHA機能分類II-IVの症状が3ヵ月以上続いている患者とした。
また、NT-proBNPが高値(左室駆出率が40%以上の場合は300pg/mL以上、36〜40%の場合は2,500pg/mL以上、31〜35%の場合は1,000pg/mL以上、30%以下の場合は600pg/mL以上、または12ヵ月以内のHF入院の既往患者)であることも条件とした。
NT-proBNPの閾値は、心房細動を有する患者ではEMPEROR-Reduced試験で2倍、EMPEROR-Preserved試験で3倍であった。
両試験において、患者は推奨された治療に加えてプラセボまたはエンパグリフロジン(1日10mg)を投与される群に無作為に割り付けられた。
EMPEROR-Reduced試験では、地域、糖尿病の状態、eGFR(60mL/min/1.73m2未満または60mL/min/1.73m2以上)により、EMPEROR-Preserved試験では、同じ変数と左室駆出率(50%未満または50%以上)により層別化された。
プロトコールは、23ヵ国、622ヵ所における治験参加施設の倫理委員会により承認され、全患者が書面によるインフォームド・コンセントを行った。
今回の解析では、ベースラインのeGFRとUACR値を用いて、KDIGO分類システムに従い患者を4つのカテゴリーに分類した。
低リスクは、「eGFR≧60mL/分/1.73m2かつUACR<30mg/g」とした。
中リスクは、「eGFR≧60mL/分/1.73m2かつUACR 30~300mg/gまたはeGFR 45~<60mL/分/1.73m2かつUACR<30mg/g」とした。
高リスクは、「eGFR 60mL/分/1.73m2以上かつUACR 300mg/g以上、eGFR 45~60mL/分/1.73m2未満かつUACR 30~300mg/g、またはeGFR 30~45mL/分/1.73m2未満かつUACR 30mg/g未満」とした。
超高リスクは、「eGFR<60mL/分/1.73m2かつUACR>300mg/g、eGFR<45mL/分/1.73m2かつUACR 30~300mg/g、またはUACRにかかわらずeGFR<30mL/分/1.73m2」とした。
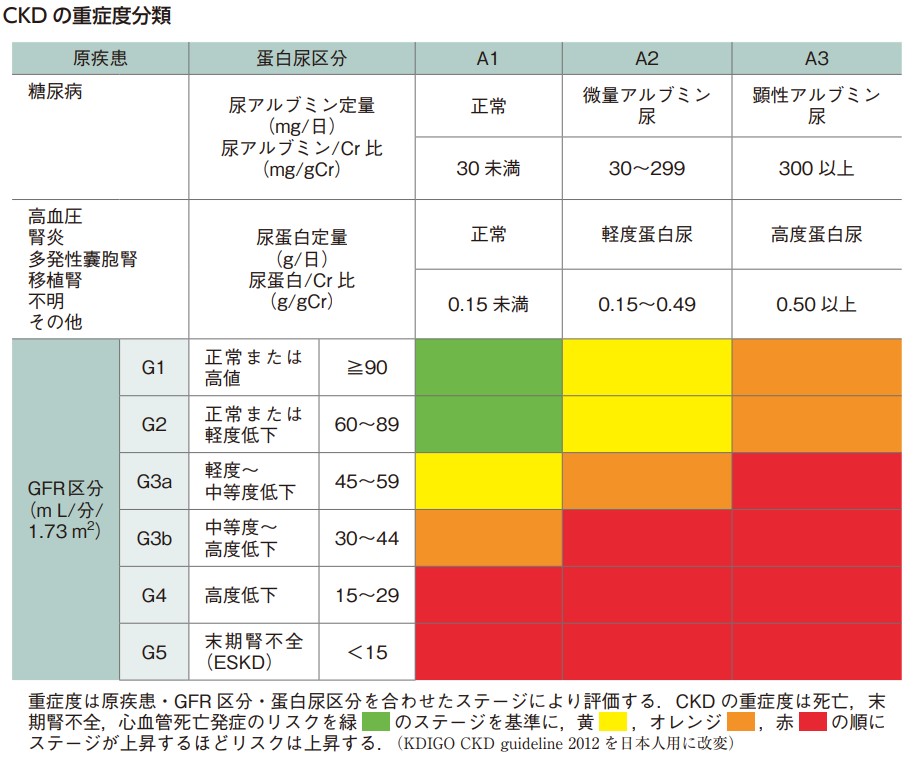
CKD診療ガイド2012より抜粋
本解析の主要なHFアウトカムは、「心血管死またはHF入院までの期間、HF総入院、HF初回入院までの期間、心血管死、カンザスシティ心筋症質問票(KCCQ)により評価した心不全患者のQOL(健康状態)」であった。
腎臓に対するエンパグリフロジンの主な影響は、「eGFR低下率および主要な腎有害転帰の複合」で評価した。
SGLT2阻害薬は、腎疾患の進行に対する効果とは独立した腎内血行動態効果によりeGFRに影響を及ぼす可能性があるため、eGFR低下率は3つの方法で評価した。
- Unconfounded slope(非拘束勾配)法:
ベースラインから試験終了時の無作為化治療中止後30日までのeGFRの低下率を年率換算(測定はいずれもプラセボまたはエンパグリフロジンを投与しない状態で実施)
- Total eGFR slope(総勾配)法:
ベースラインから試験薬投与中の各時点までの変化率で算出
EMPEROR-Reduced試験よりEMPEROR-Preserved試験の観察期間が長いため、EMPEROR-Reduced試験では124週目に、EMPEROR-Preserved試験では124週目と172週目にeGFR低下率を算出した。
このeGFR低下率の測定法では、2つの試験間でエンパグリフロジンの有意な交互作用が認められたため、各試験で別々に解析し、プールデータでは解析しなかった。
- Chronic eGFR slope(慢性勾配)法:
治療薬投与4週時点から試験薬投与中のeGFR変化率を算出
(SGLT2阻害薬の腎内血行動態効果を表すイニシャルディップの影響は除外)
腎複合エンドポイントは、「eGFRの50%以上の持続的低下、または末期腎不全(慢性透析/腎移植、またはベースラインのeGFR 30mL/分/1.73m2以上の患者ではeGFR 15mL/分/1.73m2未満、ベースラインのeGFR30mL/分/1.73m2未満の患者ではeGFR 10mL/分/1.73m2未満または腎死」であった。
このエンドポイントは、腎アウトカムの評価からみた従来のエンドポイントであり、EMPEROR試験プログラムで事前に指定されたものとは異なる。
安全性の転帰には、あらゆる有害事象、重篤な有害事象、治験薬の投与中止に至ったあらゆる有害事象、急性腎不全、体液量減少、尿路感染、骨折、低血糖の確認、性器感染などが含まれた。
結果:
EMPEROR-Reduced試験には3,730例が参加し、この内、3,728例(99.9%)がベースライン時のeGFR値を、3,710例(99.5%)がUACR値を有していた。
EMPEROR-Preserved試験には5,988例が参加し、この内、5,986例(99.9%)がベースライン時のeGFR値を、5,963例(99.6%)がUACR値を有していた。
UACR値が欠如している患者は、UACR値30未満に分類された。
KDIGOの低リスク、中リスク、高リスク、超高リスクに分類された被験者の割合は、それぞれ、32.0%、29.1%、21.9%、17.0%であった。
EMPEROR-Reduced試験とEMPEROR-Preserved試験のコホートでも同様の分布が観察された。
KDIGOのリスク分類が高い患者は低い患者と比較すると、年齢が高く、女性であり、糖尿病、高血圧、心房細動の既往割合が高く、KCCQスコアが低く、心不全重症度(NYHA分類)が高く、NT-Pro BNPが高値であった。
高リスク群では、利尿薬の使用は多かったが、RAS阻害薬やミネラルコルチコイド受容体拮抗薬(MRA)の使用は少なかった。
これらの傾向は、EMPEROR-Reduced試験とEMPEROR-Preserved試験を個々に解析した場合にも観察された。
<ベースラインのKDIGOリスク分類別におけるプラセボ群の転帰>
KDIGOのリスク分類が高い患者ほど、心血管死またはHFによる入院のリスクが高かった(低リスク群6.78例、中リスク群11.30例、高リスク群15.15例、超高リスク群20.70例/100人 年当り;交互P値<0.001)。
同様のパターンが、
HFの総入院(低リスク群6.69例、中リスク群10.56例、高リスク群16.60例、超高リスク群22.16例/100人 年当り;交互P値<0.001)、
HFの初回入院(低リスク群4.46例、中リスク群7.68例、高リスク群11.14例、超高リスク群15.98例/100人 年当り;交互P値<0.001)、
心血管死(低リスク群2.98例、中リスク群5.31例、高リスク群5.69例、超高リスク群7.60例/100人 年当り;交互P値<0.001)でもみられた。
KCCQ-CSSの経時的な改善の程度は、KDIGOリスク分類の超高リスク群で最も小さかった(52週目で低リスク群4.06、中等度リスク群3.22、高リスク群2.98、超高リスク群1.14;傾向P値=0.001)。
EMPEROR-Reduced試験とEMPEROR-Preserved試験を個々に解析しても同様の結果が得られた。
KDIGOの低リスク分類と比較すると、高リスク分類ではeGFR低下率が小さかった。
Unconfounded slope(非拘束勾配)法で算出したeGFR低下率は、超高リスク群の患者で年平均0.5~1.5mL/分/1.73m2、低リスク群の患者で年平均2.5~4.0mL/分/1.73m2であった(傾向P値<0.0001)。
同様の結果は、Total eGFR slope(総勾配)法とChronic eGFR slope(慢性勾配)法で算出したeGFR低下率でも認められ、その結果はEMPEROR-Reduced試験とEMPEROR-Preserved試験で一貫していた。
しかしながら、eGFR低下率の傾向パターンとは対照的に、ベースラインのKDIGOリスク分類が高い患者は、腎複合エンドポイントのリスクが高かった(低リスク0.42、中リスク1.16、高リスク1.41、超高リスク3.63/100人 年当り;傾向P値<0.0001)。
EMPEROR-Reduced試験のコホートとEMPEROR-Preserved試験のコホートでも、一貫した結果が得られた。
<ベースラインのKDIGOリスク分類別におけるエンパグリフロジンの転帰>
エンパグリフロジンは、すべてのKDIGOリスク分類において心血管死またはHFによる入院のリスクを一貫して減少させた[低リスク群HR 0.81(95%CI 0.66-1.01)、中リスク群HR 0.63(95%CI 0.52-0.76)、高リスク群 HR 0.82(95%CI 0.68-0.98)、超高リスク群 HR 0.84(95%CI 0.71-1.01); 傾向P値=0.30)]。
同様に、KDIGOリスク分類別におけるHF総入院(傾向P値=0.82)またはHF初回入院までの期間(傾向P値=0.19)に対しても、エンパグリフロジンの一貫した結果が示された。
一方で、KDIGOリスク分類に関わらず、心血管死(傾向P値=0.683)または全死亡(傾向P値=0.876)におけるリスク減少は示されなかった。
エンパグリフロジンは、KDIGOの全リスク分類において、52週時点におけるKCCQ-CSS(心不全患者のQOL)を同様に改善した。
すべてのHFエンドポイントについて、EMPEROR-Reduced試験とEMPEROR-Preserved試験で同様の傾向であった。
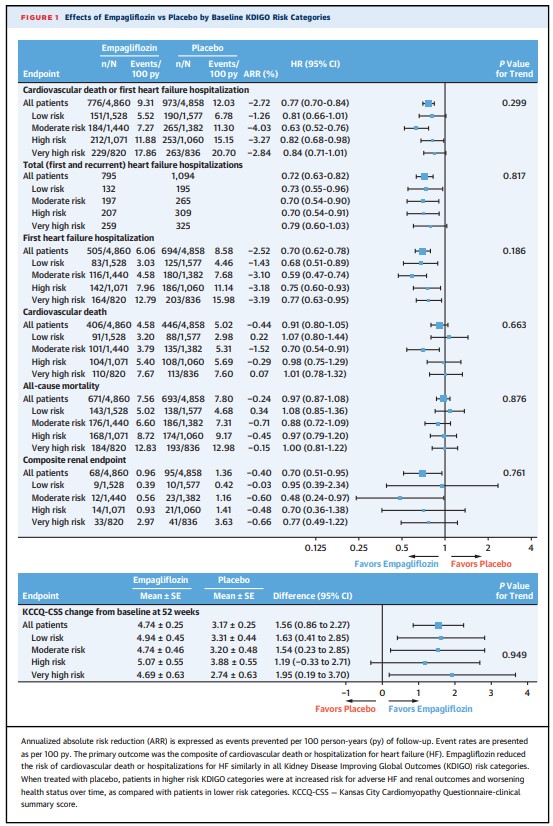
J Am Coll Cardiol. 2023 May 16;81(19):1902-1914.
<推定年間eGFR低下率と腎転帰>
エンパグリフロジンのKDIGOリスク分類別の各時点におけるeGFRに対する効果を、プールデータおよび個々の試験について補足図10~12に示す。
EMPEROR-Reduced試験とEMPEROR-Preserved試験にける、Unconfounded slope(非拘束勾配)法、Total eGFR slope(総勾配)法、Chronic eGFR slope(慢性勾配)法の3つの方法で算出したeGFR低下率に対する本剤の影響を、図2および3に別々に示す。
Total eGFR slope(総勾配)法で算出したeGFR低下率に対するエンパグリフロジンの影響は、EMPEROR-Reduced試験の方がEMPEROR-Preserved試験よりも有意に大きかった為(124週時点で0.87mL/分/1.73m2 vs 0.10mL/分/1.73m2 ; 交互P値=0.023)、この方法で算出したデータはプールされなかった。
Unconfounded slope(非拘束勾配)法で算出したeGFR低下率に対するエンパグリフロジンの影響は、EMPEROR-Reduced試験およびEMPEROR-Preserved試験のいずれにおいても有意な抑制効果を示し、KDIGOのリスク分類においても同様の結果を示した(EMPEROR-Reduced試験の傾向P値=0.35、EMPEROR-Preserved試験の傾向P値= 0.57)。
すべての解析において、Unconfounded slope(非拘束勾配)法で算出したeGFR低下率に対する影響と比較すると、Total eGFR slope(総勾配)法で算出したeGFR低下率の影響は小さかった。
しかしながら、Chronic eGFR slope(慢性勾配)法で算出したEMPEROR-Reduced試験およびEMPEROR-Preserved試験におけるeGFR低下率の影響は、Unconfounded slope(非拘束勾配)法と比較して、同等またはそれ以上であった(図2および3)。
Chronic eGFR slope(慢性勾配)法で算出したeGFR低下率の影響において、EMPEROR-Reduced試験では、低リスク分類と比較して高リスク分類でエンパグリフロジンの影響は小さかった(傾向P値=0.015)が、EMPEROR-Preserved試験ではその傾向は示さなかった(傾向P値=0.62)。
いずれの試験においても、eGFR低下率の3つの算出方法を用いた場合、KDIGOリスク分類がエンパグリフロジンの転帰に対する影響に及ぼす明らかな影響は認められなかった(図2および3)。
両試験のプールデータでは、腎複合エンドポイントに対するエンパグリフロジンの影響は、KDIGO分類のリスクが最も低い患者で最も小さかった[HR 0.95(95%CI:0.39-2.34)]が、各リスクカテゴリーのイベント数は少なく、有意な傾向は示されなかった(傾向P値=0.76)。
個々の試験のデータはまばらで、腎複合エンドポイントに対するKDIGOリスク分類の影響を評価することはできなかった(補足図8および9)。
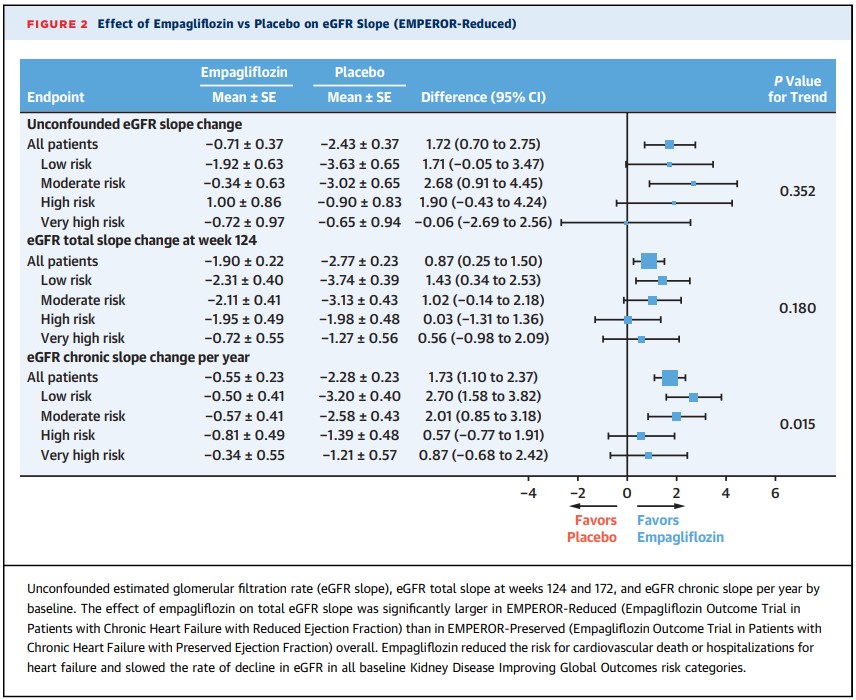
J Am Coll Cardiol. 2023 May 16;81(19):1902-1914.
<安全性アウトカム>
エンパグリフロジンのKDIGOリスク分類における安全性転帰への影響を補足表3に概説する。
観察されたエンパグリフロジンの有害事象は、KDIGOリスク分類の影響はなかった。
<考察>
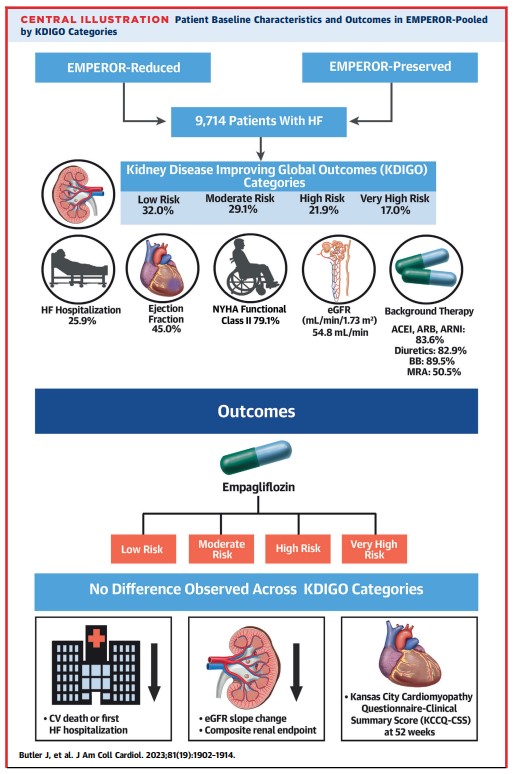
このEMPEROR-Pooled解析では、いくつかの重要な所見が示された(中央図)。
第一に、プラセボで治療された場合、KDIGO分類のリスクが高い患者は、低い患者と比較して、有害なHFおよび腎アウトカムのリスクが高く、健康状態が経時的に悪化した。
第二に、エンパグリフロジンは、ベースラインにおけるKDIGO分類のすべてのリスクカテゴリーにおいて、心血管死またはHFによる入院のリスクを減少させ、eGFR低下速度を遅らせた。
この所見は、EMPEROR-Reduced試験およびEMPEROR-Preserved試験において一貫していた。
第3に、3つの方法により算出したeGFR勾配に基づく結果は、その算出方法に大きく依存した。
EMPEROR-Reduced試験とEMPEROR-Preserved試験の合計9,714例のHF患者をKDIGOリスク分類に層別化し、低リスク患者32.0%、中リスク患者29.1%、高リスク患者21.9%、超高リスク患者17.0%とした。
プールされた集団の主なベースラインの特徴を説明する。
ベースラインにおけるKDIGO分類のすべてのリスクカテゴリーにおいて、エンパグリフロジンは、心血管死またはHFの初発入院のリスクを減少させ、eGFR低下速度を遅らせ、52週時点のKCCQ-CSSスコア(QOL)を増加させた。
これまでにHF患者を対象とした臨床試験で、KDIGOのリスク分類に応じた臨床転帰を検討した試験はない。
PARAGON-HF試験(HFpEF患者を対象としたサクビトリルバルサルタン vs バルサルタン)は、PARADIGM-HF試験(HFrEF患者を対象としたサクビトリル/バルサルタン vs エナラプリル)、TOPCAT試験(HFpEF患者を対象としたスピロノラクトン vs プラセボ)において、ベースラインのeGFR 60mL/min/1.73m2未満と以上の患者では、それぞれ、サクビトリル/バルサルタンまたはスピロノラクトンに同様の結果がみられた。
SGLT2阻害薬の2つの大規模試験(DAPA-HF試験[HFrEF患者を対象としたダパグリフロジン vs プラセボ]およびDELIVER試験[HFpEF患者を対象としたダパグリフロジン vs プラセボ])において、ベースラインのeGFR 60mL/min/1.73m2未満と以上に関わらず、ダパグリフロジンの一貫した結果が示された。
注目すべき点は、これらの試験では最も進行した腎臓病(eGFR<30mL/min/1.73m2)の患者を除外しており、UACRはPARADIGM-HF試験でのみ収集された。
対照的に、EMPERORプログラム(EMPEROR-Reduced試験とEMPEROR-Preserved試験)ではUACRを測定し、eGFR 20mL/min/1.73m2という腎機能低値の患者も含まれていた。
したがって、われわれの解析はKDIGOのリスク分類をHFの大規模試験に適用した最初のものである。
2型糖尿病患者を対象とした3つの試験(EMPA-REG OUTCOME試験 [エンパグリフロジン]、CANVAS試験 [カナグリフロジン]、VERTIS-CV試験およびVERTIS-CV 試験[エルツグリフロジン])では、KDIGO分類のリスクが高い患者ほど、リスクの低い患者と比較して、主要なHFまたは腎の有害事象リスクが高かった。
しかし、EMPA-REG OUTCOME試験とCANVAS試験では、SGLT2阻害薬によるHFと腎臓のアウトカムにおける相対リスク低下は、ベースラインのKDIGOのリスク分類に関わらず同程度であり、治療による絶対リスク低下は高リスクと超高リスクの患者で最大であった。
一方で、VERTIS-CV試験では、ベースラインのKDIGOのリスク分類は、心血管死およびHFによる入院に対するエルツグリフロジンの相対リスク減少に有意な影響を及ぼし、KDIGO分類の低リスク患者では、治療効果はほとんど認められなかった(交互P値=0.03)。
DAPA-CKD試験では、CKDに対するダパグリフロジンの効果はKDIGOのリスク分類に関わらず一貫していたが、この試験では最もリスクの低い患者は登録されなかった。
EMPEROR試験プログラムでは、HF患者のHFまたは腎アウトカムに対するエンパグリフロジンの効果はKDIGOのリスク分類に関わらず一貫しており、EMPA-REG OUTCOME試験およびCANVAS試験で報告されたものと同様の傾向が示された。
さらに、健康関連のQOL改善はKDIGOのすべてのリスク分類で観察された。
この結果は、アンジオテンシン受容体ネプリライシン阻害薬などの他のHF治療薬で観察された結果と一致している。
腎の重要な転帰を評価するのに十分なパワーがない臨床試験においては、eGFR低下率に対する治療効果の大きさを代用指標として用いることが提案されている。
eGFR勾配の群間差を検討する解析により、主要な腎イベントを評価するためにデザインされた試験よりも小規模で短期間の試験で薬効を識別できることが期待されている。
0.5~1.0mL/分/1.73m2の群間差は、腎有害転帰のリスクを30%減少させることを予測するのに使えると提唱する人もいる。
しかし、eGFR勾配の計算には数多くのアプローチが可能であり、利用可能なモデルはデータの除外や基礎となる仮定において大きく異なり、一般的に使用されているモデルは著しく異なる結果をもたらし、観察された結果と重要な不一致を示す可能性がある。
実際に、eGFR勾配の解析が上手くいくのは、治療前のeGFRが高い場合、治療がeGFRに即効性がない場合、十分な試験期間がある場合だけであるという意見もある。
SGLT2阻害薬の大規模試験に登録された慢性心不全患者には、eGFR勾配の信頼性に関するこれらの前提条件は、いずれも当てはまらない。
典型的な軽度〜中等度HF患者のeGFRは約60〜65mL/min/1.73m2であり、追跡期間は平均1.5〜2.5年に過ぎず、SGLT2阻害薬は腎内血行動態作用によりeGFRを低下させる即時可逆的効果(イニシャルディップ)を有する。
そのため、eGFR勾配を計算するために、この初期の勾配を除外し、治療中の値のみに基づいてeGFRの勾配を推定し、ベースライン値を除外する研究者もいる。
これは “慢性勾配 “と呼ばれるアプローチ[Chronic eGFR slope(慢性勾配)法]である。
また、ベースライン値を含めることを余儀なくされ、2-コンパートメントモデルを用いて ““総勾配”を計算しようとする研究者もいる。
線形性が存在しないにもかかわらず、この計算では(特定の時点における)1年ごとの低下に対する単一の値が得られるが、これは基礎となるデータも病態生理学も表していない。
重要なことは、このモデルではSGLT2阻害薬で治療された患者における治療中のすべてのeGFR値の可逆的な低下を説明できないことである。
EMPEROR試験のデータを分析する際、無作為化治療中止後30日のeGFRを測定した為、
「慢性勾配(Chronic eGFR slope)法」と「総勾配(Total eGFR slope)法」モデルの両方に内在する困難を回避することができた。
このベースライン値とオフトリートメント値を比較することで、薬剤の有無に左右されないeGFRの年変化量を推定することができた。
本稿では、この方法を 「非拘束勾配(uncfounded eGFR slope)法」と呼ぶ。
我々は、「非拘束勾配(uncfounded eGFR slope)法:ベースラインから無作為化治療中止30後までの期間を対象」によりeGFRの推定年間低下速度を算出した為、患者における「慢性勾配(Chronic eGFR slope)法:イニシャルディップの影響を除く、治療薬投与4週後から治療薬投与終了までの期間を対象」と「総勾配(Total eGFR slope)法:ベースラインから治療薬投与終了までの期間を対象」の価値を包括的に評価することができた。
プラセボ群では、腎有害転帰の低リスク患者と比較して、このリスクが最も高い患者におけるeGFR勾配の低下はかなり緩やかであり、腎機能が低下した患者ではeGFR勾配の絶対的な変化は信頼できないという推奨が再確認された。
さらに重要な点として、エンパグリフロジンの全eGFR勾配に対する効果の大きさは、「非拘束勾配(uncfounded eGFR slope)法」に対する効果と比較して小さく、「慢性勾配(Chronic eGFR slope)法」に対する効果の大きさは一般的に大きかった。
この観察結果は、「総勾配(Total eGFR slope)法」は、SGLT2阻害薬の真の治療効果を著しく過小評価する可能性が高いことを示している。
最後に、KDIGOのリスク分類全体において、エンパグリフロジンのeGFR勾配に対する効果は、腎転帰に対する本剤の効果と密接に一致しなかったが、この観察は、特に低リスク患者における腎イベントの数が少ないために制限されている。
今回の解析の主な限界は、二重盲検療法の期間が比較的短く、eGFRの変化と腎臓の主な有害転帰の発生を関連付ける能力に限界があったことである。
結論:
エンパグリフロジンは、EMPEROR-Reduced試験およびEMPEROR-Preserved試験のデータをプール解析した場合、別々に解析した場合でも、KDIGOの全てのリスク分類において心血管死またはHF入院のリスクを減少させた。
「総勾配(Total eGFR slope)法:ベースラインから治療薬投与終了までの期間を対象」を用いた場合、SGLT2阻害薬のイニシャルディップによる腎内血行動態への影響が含まれる為、eGFR勾配に対するSGLT2阻害薬の真の治療効果を過小評価する可能性がある。
J Am Coll Cardiol. 2023 May 16;81(19):1902-1914.